1��ѡ���� Ԫ��R�����·�Ӧ��RO3����5R����6H��===3R2��3H2O������˵����ȷ���ǣ�?��
A��Ԫ��Rλ�����ڱ��еڢ�A��
B��RO3���е�Rֻ�ܱ���ԭ
C��ÿ��Ӧ����1 mol RO3����ת�Ƶ��ӵ����ʵ���Ϊ5 mol
D��R2�ڳ��³�ѹ��һ��������
�ο��𰸣�C
������������ݷ�Ӧʽ��֪��R����ͼ��ǣ�1�ۣ���������ǣ�7�ۣ���R�ǵڢ�AԪ�ء�RO�е�R���ϼ��ǣ�5�ۣ������м��̬�����ܱ���ԭ��Ҳ�ܱ�����������Ҳ�������壬����ֻ��ѡ��C����ȷ�ģ���ѡC��
�����Ѷȣ���
2��ѡ���� X��Y��Z��ԭ���������ε����Ķ�����Ԫ�أ�3��Ԫ�ص�ԭ�Ӻ��������֮����Ca2���ĺ����������ȣ�X��Z�ֱ�õ�һ�����Ӻ���γ�ϡ������ԭ�ӵ��ȶ����Ӳ�ṹ������˵����ȷ����
A��ԭ�Ӱ뾶��Z��Y��X
B��Z��X�γɻ�����ķе����Z��ͬ��Ԫ����X�γɻ�����ķе�
C��CaY2��ˮ����������ԭ��Ӧʱ��CaY2ֻ��������
D��CaX2��CaY2��CaZ2��3�ֻ������У��������������Ӹ����Ⱦ�Ϊ1�U2
�ο��𰸣�B
���������Ca2+�ĺ��������Ϊ18��X���ڷֱ�õ�һ�����Ӻ���γ�ϡ������ԭ�ӵ��ȶ����Ӳ�ṹ˵��X��Z���γɸ�1�����ӣ���XΪH��ZΪF����X������ΪF��Z������ΪCl���ɴ˿ɽ�һ���Ƴ�YΪO��ԭ�Ӱ뾶��O>F>H��A�����HF���Ӽ�������������е���ͬ����Ԫ���⻯������ߵģ�B����ȷ��CaO2��ˮ������Ӧʱ��O22���绯��������������������ԭ����C�����CaO2�е��������������Ӹ����Ⱦ�Ϊ1:1��D�����
�����㶨λ�����⿼�������Ԫ�ص������ƶϺ�Ԫ�����ڱ�֪ʶ��
�����Ѷȣ�һ��
3������� ��7�֣�����ͼ�����ڱ��ж����ڵ�һ���֣�A.B.C����Ԫ�ص�ԭ�Ӻ��������֮�͵���B����������2����
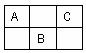
1��(��Ԫ�ط��ű�ʾ)A?B?C?
2��B�����������Ļ�ѧʽ?������?���塣
3��C����̬�⻯��Ļ�ѧʽ?�����д���?����
�ο��𰸣�(7��)? N? S? F? SO3?����? HF?����
�����������
�����Ѷȣ�һ��
4��ѡ���� ���и���Ԫ���������������ƶ���ȷ����
A��Na��Mg��Al�Ļ�ԭ��������ǿ
B��HF��HCl��HBr���ȶ���������ǿ
C��H3PO4��H2SO4��HClO4������������ǿ
D��NaOH��KOH��CsOH�ļ������μ���
�ο��𰸣�C
���������ͬ�����������ң��������������ǽ���������ǿ������������ˮ�������������ǿ��A����ȷ��C��ȷ��ͬ�������϶��½���������ǿ������������ˮ����ļ�������ǿ���ǽ�������������Ӧ�⻯����ȶ�������������BD���Ǵ���ģ���ѡC��
�����Ѷȣ���
5��ѡ���� ����˵������ȷ����
A.1mol FeCl3ת���������������������NA����������������
B.�����ЧӦ����Һ�ͽ���ı�������
C.��Fe��OH��3�����в�������ʯī�缫��ֱͨ���磬��������Һ����ɫ����
D.���ײ�����ֱ��һ��Ӽ�������ʮ���ף�������ײ������ڽ���
�ο��𰸣�C
���������������A�������������������ļ����壻
B����ɢϵ�ı�����������ֱ����С��
C����������������������������ӣ�ͨ������������
D�����ײ�����ֱ��һ��Ӽ�������ʮ�����Ƿ�ɢ�ʣ�
���A�������������������ļ����壬1mol FeCl3ת�����������������������������������С��NA������A����
B�������ЧӦ����Һ�ͽ���ļ�������ɢ����ֱ���Ĵ�С�DZ������𣬹�B����
C��������������������������ӣ�ͨ������������������Ӿ����C��ȷ��
D�����ײ�����ֱ��һ��Ӽ�������ʮ�����Ƿ�ɢ�ʣ��ڷ�ɢ�����γɽ��������D����
��ѡC��
���������⿼���˽�������Ӧ�ã��������𣬽��������������ú͵�Ӿ����ķ����жϣ��ϼ�
�����Ѷȣ�һ��