1、填空题 由amolFe+bmolFe2O3组成的混和物,用足量的盐酸溶解。随着a/b的不同,反应产物各不相同。按照a/b的不同比值,结合有关氧化还原的反应竞争顺序,填写下列表格内容。表格可不填满,若不足可添加表格。
a/b
| 氧化还原反应主要产物
| 有关的离子方程式
|
?
| ?
| ?
|
?
| ?
| ?
|
?
| ?
| ?
|
?
| ?
| ?
|
?
| ?
| ?
参考答案:(14分,每个1分,)
a/b
氧化还原反应产物
有关的离子方程式
a/b<1
FeCl2
Fe2O3+6H+=2Fe3++3H2O;2Fe3++Fe=3Fe2+
a/b=1
FeCl2
Fe2O3+6H+=2Fe3++3H2O;2Fe3++Fe=3Fe2+
a/b>1
FeCl2?H2
Fe2O3+6H+=2Fe3++3H2O;2Fe3++Fe=3Fe2+;Fe+2H+=Fe2++H2↑
本题解析:本题所涉及到的常见氧化性离子的氧化性顺序为:Fe3+>H+;
当a=b时,Fe2O3+6H+=Fe3++3H2O,生成的Fe3+恰好被铁还原:2Fe3++Fe=3Fe2+;
当a>b时,铁过量,Fe2O3+6H+=Fe3++3H2O生成的Fe3+被部分铁还原:2Fe3++Fe=3Fe2+,余下的铁:Fe+2H+=Fe2++H2↑
当a<b时,铁不足,Fe2O3+6H+=Fe3++3H2O,生成的Fe3+被铁还原后仍有剩余:2Fe3++Fe=3Fe2+;
本题难度:一般
2、选择题 下列说法正确的是
A.金属原子失电子越多,其还原性越强
B.CH4的摩尔质量为16g
C.10 mL质量分数为98%的H2SO4,用水稀释至100 mL,H2SO4的质量分数为9.8%
D.电解质物质本身可能导电
|
参考答案:D
本题解析:A、金属的还原性取决于失电子难易,和失电子多少无关,如钠失去一个电子,铝失去3个电子,钠的金属性大于铝,A错误;B、CH4的摩尔质量为16g/mol,B错误;C、10mL质量分数为98%的H2SO4,用水稀释至100mL,由于硫酸溶液的密度大于水的密度,所以稀释后H2SO4的质量分数大于9.8%,C错误;D、电解质物质本身可能导电,例如熔融的氯化钠,正确,选D。
考点:考查还原性强弱的判断,摩尔质量的概念,溶液的稀释,电解质等知识。
本题难度:一般
3、选择题 已知2FeCl3?+?2KI?=?2FeCl2?+?2KCl?+?I2,H2S?+?I2?=?2HI?+?S,下列叙述正确的是
[? ]
A.?氧化性:Fe3+>I2>S?
B.?氧化性:I2>S>Fe3+
C.?还原性:Fe2+>I->H2S?
D.?还原性:Fe2+>H2S>I-
参考答案:A
本题解析:
本题难度:一般
4、实验题 某小组同学为探究H2O2、H2SO3、Br2氧化性强弱,设计如下实验(夹持仪器已略去,装置的气密性已检验)。
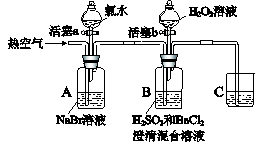
实验记录如下:
?
| 实验操作
| 实验现象
|
I
| 打开活塞a,滴加氯水,关闭活塞a
| A中溶液变为红棕色。
|
II
| 吹入热空气
| A中红棕色明显变浅;B中有气泡,产生大量白色沉淀,混合液颜色无明显变化。
|
III
| 停止吹入空气,打开活塞b,逐滴加入H2O2溶液
| 开始时颜色无明显变化;继续滴加H2O2溶液,一段时间后,混合液逐渐变成红棕色。
|
?
请回答下列问题:
(1)A中反应的离子方程式是?。
(2)实验操作II吹入热空气的目的是?。
(3)装置C的作用是?,C中盛放的药品是?。
(4)实验操作III,混合液逐渐变成红棕色,其对应的离子方程式?。
(5)由上述实验得出的结论是?。
(6)实验反思:
①有同学认为实验操作II吹入的热空气,会干扰(5)中结论的得出,你认为是否干扰,理由是?。
②实验操作III,开始时颜色无明显变化的原因是(写出一条即可):?
?。
参考答案:(16分,每空2分)
(1)2Br-+Cl2=Br2+2Cl-
(2)吹出单质Br2
(3)吸收尾气? NaOH溶液
(4)H2O2+2Br-+2H+=Br2+2H2O
(5)氧化性:H2O2>Br2>H2SO3
(6)
① 不干扰,无论热空气是否参加氧化H2SO3,只要观察到产生白色沉淀的同时无明显颜色变化,即能证明Br2氧化了H2SO3
② H2SO3有剩余(H2O2浓度小或Br-与H2O2反应慢等因素都可)
本题解析:(1)氯水中的Cl2置换Br?。
(2)利用Br2的挥发性,吹入热空气使Br2挥发。
(3)因为Cl2、Br2有毒,所以C中盛放NaOH溶液,除去尾气中的有毒气体,防止污染环境。
(4)混合液逐渐变成红棕色,说明H2O2把Br?氧化为Br2,配平可得离子方程式。
(5)根据氧化剂的氧化性大于氧化产物,可知:H2O2>Br2>H2SO3。
(6)①溶液无明显颜色变化,说明Br2参加了反应,即氧化了H2SO3。
②实验操作III发生的反应为H2O2氧化Br?,开始时颜色无明显变化,说明反应收到了影响,H2SO3有剩余、H2O2浓度小、Br-与H2O2反应慢等都是可能因素。
本题难度:困难
5、选择题 实现下列反应需要加入氧化剂的是(?)
A.NaOH →Na2CO3
B.SO2→SO3
C.H2SO4→H2
D.CaCO3→CO2
参考答案:B
本题解析:根据选项中存在元素的化合价升高的变化可知,选项中的物质具有还原性,则需要加入合适的氧化剂来实现氧化还原反应.
A. NaOH →Na2CO3的反应中,各元素的化合价没有发生变化,故A不选
B、SO2→SO3中S元素的化合价升高,则需要加入合适的氧化剂来实现,如加入氧气,故B选;.
C. H2SO4→H2中H元素的化合价降低,则需要加入合适的还原剂来实现,如加入铁,故C不选;
D、CaCO3→CO2的反应中,各元素的化合价没有发生变化,故D不选;
故选B
本题难度:简单