1ЎўјтҙрМв БӘ°ұЈЁN2H4Ј©ј°ЖдСЬЙъОпКЗТ»АаЦШТӘөД»рјэИјБПЈ®N2H4УлN204·ҙУҰДЬ·ЕіцҙуБҝөДИИЈ®
ЈЁ1Ј©ТСЦӘЈә2N02ЈЁgЈ©ЁTN204ЈЁgЈ©ЎчH=Т»57.20kJ?mol-Ј®Т»¶ЁОВ¶ИПВЈ¬ФЪГЬұХИЭЖчЦР·ҙУҰ2N02ЈЁgЈ©?
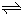
?N204ЈЁgЈ©ҙпөҪЖҪәвЈ®ЖдЛыМхјюІ»ұдКұЈ¬ПВБРҙлК©ДЬМбёЯNOzЧӘ»ҜВКөДКЗ______ЈЁМоЧЦДёЈ©
AЈ®јхРЎN02өДЕЁ¶И?BЈ®ҪөөНОВ¶И?CЈ®ФцјУN02өДЕЁ¶И?DЈ®ЙэёЯОВ¶И
ЈЁ2Ј©17ЎжЎў1.0IЎБ105PaЈ¬2LГЬұХИЭЖчЦРN204әНN02өД»мәПЖшМеҙпөҪЖҪәвКұЈ¬ҙжФЪOЈ®0600molN02Ј¬0.0240mol?N204Ј®ФтҙЛ·ҙУҰ2N02ЈЁgЈ©
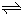
N204ЈЁgЈ©өДЖҪәвіЈКэK______Ј»
ИфјхЙЩИЭЖчМе»эЈ¬ФтЖҪәвіЈКэK______ЈЁМоЎ°ФцҙуЎұЎўЎ°јхРЎЎұ»тЎ°І»ұдЎұЈ©Ј®
ИфЙэёЯМеПөОВ¶ИЈ¬ФтЖҪәвіЈКэK______ЈЁМоЎ°ФцҙуЎұЎўЎ°јхРЎЎұ»тЎ°І»ұдЎұЈ©Ј®
2ЎўМоҝХМв ЈЁ1Ј©ОӘМҪҫҝУГCO2АҙЙъІъИјБПјЧҙјөД·ҙУҰФӯАнЈ¬ПЦҪшРРИзПВКөСйЈәФЪМе»эОӘ1LөДГЬұХИЭЖчЦРЈ¬ідИл1mol
CO2әН3molH2Ј¬Т»¶ЁМхјюПВ·ўЙъ·ҙУҰЈәCO2(g)+3H2(g)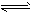 CH3OH(g)+H2O(g) ЎчH=-49.0kJ/mol ІвөГCO2әН
CH3OH(g)+H2O(g) ЎчH=-49.0kJ/mol ІвөГCO2әН
CH3OHЈЁgЈ©өДЕЁ¶ИЛжКұјдұд»ҜИзНјЎЈЗл»Шҙр
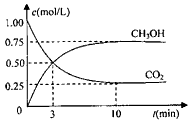
ўЩ ҙУ·ҙУҰҝӘКјөҪЖҪәвЈ¬ЗвЖшөДЖҪҫщ·ҙУҰЛЩВКЈәv(H2)=________mol/ЈЁLЎӨminЈ©ЎЈ
ўЪЙэёЯОВ¶ИЈ¬ёГ·ҙУҰөДЖҪәвіЈКэөДКэЦөҪ«________ЈЁМоЎ°ФцҙуЎұЎўЎ°јхРЎЎұ»тЎ°І»ұдЎұЈ©ЎЈ
ўЫПВБРҙлК©ЦРДЬК№ЖҪәв»мәПОпЦРnЈЁCH3OHЈ©/nЈЁCO2Ј©ФцҙуөДКЗ________
AЈ®јУИлҙЯ»ҜјБ
BЈ®ідИлHeЈЁgЈ©Ј¬К№МеПөС№ЗҝФцҙу
CЈ®Ҫ«H2OЈЁgЈ©ҙУМеПөЦР·ЦАл
DЈ®ФЩідИл3molH2
ЈЁ2Ј©әПіЙ°ұөДИИ»ҜС§·ҪіМКҪОӘЈәN2(g)+3H2(g)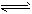 2NH3(g) ЎчH=-92 kJЎӨmol-1ЎЈ
2NH3(g) ЎчH=-92 kJЎӨmol-1ЎЈ
ўЩДіОВ¶ИПВЈ¬Иф°С10mol N2Ул30mol H2ЦГУЪМе»эОӘ10LөДГЬұХәПіЙЛюДЪЈ¬·ҙУҰҙпөҪЖҪәвЧҙМ¬КұЈ¬ІвөГЖҪәв»мәПЖшМеЦР°ұөДМе»э·ЦКэОӘ1/5Ј¬ФтёГОВ¶ИПВ·ҙУҰөДK=___________ЈЁҝЙУГ·ЦКэұнКҫЈ©ЎЈ
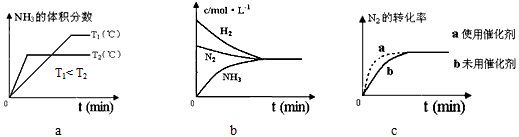
ўЪ¶ФУЪәПіЙ°ұ·ҙУҰ¶шСФЈ¬ПВБРУР№ШНјПуТ»¶ЁХэИ·өДКЗЈЁМоРтәЕЈ©_______________
3ЎўМоҝХМв ЈЁ14·ЦЈ©ОӘБЛјхЙЩГәИјЙХ¶ФҙуЖшФміЙөДОЫИҫЈ¬ГәөДЖш»ҜәНТә»ҜКЗёЯР§ЎўЗеҪаАыУГГәМҝөДЦШТӘНҫҫ¶Ј¬¶шјхЙЩCO2ЖшМеөДЕЕ·ЕТІКЗИЛАаГжБЩөДЦШҙуҝОМвЈ®ГәЧЫәПАыУГөДТ»ЦЦНҫҫ¶ИзПВЛщКҫЈә
ЈЁ1Ј©ТСЦӘЈәC(s)+H2O(g)====CO(g)+H2(g) ЎчH1=+131.3kJ?mol-1
C(s)+2H2O(g)====CO2(g)+2H2(g) ЎчH2=+90kJ?mol-1
ФтТ»Сх»ҜМјУлЛ®ХфЖш·ҙУҰЙъіЙ¶юСх»ҜМјәНЗвЖшөДИИ»ҜС§·ҪіМКҪКЗ ЎЈ
ЈЁ2Ј©Ҫ«ИјГә·ПЖшЦРөДCO2ЧӘ»ҜОӘ¶юјЧГСөД·ҙУҰФӯАнОӘЈә2CO2(g)+6H2(g)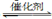 CH3OCH3(g)+3H2O(g)Ј»ҰӨH
CH3OCH3(g)+3H2O(g)Ј»ҰӨH
ўЩёГ·ҙУҰЖҪәвіЈКэұнҙпКҪОӘKЈҪ ЎЈ
ўЪТСЦӘФЪДіС№ЗҝПВЈ¬ёГ·ҙУҰФЪІ»Н¬ОВ¶ИЎўІ»Н¬Н¶БПұИКұЈ¬CO2өДЧӘ»ҜВКИзНјЛщКҫЎЈ
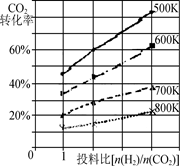
ёГ·ҙУҰөДҰӨH________(МоЎ°>ЎұЎўЎ°<Ўұ»тЎ°ЈҪЎұ)0ЎЈИфОВ¶ИІ»ұдЈ¬јхРЎ·ҙУҰН¶БПұИ[n(H2) /n(CO2)]Ј¬ФтKҪ«________(МоЎ°ФцҙуЎұЎўЎ°јхРЎЎұ»тЎ°І»ұдЎұ)ЎЈ
ЈЁ3Ј©Т»ЦЦРВРНЗвСхИјБПөзіШ№ӨЧчФӯАнИзПВНјЛщКҫЎЈ
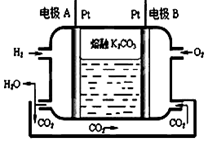
ўЩРҙіцөзј«AөДөзј«·ҙУҰКҪ ·Еөз№эіМЦРЈ¬ИЬТәЦРөДCO32-Ҫ«ТЖПтөзј« ЈЁМоA»тBЈ©
ўЪТФЙПКцөзіШөзҪвұҘәНКіСОЛ®Ј¬ИфЙъіЙ0.2mol Cl2Ј¬ФтЦБЙЩРиНЁИлO2өДМе»эОӘ LЈЁұкЧјЧҙҝцЈ©
4ЎўСЎФсМв COCl2(g)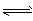 CO(g)+Cl2(g);ЎчH>0Бҝөұ·ҙУҰҙпөҪЖҪәвКұЈ¬ПВБРҙлК©ДЬМбёЯCOCl2ЧӘ»ҜВКөДКЗ
CO(g)+Cl2(g);ЎчH>0Бҝөұ·ҙУҰҙпөҪЖҪәвКұЈ¬ПВБРҙлК©ДЬМбёЯCOCl2ЧӘ»ҜВКөДКЗ
[? ]
ўЩЙэОВ ўЪәгИЭНЁИл¶иРФЖшМе ўЫФцјУCOөДЕЁ¶И ўЬјхС№ ўЭјУҙЯ»ҜјБ ўЮәгС№НЁИл¶иРФЖшМеЈ¬
AЈ®ўЩўЪўЬ
BЈ®ўЩўЬўЮ
CЈ®ўЪўЫўЮ
DЈ®ўЫўЭўЮ
5ЎўМоҝХМв ЈЁұҫРЎМвВъ·Ц9·ЦЈ©
ЈЁ1Ј©°С6 mol AЖшМеәН5 mol BЖшМе»мәП·ЕИл4 LГЬұХИЭЖчЦРЈ¬ФЪТ»¶ЁМхјюПВ·ўЙъ·ҙУҰЈә3A(g)+B(g) 2C(g)+xD(g)Ј¬ҫӯ5minҙпөҪЖҪәвЈ¬ҙЛКұЙъіЙ2 mol CЈ¬ІвөГDөДЖҪҫщ·ҙУҰЛЩВКОӘ0.15 mol/(LЎӨmin)Ј¬ФтЖҪәвКұAөДОпЦКөДБҝЕЁ¶ИКЗ____________Ј»BөДЧӘ»ҜВККЗ__________Ј»xөДЦөКЗ___________ЎЈ
2C(g)+xD(g)Ј¬ҫӯ5minҙпөҪЖҪәвЈ¬ҙЛКұЙъіЙ2 mol CЈ¬ІвөГDөДЖҪҫщ·ҙУҰЛЩВКОӘ0.15 mol/(LЎӨmin)Ј¬ФтЖҪәвКұAөДОпЦКөДБҝЕЁ¶ИКЗ____________Ј»BөДЧӘ»ҜВККЗ__________Ј»xөДЦөКЗ___________ЎЈ
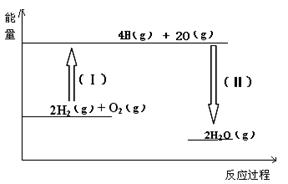
ЈЁ2Ј©·ҙУҰ2H2ЈЁgЈ© + O2ЈЁgЈ©ЈҪ 2H2OЈЁgЈ©өДДЬБҝұд»ҜИзНјЛщКҫЎЈТСЦӘІрҝӘ1molH2Ўў1molO2әН1molH-OЦРөД»ҜС§јь·ЦұрРиТӘПыәД436KJЎў496KJәН463KJДЬБҝЈ¬ФтёГ·ҙУҰ??ЈЁМоЎ°ОьКХЎұ »тЎ°·ЕіцЎұЈ©??KJИИБҝЎЈ
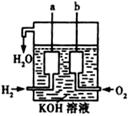
ЈЁ3Ј©ГА№ъ°ўІЁВЮУоЦж·Йҙ¬ЙПК№УГБЛТ»ЦЦРВРНЧ°ЦГЈ¬Жд№№ФмИзУТНјЛщКҫЈә
aЎўbБҪёцөзј«ҫщУЙ¶аҝЧөДМјҝйЧйіЙЎЈРҙіцaј«өДөзј«·ҙУҰКҪЈә?ЎЈ
ЈЁ4Ј©№ӨТөЙПУГөзҪвұҘәНКіСОЛ®өД·Ҫ·ЁЦЖИЎҪрКфВИЖшЈ¬·ҙУҰЦРДЬБҝөДЧӘ»ҜРОКҪКЗ?Ј»ВИЖшФЪ?ј«ЙПІъЙъЈ¬·ҙУҰәуИЬТәөДpH?ЎЈЈЁМоЎ°ФцҙуЎұ»тЎ°јхРЎЎұЈ©ЎЈ