1、选择题 下列图示与对应的叙述相符的是
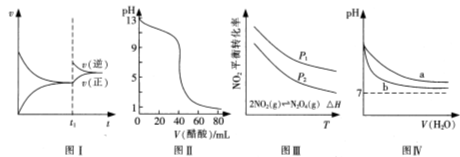
A.图I可表示N2+3H2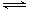 2NH3的速率时间图像,t1时刻改变的条件是升高温度
2NH3的速率时间图像,t1时刻改变的条件是升高温度
B.图Ⅱ可表示用0.1 000 mol/L醋酸滴定40.00 mL0.1000 mol/LNaOH溶液得到的滴定曲线
C.图Ⅲ可表示NO2平衡转化率与温度、压强的变化关系,由图可知:△H<0、P1<P2
D.图Ⅳ可表示pH相同的NaOH溶液与氨水稀释过程的pH变化.其中曲线a对应氨水
参考答案:D
本题解析:A、升高温度正逆反应速率均增大,错误;B、醋酸是弱电解质,0.1 000 mol/L醋酸的pH大于1,而且滴定时突变曲线比较平缓,错误;C、图像中有多个变量时要注意定一议一,随温度升高,NO2平衡转化率降低,平衡逆向移动,正向为放热反应,△H<0;相同温度下,压强大平衡正向移动,NO2平衡转化率增大,故P2<P1,错误;D、氨水是弱电解质,加水稀释过程中不断电离产生OH-,使得氨水的pH高于加同样水的氢氧化钠溶液,但随水的量的增加,pH无限接近7,正确。
本题难度:一般
2、填空题 根据下图填空:
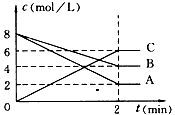
(1)反应物是_________;生成物是_________。
(2)在2 min内A,B,C三者的反应速率各是多少?________________________
(3)该反应的化学方程式是:_____________________
参考答案:(1)A和B;C
(2)v(A) =3 mol/(L・min)、v(B) = 2 mol/(L・min)、v(C) =3 mol/(L・min)
(3)
本题解析:
本题难度:一般
3、选择题 一定条件下,可逆反应N2 +3H2 2NH3?
2NH3?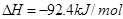 ,有关该反应的叙述正确的是(?)
,有关该反应的叙述正确的是(?)
A.正催化剂能加快正反应速率v正,不影响v逆,所以缩短了反应达平衡所需的时间
B.将lmol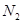 和3mol
和3mol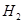 充分反应达到平衡时,放出的热量等于92.4kJ
充分反应达到平衡时,放出的热量等于92.4kJ
C.当c(N2):c(H2):c(NH3)=1:3:2时,反应就达到平衡状态
D.平衡时增大氮气的浓度,达新平衡时N2 转换率减小,H2转化率增大
参考答案:D
本题解析:A、催化剂降低活化能,以相同的倍数增大正逆反应速率;
B、可逆反应不可能进行到底,放出的热量小于92.4KJ;
C、平衡状态浓度之间没有关系,各物质浓度保持不变。
本题难度:一般
4、选择题 在t℃时,向一密闭容器(固定体积)中放入1mol A和1mol B,发生反应A(s) + B(g)  ?C(g) + 2D(g)达平衡时C的含量为m%,保持温度不变,若按下列配比的物质放入该容器中,达平衡时C的含量仍为m%的是(?)
?C(g) + 2D(g)达平衡时C的含量为m%,保持温度不变,若按下列配比的物质放入该容器中,达平衡时C的含量仍为m%的是(?)
A.2molA和1molB
B.2molD,1molA和1molB
C.2molC和4molD
D.1molC和1molD
参考答案:A
本题解析:A、因为A为固体,它的量不影响气体浓度,正确;B、D为气体,增大了生成物的浓度并且增大了压强,平衡会移动,错误;C、压强增大,平衡左移,错误;D、因为1molB对应的是2molD,错误。
本题难度:一般
5、选择题 反应C(s)+H2O(g) CO(g)+H2(g)在一可变容积的密闭容器中进行,达到平衡,下列条件能使平衡移动的是(?)
CO(g)+H2(g)在一可变容积的密闭容器中进行,达到平衡,下列条件能使平衡移动的是(?)
A.增加C的量
B.加催化剂
C.保持体积不变,充入氮气使体系压强增大
D.保持压强不变,充入氮气使容器体积增大
参考答案:D
本题解析:A、因浓度越大,化学反应速率越快,但是固体量的增减不影响反应速率,所以增加C(s)的量,反应速率不变,化学平衡不移动,故错;
B、催化剂能改变化学反应速率,不能使化学平衡移动,故错;
C、保持体积不变,充入氮气,氮气不参与反应,反应体系中的各物质的浓度不变,则反应速率不变,化学平衡不移动,故错;
D、保持压强不变,充入氮气,使容器的体积变大,反应体系中各物质的浓度减小,则反应速率减小,化学平衡发生移动,故对。
故选D。
点评:影响化学平衡移动的因素有:温度、浓度、压强,需要注意的是改变纯固体或液体的量、使用催化剂,化学平衡不移动,压强改变必须引起浓度的改变才能引起化学化学平衡的移动。
本题难度:简单