1、选择题 某温度下在密闭容器中发生如下反应:2M(g)+ N(g)  2G(g)若开始时只充入2molG(g),达平衡时,混合气体的压强比起始时增加20%,若开始时只充入2molM和1molN的混合气体,达平衡时M的转化率为
2G(g)若开始时只充入2molG(g),达平衡时,混合气体的压强比起始时增加20%,若开始时只充入2molM和1molN的混合气体,达平衡时M的转化率为
A.20%
B.40%
C.60%
D.80%
2、填空题 (13分)
Ⅰ?某温度下,密闭容器中充入1 mol N2和3 mol H2,使之反应合成NH3,平衡后,测得NH3的体积分数为w,如果温度不变,只改变起始加入量,使之反应平衡后NH3的体积分数仍为w,N2、H2、NH3的物质的量分别用x、y、z表示.
(1)恒温恒容条件下:若x=0.75 mol, 则y=________,z=________.
(2)恒温恒压条件下,x、y、z(均不小于0)满足的一般条件是_______________________.
Ⅱ?一定条件下,可逆反应X(g)+Y(g) 2Z(g)达到平衡时,各物质的平衡浓度为c(X)=0.5mol/L;c(Y) ="0.1" mol /L ; c (Z)="1.6" mol /L若用a、b、c 分别表示X Y Z的初始浓度(mol/L)则a、b应满足的关系是________?____, a的取值范围为_______________
2Z(g)达到平衡时,各物质的平衡浓度为c(X)=0.5mol/L;c(Y) ="0.1" mol /L ; c (Z)="1.6" mol /L若用a、b、c 分别表示X Y Z的初始浓度(mol/L)则a、b应满足的关系是________?____, a的取值范围为_______________
Ⅲ?在10℃和4×105Pa的条件下,当反应aA(g) dD(g)+eE(g),建立平衡后,维持温度不变而压强改变,测得D的浓度变化如下:
dD(g)+eE(g),建立平衡后,维持温度不变而压强改变,测得D的浓度变化如下:
压强(Pa)
| 4×105
| 6×105
| 10×105
| 20×105
|
D的浓度(mol/L)
| 0.085
| 0.126
| 0.200
| 0.440
|
(1)压强从4×105Pa增加到6×105Pa时,平衡向?(填“正”或“逆”)方向移动,理由是_________________________________________________________________
(2)压强从10×105Pa增加到20×105Pa时,平衡向_______(填“正”或“逆”)方向移动
3、选择题 2 mol A与2 mol B混合于2 L的密闭容器中,发生如下反应:2A(g)+3B(g) 2C(g)+zD(g),若2 s后,A的转化率为50%,测得v(D)=0.25 mol・L-1・s-1,下列推断正确的是( )
2C(g)+zD(g),若2 s后,A的转化率为50%,测得v(D)=0.25 mol・L-1・s-1,下列推断正确的是( )
A.v(C)=0.2 mol・L-1・s-1? B.z=3 ?C.B的转化率为25%? D.C的体积分数为28.6%
4、填空题 已知化学反应①:Fe(s)+CO2(g)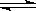 ?FeO(s)+CO(g),其平衡常数为K1;化学反应②:Fe(s)+H2O(g)
?FeO(s)+CO(g),其平衡常数为K1;化学反应②:Fe(s)+H2O(g)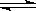 FeO(s)+H2(g),其平衡常数为K2,在温度973 K和1173 K情况下,K1、K2的值分别如下:
FeO(s)+H2(g),其平衡常数为K2,在温度973 K和1173 K情况下,K1、K2的值分别如下:
温度
| K1
| K2
|
973 K
| 1.47
| 2.38
|
1173 K
| 2.15
| 1.67
|
?
请填空:
(1)通过表格中的数值可以推断:反应①是________(填“吸热”或“放热”)反应.
(2)现有反应③:CO2(g)+H2(g)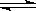 CO(g)+H2O(g),请你写出该反应的平衡常数K3的数学表达式:K3=?.
CO(g)+H2O(g),请你写出该反应的平衡常数K3的数学表达式:K3=?.
(3)在相同温度下,根据反应①与②可推导出K1、K2与K3之间的关系式________,据此关系式及上表数据,也能推断出反应③是________(填“吸热”或“放热”)反应.
(4)要使反应③在一定条件下建立的平衡向正反应方向移动,可采取的措施有________(填写字母序号,下同).
A.增大压强? B.体积不变时充入稀有气体? C.升高温度
D.使用合适的催化剂? E.在体系中投入少量P2O5固体
(5)图甲、乙分别表示反应③在t1时刻达到平衡,在t2时刻因改变某个条件而发生变化的情况:①图甲中t2时刻发生改变的条件可能是________________.
②图乙中t2时刻发生改变的条件可能是?.
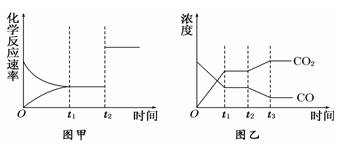
A.升高温度? B.降低温度? C.加入催化剂? D.增大压强?
E.减小压强? F.充入CO2? G.分离出部分CO
5、选择题 在2A + B = 3C + 4D的反应中,下列表示该反应速率最大的是
[? ]
A.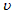 (A)=0.5 mol・L-1・min-1
(A)=0.5 mol・L-1・min-1
B.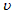 (B)=0.3 mol・L-1・min-1
(B)=0.3 mol・L-1・min-1
C.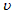 (A)=0.8 mol・L-1・min-1
(A)=0.8 mol・L-1・min-1
D.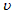 (D)=1 mol・L-1・min-1
(D)=1 mol・L-1・min-1