1、选择题 铁是一种应用广泛的金属。下列有关铁的说法正确的是
A.铁与盐酸反应生成氯化铁和氢气
B.常温下铁在浓硫酸中钝化
C.铁在氧气中燃烧生成物为三氧化二铁
D.纯铁(块状)是黑色金属
参考答案:B
本题解析:.铁与盐酸反应生成氯化亚铁和氢气,A不正确;B正确,C不正确,铁在氧气中燃烧生成四氧化三铁。纯铁是银白色金属,D不正确,答案选B。
点评:该题是识记性知识的考查,难度不大。平时注意知识的积累和总结,并能灵活运用即可,有利于巩固基础,通过学生的应试能力。
本题难度:一般
2、实验题 (16分)钢铁工业是国家工业的基础,是日常生活中用途最广、用量最大的金属材料。
(1)常温下,可用铁质容器盛装浓硫酸的原因是?。
(2)在一定条件下用普通铁粉和水蒸气反应,可以得到铁的氧化物。该氧化物又可以经过此反应的逆反应,生成颗粒很细的铁粉。这种铁粉具有很高的反应活性,俗称“引火铁”。请分别用下图中示意的两套仪器装置,制取上述铁的氧化物和“引火铁”。实验中必须使用普通铁粉和6mol/L盐酸,其他试剂自选(装置中必要的铁架台、铁夹、铁圈、石棉网、加热设备等在图中均已略去)。
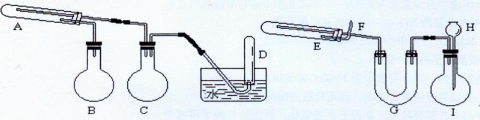
填写下列空白:
①实验进行时试管A中应加入的试剂是?;烧瓶B的作用是?;烧瓶C的作用是?。
②实验时,U型管G中加入的试剂是?;长颈漏斗H中应加入?。
③试管E中发生反应的化学方程式是?。
④为了安全,在E管中的反应发生前,在F出口处必须?。
参考答案:

本题解析:
(1)常温下,铁在浓硫酸中发生钝化现象使铁表面形成一层致密稳定的氧化膜,故铁制品容器可以盛放浓硫酸,故答案为:浓硫酸使铁表面形成一层致密稳定的氧化膜;
⑵①根据题干中所提供的物质可以推断出第一步实验中除了生成四氧化三铁外还会生成氢气,发生的反应为铁在高温和水蒸气反应生成四氧化三铁和氢气,反应的化学方程式为:3Fe+4H2O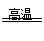 4H2+Fe3O4;试管A是铁与水蒸气反应的装置,故在A中装的应该是普通铁粉,在反应过程中 要生成氢气,所以D是用来收集氢气的,烧瓶的作用就是加热液体或者对液体进行蒸馏,所以这里蒸馏瓶所起的作用就是产生水蒸气,为了防止向试管中通入水蒸气使试管骤冷,引起水的倒流从而在试管和收集气体的试管中间加上了广口瓶,保证实验安全;A中是铁和水蒸气的反应;B中为产生水蒸气的装置,C为安全瓶防止倒吸的作用,D中收集的是氢气,
4H2+Fe3O4;试管A是铁与水蒸气反应的装置,故在A中装的应该是普通铁粉,在反应过程中 要生成氢气,所以D是用来收集氢气的,烧瓶的作用就是加热液体或者对液体进行蒸馏,所以这里蒸馏瓶所起的作用就是产生水蒸气,为了防止向试管中通入水蒸气使试管骤冷,引起水的倒流从而在试管和收集气体的试管中间加上了广口瓶,保证实验安全;A中是铁和水蒸气的反应;B中为产生水蒸气的装置,C为安全瓶防止倒吸的作用,D中收集的是氢气,
故答案为:普通铁粉(或铁粉);产生水蒸气;防止水倒吸(或用作安全瓶);氢气;
②装置I是用来制取氢气的装置,所以装置H是用来添加盐酸的,F中发生反应:Fe3O4+4H2 3Fe+4H2O;由于使用的是稀盐酸来制取氢气,所以在产生氢气的同时可能带出部分水蒸气和氯化氢气体,故在U型管中加入固体来干燥气体,吸收氯化氢和水蒸气,所以U型管中为固体NaOH(或碱石灰、CaO等碱性固体干燥剂),
3Fe+4H2O;由于使用的是稀盐酸来制取氢气,所以在产生氢气的同时可能带出部分水蒸气和氯化氢气体,故在U型管中加入固体来干燥气体,吸收氯化氢和水蒸气,所以U型管中为固体NaOH(或碱石灰、CaO等碱性固体干燥剂),
故答案为:固体NaOH(或碱石灰、CaO等碱性固体干燥剂);6摩/升的稀盐酸;
③依据装置和实验目的分析,试管E中发生反应是氢气还原四氧化三铁的反应,反应的化学方程式是:Fe3O4+4H2 3Fe+4H2O,故答案为:Fe3O4+4H2
3Fe+4H2O,故答案为:Fe3O4+4H2 3Fe+4H2O;
3Fe+4H2O;
④氢气是可燃性气体,做氢气的性质实验时必须保证氢气是纯净的,为了安全,在E管中的反应发生前,在F出口处必须进行气体验证纯度;E管中的反应开始后,在F出口处应点燃氢气,避免排放到空气中遇火爆炸;故答案为:检验氢气的纯度;点燃氢气.
本题难度:一般
3、填空题 氟化铜是一种锂/氟化铜电池正极活性材料,可通过下列方法制备:在铂皿中将氧化铜用过量的40%氢氟酸溶解,先制成CuF2・5HF・5H2O,再将生成物放入镍管内的铂舟中,在干燥的氟化氢气流中以400%进行加热脱水,最后通入氮气。
(1)制备过程中用铂皿而不用玻璃器皿的原因是______________________________________(用化学方程式表示)。
(2) 锂/氟化铜电池放电时总反应为置换反应,其化学方程式为____________________________________________________。
(3)准备称取上述制备的样品(仅含CuF2和CuO) 2.120 g,在通风橱中加入稀硫酸至完全溶解,然后加入足量的氢氧化钠溶液,得沉淀,将沉淀充分灼烧,得1.680 g黑色固体,计算样品中CuF2和CuO的物质的量之比。
参考答案:(1)SiO2+4HF=SiF4↑+2H2O
(2)CuF2+2Li=Cu+2LiF
(3)20:1
本题解析:(1)氢氟酸会腐蚀玻璃,生成SiF4。(2)题给信息中已经标明了反应物是锂和氟化铜,且注明了反应类型。(3)由题意知:CuF2、CuO→CuSO4→Cu(OH)2→CuO,故可用差量法求出CuF2。
CuF2 ~ CuO Δm
102 g ?80 g?22 g
m(CuF2) 2.120 g-1.680 g=0.440 g
m(CuF2)=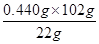 =2.040 g
=2.040 g
n(CuF2)=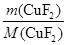 =
=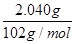 =0.020 mol
=0.020 mol
m(CuO)=2.120 g-2.040 g=0.080 g
n(CuO)=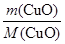 =
=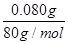 =0.001 mol,
=0.001 mol,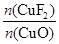 =
= =20∶1
=20∶1
本题难度:一般
4、选择题 下列叙述中正确的是( )
A.向含有CaCO3沉淀的水中通入CO2至沉淀恰好溶解,再向溶液中加入NaHCO3饱和溶液,又有CaCO3沉淀生成
B.向Na2CO3溶液中逐滴加入等物质的量的稀盐酸,生成的CO2与原Na2CO3的物质的量之比为1∶2
C.等质量的NaHCO3和Na2CO3分别与足量盐酸反应,在同温同压下,生成的CO2体积相同
D.向Na2CO3饱和溶液中通入CO2,有NaHCO3结晶析出
参考答案:D
本题解析:向含有CaCO3沉淀的水中通入CO2,至沉淀恰好溶解,溶液为Ca(HCO3)2,与加入的NaHCO3饱和溶液不反应,不能生成CaCO3沉淀,A错;向Na2CO3溶液中逐滴加入等物质的量的稀盐酸,生成了NaHCO3,不会放出CO2,B错;等质量的NaHCO3和Na2CO3,n(NaHCO3)>n(Na2CO3),分别与足量盐酸反应,在同温同压下NaHCO3生成的CO2体积大,C错;同温度下,NaHCO3的溶解度小于Na2CO3的溶解度,所以将CO2通入饱和Na2CO3溶液时,NaHCO3会结晶析出。
本题难度:一般
5、实验题 某小组同学设计实验探究Fe3+与Fe2+相互转化,实验方案及现象如下:
Ⅰ. 配制FeCl2溶液
取部分变质的氯化亚铁固体[含有难溶性杂质Fe(OH)2Cl],向其中加入稀盐酸,使其完全溶解,再加入适量铁粉。
Ⅱ. 实验探究Fe3+与Fe2+相互转化
实验1:
0.1 mol/L FeCl2溶液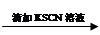 无明显现象
无明显现象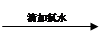 溶液变红
溶液变红
实验2:
0.1 mol/L FeCl3溶液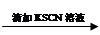 溶液变红
溶液变红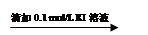 溶液红色未褪去
溶液红色未褪去
写出Fe(OH)2Cl与盐酸反应的离子方程式?。
(2)请用离子方程式解释实验1中滴加氯水后溶液变红的原因?。
(3)实验2的现象与预测不同, 为探究可能的原因,该小组同学又进行了如下实验,方案及现象如下:
步骤1:10 mL 0.1 mol/L KI溶液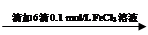 溶液明显变黄
溶液明显变黄
步骤2:将黄色溶液分为三份:
试管1 取2 mL黄色溶液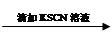 溶液变红
溶液变红
试管2 取3 mL黄色溶液 溶液变蓝
溶液变蓝
试管3 取3 mL黄色溶液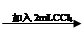 取上层溶液
取上层溶液 溶液变蓝(比试管2中溶液颜色深)
溶液变蓝(比试管2中溶液颜色深)
① 试管2中滴加K3[Fe(CN)6]检验的离子是?。
② 黄色溶液中含有的溶质微粒有K+、Cl-和?。
③ 综合上述实验现象,得出的实验结论是?。
参考答案:
(1)Fe(OH)2Cl + 2H+ = Fe3+ + Cl- + 2H2O(1分)
(2)2Fe2+ + Cl2 = 2Cl- + 2Fe3+(1分)
(3)①Fe2+(1分)?②Fe3+、Fe2+、I2?(2分)?③Fe3+与I-的反应为可逆反应(2分)
本题解析:
(1)根据题意可得:Fe(OH)2Cl + 2H+ = Fe3+ + Cl- + 2H2O
(2)Cl2 与Fe2+发生氧化还原反应:2Fe2+ + Cl2 = 2Cl- + 2Fe3+(1分)
(3)①K3[Fe(CN)6]专门用于检验的Fe2+试剂;?②滴加KSCN溶液溶液变红有Fe3+、加2滴K3[Fe(CN)6]溶液溶液变蓝有Fe2+、滴加6滴0.1 mol/L FeCl3溶液溶液明显变黄有I2?;③反应物、生成物都存在,试管3中实验说明平衡移动,则Fe3+与I-的反应必为可逆反应。
本题难度:一般