1������� ��֪A��B��CΪ��ѧ��ѧ�г����ĵ��ʣ� AΪ�����������������������;���Ľ������ʣ�������B�ǻ���ɫ���壬CΪ��ɫ���塣��һ���������ת���Ĺ�ϵ��ͼ��ʾ��
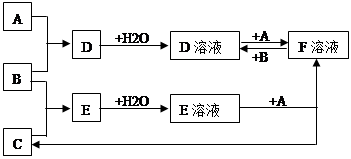
��ش��������⣺
��1��A��B��C�ֱ���ʲô���ʣ�A��?��B��?��C��?��F��?���ѧʽ��
��2��д��A��B����D�Ļ�ѧ����ʽ��?����D��Һ�м�
��?��Һ�ɿ�����Һ��Ѫ��ɫ��
��3��д��F��Һ�м���B�����ӷ���ʽ��??
�ο��𰸣�����10�֣���1��Fe? Cl2? H2?FeCl2?����1�֣�
��2��2Fe?+?3Cl2?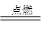 ?2FeCl3?��2�֣�?KSCN��������أ�2�֣�
?2FeCl3?��2�֣�?KSCN��������أ�2�֣�
��3��Cl2 +2Fe2+�� 2Cl�� + 2Fe3+��2�֣�
���������AΪ�����������������������;���Ľ������ʣ���A������������B�ǻ���ɫ���壬��B������������������Ӧ�����Ȼ�������D���Ȼ������Ȼ���������Ӧ�����Ȼ�����������F���Ȼ��������Ȼ�������������Ӧ�������Ȼ�����E������Ӧ�����Ȼ�������C������ΪC��һ����ɫ���壬����C��������E���Ȼ��⡣
�������������е��Ѷȵ����⣬���������ǿ����������������������ѧ����Ҫ��ȷ���ǻ�ѧ�ƶ�����һ���ۺ��Խ�ǿ�����⣬��Ԫ�ؼ����������ʺ�������������������ѧ�����֪ʶ����������ѧ�Ƽ��ۺϡ��������ɿ���ѧ���Ի�ѧ֪ʶ������̶ȣ�����Ҫ��������ѧ�����ۺϷ���������˼ά���������ͼ��ķ�������ؼ�����Ѱ�ҡ�ͻ�ƿڡ�����ͻ�ƿڡ�����ץ���ء��֣�����������ɫ������״̬��������ζ�����ⷴӦ���������������Ʒ���������;�ȡ�
�����Ѷȣ�һ��
2��ѡ���� �������ʵ����ƺͻ�ѧʽ���������
A��������Fe2O3��
B��������FeS2��
C�����죨Fe2O3��
D��������FeO��
�ο��𰸣�D
�����������
�����Ѷȣ���
3������� ����ڵ��µ���ͭ����ʴ���̿��Ա�ʾΪ��
��1����ͭ����ʴ�����еIJ�����__________________________________________________��
��2����ͭ���������ֹ��ͭ��������ʴ�Ĺؼ���____________________________________��
�ο��𰸣���1��CuCl��Cu2O��Cu2(OH)2CO3��Cu4(OH)6Cl2��
��2����H2O��O2�ȸ���
�����������ͭ����ʴ�����еIJ����ͼ�п��������������ͼ�п�����ʴ��Ӧ�������Ǵ���O2��ˮ������������CO2��HCl�ȣ�����O2�ǹؼ���
�����Ѷȣ�һ��
4������� ��FeCl3��Һʴ��ͭ�������·��Ĺ����У���Һ��������Դ���յĹ��̼������£���ش��������⣺
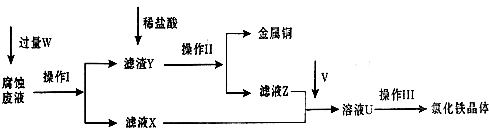
��1����д��FeCl3��Һ��ͭ��Ӧ�����ӷ���ʽ��______�������������Լ�W��______��
��2��������֮ǰ��ü�������ϡ���ᣬijͬѧ��10mol-L-1?��Ũ��������250mL?1mol-L-1?��ϡ���ᣬ�������й�ʵ�飮
����Ҫ��ȡŨ����______mL��
�����Ƹ�ϡ����ʱ����Ͳ���ձ����������⣬�������õ���������______��______��
������֪Ũ�ȵ�����������Һ�ζ�ϡ���ᣬ�ζ��������۾�Ӧע��______��ʵ��ʱδ�ñ�Һ��ϴ�ζ��ܣ������ƿ�д���Һ��Ũ��______ʵ��Ũ�ȣ������������������=������
��3��������ǰ��Ҫͨ������V����д��ʵ������ȡ����V�Ļ�ѧ����ʽ��______���÷�Ӧ��______����������
��4��������Ӧ��HCl������Χ�н��У���ԭ����______��
��5����ͨ���V�������㣬������Ƶõ��Ȼ������岻������������Ϊ��ҺU�к�������______������ƺ�����ʵ�飬��֤��ҺU�еijɷ֣����ж�ͨ���V�����Ƿ���______����Ҫ˵��ʵ�鲽�衢����ͽ��ۣ���
��ѡ����Լ�������KMnO4��Һ��KSCN��Һ����ˮ��
��6�������Ȼ�����Һ�м���һ����ʯ��ˮ��������ҺpH���ɵú��ɫ�������ù����е�����Һ��pHΪ5�����������Ũ��Ϊ______������֪��Ksp[Fe��OH��3]=4.0��10-38��
�ο��𰸣���1��FeCl3��Һ��ͭ��Ӧ�����ӷ���ʽΪ��2Fe3++Cu�T2Fe2++Cu2+�����������Խ�����ͭ���������û����������Լӵ�W�����ۻ�Fe���ʴ�Ϊ��2Fe3++Cu�T2Fe2++Cu2+�����ۻ�Fe��
��2������10mol?L-1?��Ũ��������250mL?1mol?L-1?��ϡ���ᣬϡ��ǰ�����ʵ����ʵ������䣬������Ũ����������V����V?10mol?L-1=250mL?1mol?L-1�����V=25mL���ʴ�Ϊ��25mL��
������һ�����ʵ���Ũ�ȵ���Һ����IJ��������У���Ͳ���ձ�����������250mL����ƿ����ͷ�ιܣ��ʴ�Ϊ��250mL����ƿ����ͷ�ιܣ�
������֪Ũ�ȵ�����������Һ�ζ�ϡ���ᣬ�ζ��������۾�Ӧע����ƿ����Һ��ɫ�ı仯��δ�ñ�Һ��ϴ�ζ��ܣ��൱�ڽ���Һϡ�ͣ������Һ��������࣬���Բ����ƿ�д���Һ��Ũ�ȴ���ʵ��Ũ�ȣ��ʴ�Ϊ����ƿ����Һ��ɫ�ı仯�����ڣ�
��3��ʵ�����������Ļ�ѧ����ʽΪ��MnO2+4HCl��Ũ��?��?.?MnCl2+Cl2��+2H2O��izhongMn�Ļ��ϼ۽��ͣ����Զ������������������ʴ�Ϊ��MnO2+4HCl��Ũ��?��?.?MnCl2+Cl2��+2H2O��MnO2��
��4��������������ˮ�⣬�Ȼ�����Һ���ɵò����Ȼ������壬������Ҫ������������������ˮ�⣬�ʴ�Ϊ������Fe3+����FeCl3����ˮ�⣻
��5����ͨ��������������㣬�������Ӳ�����ȫ������Ϊ���������ӣ���������Ƶõ��Ȼ������岻�������Ậ���Ȼ��������������Ӿ��л�ԭ�ԣ������Ǹ��������ɫ��������������ʹ������ر�Ϊ��ɫ�����Ծݴ������飬
�ʴ�Ϊ��FeCl2��Fe2+����ȡ������ҺU�����뼸��KSCN��Һ����Һ�Ժ�ɫ���������ҺU����Fe3+��FeCl3������ȡ������ҺU�����뼸������KMnO4��Һ����KMnO4��Һ��ɫ���������ҺU����Fe2+����FeCl2����˵��ͨ��������������㹻����KMnO4��Һ����ɫ����˵��ͨ��������������㣻
��6����������������Ksp����ʽ��Ksp=[Fe3+][[OH-]3]����Һ��pHΪ5��[H+]=10-5mol/L�����Խ���������Ũ��Ϊ4.0��10-11?mol?L-1���ʴ�Ϊ��4.0��10-11mol?L-1��
���������
�����Ѷȣ�һ��
5��ѡ���� ����1mol HNO3��ϡ����ֱ��벻ͬ���������۷�Ӧ��������������a��b���������ʵ�����ϵ��ͼ��ʾ�������й��ж���ȷ����?��?��
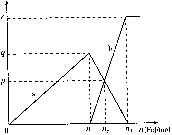
A��a��Fe��NO3��2
B��n1=0��375
C��P=0��125
D��n2=0��30
�ο��𰸣�D
�����������
�����Ѷȣ�һ��