| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学必备知识点《水的电离平衡》在线测试(2017年最新版)(四)
参考答案:B 本题解析:pH=3的盐酸和c(OH-)=10-3mol・L-1的Ba(OH)2溶液等体积混合,溶液呈中性,故a=d;pH=3的盐酸和c(NH3・H2O)=10-3mol・L-1的氨水等体积混合时恰好完全反应,溶液呈酸性,要使溶液呈中性,氨水的体积要大于盐酸,故b>a;pH=3的盐酸和c(OH-)=10-3mol・L-1的氨水等体积混合时氨水有剩余,PH>7,要使溶液呈中性,氨水的体积要小于盐酸,故a>c;所以b>a=d>c, B项正确。 本题难度:一般 4、选择题 常温时,向pH=12的Ba(OH)2溶液中加入等体积的下列溶液后,滴入酚酞试液出现红色,该溶液应该是 |
参考答案:D
本题解析:
常温下,酚酞试液的变色范围:8-10,滴入酚酞试液出现红色,说明混合液显碱性。
A、向pH=12的Ba(OH)2溶液中加入等体积的pH=2的硫酸溶液,二者的氢离子和氢氧根恰好完全反应,呈中性,故A不合题意;
B、向pH=12的Ba(OH)2溶液中加入等体积的pH=2的醋酸溶液,醋酸过量,混合液显酸性,故B不合题意;
C、向pH=12的Ba(OH)2溶液中加入等体积的0.05mol/L盐酸溶液,盐酸过量,混合液显酸性,故C不合题意;
D、向pH=12的Ba(OH)2溶液中加入等体积的0.05mol/LNa2SO4溶液,反应生成硫酸钡沉淀和氢氧化钠,混合液显碱性,故D符合题意。
考点:考查酸碱中和反应、指示剂的变色范围
点评:本题考查了酸碱中和反应、指示剂的变色范围,难度不大。易错点是涉及到弱酸的PH与酸的浓度的关系,如B项,误以为是酸碱恰好完全反应。
本题难度:一般
5、选择题 用已知浓度的盐酸滴定未知浓度的氢氧化钠溶液,以甲基橙为指示剂,下列有关说法正确的是
A.用碱式滴定管向锥形瓶内注入10mL氢氧化钠溶液,若开始时滴定管尖嘴有气泡,则测定结果偏高
B.边滴边振荡,直到溶液由橙色变成黄色且半分钟内不褪色为止
C.接近滴定终点时,往锥形瓶加入少量蒸馏水,则测定结果偏高
D.用酸式滴定管时,起始读数俯视,结束读数仰视,则测定结果偏高
参考答案:A
本题解析:A、用碱式滴定管向锥形瓶内注入10mL氢氧化钠溶液,若开始时滴定管尖嘴有气泡,则所取溶液的量偏少,滴定所消耗的盐酸会偏少,根据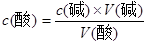 ,可知c(酸)偏高,A正确;B、未知浓度是氢氧化钠,加入甲基橙为黄色,滴定终点是由黄色变为橙红色或浅红色,B错误;C、接近滴定终点时,往锥形瓶加入少量蒸馏水,测定结果不变,C错误;D、用酸式滴定管时,起始读数俯视,结束读数仰视,造成V(酸)偏大,根据
,可知c(酸)偏高,A正确;B、未知浓度是氢氧化钠,加入甲基橙为黄色,滴定终点是由黄色变为橙红色或浅红色,B错误;C、接近滴定终点时,往锥形瓶加入少量蒸馏水,测定结果不变,C错误;D、用酸式滴定管时,起始读数俯视,结束读数仰视,造成V(酸)偏大,根据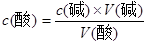 ,则测定结果c(酸)偏低,答案选A。
,则测定结果c(酸)偏低,答案选A。
考点:考查酸碱中和滴定。
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学试题《键参数――键能、.. | |