1、选择题 物质的量浓度相同的200mL Ba(OH)2溶液和150mL NaHCO3混合后,最终溶液中离子的物质的量浓度关系正确的是
A.c(OH-)>c(Ba2+)>c(Na+)>c(CO32-)
B.c(OH-)>c(Na+)>c(Ba2+)>C(H+)
C.c(OH-)=c(Ba2+)+c(Na+)+c(H+)
D.c(H+)+c(Na+)+2c(Ba2+)=c(OH-)
参考答案:B
本题解析:为了便于计算,设 Ba(OH)2和 NaHCO3的物质的量分别为4mol和3mol,则
n(OH-)="8mol?" n(Ba2+)="4mol?" n(Na+)="3mol?" n(HCO3-)="3mol?" ;反应后:
n(OH-)="5mol?" n(Ba2+)="1mol?" n(Na+)="3mol?" ,所以选B
本题难度:一般
2、选择题 分别将下列物质:①CuSO4?②Na2O2?③NaCl?④FeCl3?投入水中,对其溶液加热蒸干,仍能得到原物质的是
A.①②③
B.①③
C.③④
D.③
参考答案:B
本题解析:该题出的不够科学,该为分别投入水中
过氧化钠与水反应生成NaOH,FeCl3加热水解生成Fe(OH)3和HCl,且HCl挥发,最终得到Fe(OH)3;故答案为B。
本题难度:一般
3、选择题 在48ml0.1mol/LHNO3溶液中加入12ml0.4mol/LKOH溶液后,所得到的溶液呈
A.弱酸性
B.强酸性
C.碱性
D.中性
参考答案:D
本题解析:略
本题难度:一般
4、选择题 下列说法中,不正确的是(?)
A.在NaAlO2溶液中,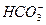 不可能大量存在
不可能大量存在
B.在0.1 mol・L-1的氢溴酸中加入适量的蒸馏水,溶液的c(H+)减小
C.在由水电离出的c(OH-)=1×10-12 mol・L-1的溶液中,Al3+不可能大量存在
D.室温下pH=6的酸性溶液中,可能存在NH3・H2O分子
参考答案:C
本题解析:A项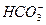 酸性强于氢氧化铝的酸性,向NaAlO2溶液中加入
酸性强于氢氧化铝的酸性,向NaAlO2溶液中加入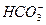 可发生
可发生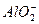 +
+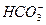 +H2O====Al(OH)3↓+
+H2O====Al(OH)3↓+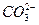 。C项由水电离出的c(OH-)=1×10-12 mol・L-1的溶液可能是酸性溶液,也可能是碱性溶液,若为酸性Al3+可能大量存在。D项室温下pH=6的NH4Cl溶液中存在NH3・H2O分子。
。C项由水电离出的c(OH-)=1×10-12 mol・L-1的溶液可能是酸性溶液,也可能是碱性溶液,若为酸性Al3+可能大量存在。D项室温下pH=6的NH4Cl溶液中存在NH3・H2O分子。
本题难度:简单
5、选择题 相同物质的量浓度的NaCN和NaClO相比,NaCN溶液的pH较大,则下列关于同温、同体积、同浓度的HCN和HClO溶液的说法中正确的是( )
A.酸的强弱:HCN>HClO
B.pH:HClO>HCN
C.与NaOH恰好完全反应时,消耗NaOH的物质的量:HClO>HCN
D.酸根离子浓度:c(CN-)<c(ClO-)
参考答案:D
本题解析:强碱弱酸盐的水溶液呈碱性,相应酸的酸性越弱,其强碱盐溶液的碱性越强。NaCN溶液的pH比NaClO大,说明HCN比HClO酸性弱。
本题难度:一般