1、实验题 实验室用固体烧碱配制500ml,0.1mol/LNaOH溶液
(1)需要称取__________g的烧碱固体,固体应放在__________中称量。
(2)配制的过程中不需要使用的仪器是__________(填标号字母)
A.?托盘天平?B.烧杯?C.玻璃棒? D.1000ml的容量瓶?E.碱式滴定管?F.胶头滴管
(3)根据实验的实际需要和(2)中所列出的仪器判断,完成该实验还缺少的玻璃仪器是______________。
(4)在容量瓶内确定溶液体积的过程中,完成后期加入少量的水(即定容)的操作方式是___________________。
(5)下列各项操作中,可能导致实际浓度偏高的是__________。(填选项字母) ?
A.称量NaOH固体时,砝码和物质的位置对调
B.向容量瓶中转移时,不慎洒出
C.NaOH溶解时放出大量的热,未及冷却立即配制溶液
D.定容时,仰视容量瓶的刻度线
E.定容时,加水超过刻度线,再用胶头滴管吸出多余的部分
F.称取氢氧化钠固体时所用的砝码生锈
(6)下图分别表示四种操作,其中有两处错误的是?_________
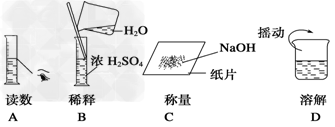
参考答案:(1)2.0g;烧杯(或玻璃器皿中)
(2)D、E
(3)500ml的容量瓶
(4)往容量瓶中加水至液面离容量瓶颈刻度下1-2cm时,改用胶头滴管滴加蒸馏水,滴加至液面与刻度线平视相切
(5)C
(6)BF
本题解析:
本题难度:一般
2、填空题 用20gNaOH配成500mL溶液,NaOH的物质的量的浓度为_______________。取出50mL,它的物质的量浓度为_______________,含NaOH的物质的量为_______________,含NaOH的质量为_______________g,把这50mL溶液加水稀释到200mL,NaOH的物质的量浓度为_______________。
参考答案:1mol/L;1mol/L;0.05mol;2;0.25mol/L
本题解析:
本题难度:一般
3、计算题 (4分)(1)密度为1.17g/cm3,浓度为36.5%的浓盐 酸中HCl的物质的量的浓度为 。
酸中HCl的物质的量的浓度为 。
(2)Na2O和Na2O2的混合物14g和足量的水反应,得到300mL溶液,其中含溶质16g。原混合物中Na2O和Na2O2的质量分别多少 。
参考答案:(1)11.7mol/L (2分,单位漏写扣1分)(2) Na2O 6.2g,Na2O2 7.8g。(各1分)
本题解析:略
本题难度:一般
4、选择题 某结晶水合物的化学式为A?nH2O,其相对分子质量为M,在25℃时,ag晶体溶于bg水中即达饱和,形成密度为ρg?mL-1的溶液,下列表达式正确的是( )
A.饱和溶液的物质的量浓度为:1000a(M-18n)/M(a+b)mol?L-1
B.饱和溶液中溶质的质量分数为:100a(M-18n)/M(a+b)%
C.饱和溶液的体积为:(a+b)/ρL
D.25℃时,A的溶解度为:100a(M-18n)/bMg
参考答案:晶体的物质的量为aMmol,溶质的质量为a(M-18n)Mg,溶液的质量为(a+b)g,溶液的体积为(a+b)gρg/ml=(a+b)ρml,
A、饱和溶液的物质的量浓度为:aM(a+b)ρ×10-3L=1000aρ(a+b)Mmol/L,故A错误;
B、饱和溶液中溶质的质量分数为:a(M-18n)Mg(a+b)g×100%=100a(M-18n)M(a+b)%,故B正确;
C、溶液的体积为:溶液的体积为(a+b)gρg/ml=(a+b)ρml,故C错误;
D、设25℃时,A的溶解度为S,则a(M-18n)Mg(a+b)s=s100+s,解之得s=100a(M-18n)bM+18an,故D错误.
故选B.
本题解析:
本题难度:一般
5、简答题 配制2mol/L/的NaOH溶液100mL,需要称取固体NaOH的质量是多少?简述操作步骤.
参考答案:配制2mol/L/的NaOH溶液100mL,氢氧化钠的物质的量为:0.1L×2mol?L-1=0.2mol,需氢氧化钠的质量为m=0.2mol×40g/mol=8.0g.
操作步骤有计算、称量、溶解、移液、洗涤移液、定容、摇匀等操作,一般用托盘天平称量,用药匙取用药品,在烧杯中溶解(可用量筒量取水加入烧杯),并用玻璃棒搅拌,加速溶解.冷却后转移到100mL容量瓶中,并用玻璃棒引流,洗涤烧杯、玻璃棒2-3次,并将洗涤液移入容量瓶中,加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,最后定容颠倒摇匀;
答:需要称取固体NaOH的质量是8.0g;操作步骤为:一般用托盘天平称量,用药匙取用药品,在烧杯中溶解(可用量筒量取水加入烧杯),并用玻璃棒搅拌,加速溶解.冷却后转移到100mL容量瓶中,并用玻璃棒引流,洗涤烧杯、玻璃棒2-3次,并将洗涤液移入容量瓶中,加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,最后定容颠倒摇匀.
本题解析:
本题难度:一般