|
高中化学必备知识点《物质的分离、提纯》试题特训(2017年最新版)(十)
2017-11-05 22:40:52
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
1、选择题 除去二氧化碳中混有的少量二氧化硫气体,可选的试剂是:
[? ]
A、酸性高锰酸钾溶液
B、NaOH溶液
C、饱和NaHCO3溶液
D、石灰水
参考答案:AD
本题解析:
本题难度:一般
2、填空题 Ⅰ.如图是中学化学中常用于混合物的分离与提纯的装置,请根据装置回答问题:
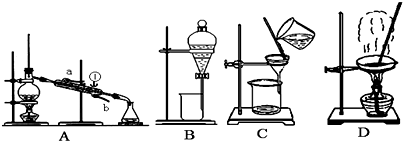
(1)从氯化钾溶液中得到氯化钾固体,选择装置______(填代表装置图的字母,下同);除去自来水中的Cl-等杂质,选择装置______.
(2)从碘水中分离出I2,选择装置______,该分离方法的名称为______.
(3)装置A中①的名称是______,进出水的方向是______.
(4)装置B在分液时为使液体顺利下滴,应进行的具体操作是______.(填代表选项的字母)
A.应该先将分液漏斗上的活塞拿下后再打开旋塞放出液体
B.加热
C.使分液漏斗上的活塞上的凹槽对准分液漏斗上的小孔后再打开旋塞放出液体.
Ⅱ.某同学按下列步骤配制250mL?0.2mol?L-1NaCl溶液,请回答有关问题.
实验步骤
有关问题
①计算所需NaCl的质量
②称量NaCl固体
用托盘天平需要称量NaCl的质量为______g.
③将NaCl加入100mL烧杯中,并加入适量水
为了加快溶解速率,可以采取哪些措施:______.
④将烧杯中溶液转移至250mL容量瓶中
为了防止溶液溅出,应采取什么措施:______.
⑤向容量瓶中加蒸馏水至刻度线
在进行此操作时当加水至刻度线1-2厘米处应如何操作:
______.
| (1)配制时,实验室提供了以下仪器:烧杯、100mL量筒、玻璃棒、托盘天平(带砝码)、胶头滴管,还缺少的玻璃仪器是______.上述实验中使用容量瓶前应______.
(2)取出该NaCl溶液10mL加水稀释到100mL,稀释后溶液中Na+的物质的量浓度是______.
(3)若进行⑤步操作时加蒸馏水超过刻度线,则需______.
(4)配制NaCl溶液时,下列操作情况会使结果偏高的是______.
A.移液前,容量瓶中有少量蒸馏水
B.溶解搅拌时有液体飞溅
C.定容时俯视容量瓶瓶颈刻度线
D.定容后,倒置容量瓶摇匀经平放静置,液面低于刻度线,再加水定容.
参考答案:Ⅰ.(1)蒸发可以实现易溶于水的固体和水的分离,从氯化钾溶液中得到氯化钾固体可用蒸发,因蒸馏可以实现水中难挥发性杂质和水的分离,则除去自来水中的Cl─等杂质,可用蒸馏,故答案为:D;A;
(2)碘微溶于水,碘易溶于苯、四氯化碳等有机溶剂,且苯、四氯化碳与水互不相溶,可用萃取法分离,故答案为:B;萃取;
(3)装置A中①的名称是冷凝管,使用时下口进水上口出水,故答案为:冷凝管;b进a出;
(4)在使用分液漏斗时,应该先将分液漏斗上的活塞拿下后再打开旋塞放出液体或打开分液漏斗上端活塞或使凹孔对准小孔,以保证内部液体顺利流下,
故答案为:AC或A或C;
Ⅱ.需氯化钠的质量为m=0.25L×0.2mol?L-1×58.5g/mol=2.925g≈2.9g;
为加快氯化钠溶解可以采取搅拌、加热、研细氯化钠等措施;
为防止溶液溅出通常采取用玻璃棒引流;
定容应注意:加水至液面距离刻度线1~2cm时,改用胶头滴管滴加至溶液凹液面与刻度线水平相切.
故答案为:2.9g;用玻璃棒搅拌;用玻璃棒引流;改用胶头滴管加水至刻度线;
(1)操作步骤有称量、溶解、移液、洗涤、定容、摇匀等操作,一般用托盘天平称量,用药匙取用药品,在烧杯中溶解,冷却后转移到250mL容量瓶中,并用玻璃棒引流,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,所以还需要的仪器为250mL容量瓶,容量瓶在使用前应检查是否漏水,故答案为:250mL?容量瓶;检查是否漏水;
(2)溶液稀释前后溶质的物质的量不变,则c(NaCl)=0.2mol/L×0.01L0.1L=0.02mol/L,故答案为:0.02mol/L;
(3)若进行⑤步操作时加蒸馏水超过刻度线,应重新配制,故答案为:重新配制;
(4)A.移液前,容量瓶中有少量蒸馏水,对实验没有影响,故A不选;
B.溶解搅拌时有液体飞溅,会导致溶质减少,浓度减小,故B不选;
C.定容时俯视容量瓶瓶颈刻度线,会导致溶液体积偏小,浓度偏大,故C选;
D.定容后,倒置容量瓶摇匀经平放静置,液面低于刻度线,再加水定容,会导致溶液浓度偏小,故D不选.
故答案为C.
本题解析:
本题难度:一般
3、选择题 有三组溶液:①汽油和氯化钠溶液 ②四氯化碳(沸点为76.75°C)和甲苯(沸点为110.6°C)溶液 ⑧氯化钠和单质溴的水溶液,分离以上各混合液的正确方法依次为? (? )
A.分液、萃取、蒸馏? B.萃取、蒸馏、分液
C.分液、蒸馏、萃取? D.蒸馏、萃取、分液
参考答案:C
本题解析:
正确答案:C
①汽油和氯化钠溶液互不相溶,通过分液来分离 ②四氯化碳(沸点为76.75°C)和甲苯(沸点为110.6°C)溶液,沸点相差高于30℃,可用蒸馏法分离 ⑧氯化钠和单质溴的水溶液,溴在CCl4中溶解度大,用萃取法分离。
本题难度:简单
4、实验题 用纯碱和双氧水混合可制作新型液体洗涤剂(2Na2CO3・3H2O2),它具有杀菌消毒去油污的能力且不会污染水源。
(1)检验这种新型洗涤剂中金属阳离子的操作和现象是_______________________________________。
(2)这种洗涤剂中的双氧水可以将废水中的氰化物转化为无毒物同时生成NH3,写出反应的离子方程式:___________________________________
(3)如果配制洗涤剂的水中含有铁离子,不仅会削弱洗涤剂的去污能力,甚至完全失去杀菌作用。试分析其中的原因(用离子方程式和简要文字表述):__________________________________________________________________
(4)某化学学习小组为定性探究铁离子对这种新型洗涤剂的不良影响,取该洗涤剂100 mL,加入25 gFeCl3固体,产生大量无色无味气体,用贮气瓶收集气体。请选用下列试剂和实验用品完成气体成分的探究过程:0.10 mol・L-1 NaOH溶液、8.0 mol・L-1 NaOH溶液、澄清石灰水、0.01 mol・L-1 KMnO4溶液、BaCl2稀溶液、品红溶液、蒸馏水、小木条、酒精灯、火柴、洗气瓶。
①提出假设:对该气体成分提出合理假设。
假设1:气体是O2;
假设2:气体是________________;
假设3:气体是CO2。
②设计方案:设计实验方案证明你的假设,在下表中完成实验步骤、预期现象与结论。
实验步骤
| 预期现象与结论
| 将气体依次通入盛有________、________的洗气瓶中,________
| __________________
|
?
参考答案:(1)用洁净的铂丝蘸取洗涤剂在酒精灯火焰上灼烧,火焰呈黄色(合理即可)
(2)H2O2+CN-+H2O=HCO3―+NH3
(3)2H2O2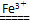 2H2O+O2↑,铁离子会加速H2O2分解,使洗涤剂失去杀菌作用;2Fe3++3CO32―+3H2O=2Fe(OH)3↓+3CO2↑,Fe3+与CO32―水解相互促进,使洗涤剂失去去污能力 2H2O+O2↑,铁离子会加速H2O2分解,使洗涤剂失去杀菌作用;2Fe3++3CO32―+3H2O=2Fe(OH)3↓+3CO2↑,Fe3+与CO32―水解相互促进,使洗涤剂失去去污能力
(4)①CO2和O2
②
实验步骤
预期现象与结论
澄清石灰水
8.0 mol・L-1 NaOH溶液 并将带火星的小木条放在最后一个洗气瓶的出口处
若澄清石灰水不变浑浊,木条复燃,则假设1成立;若澄清石灰水变浑浊,木条复燃,则假设2成立;若澄清石灰水变浑浊,木条不复燃,则假设3成立
本题解析:(1)这种新型液体洗涤剂的阳离子为Na+,可用焰色反应进行检验。(3)铁离子可以作为过氧化氢分解的催化剂,从而导致过氧化氢分解而失效;铁离子与碳酸根离子发生水解相互促进反应,使洗涤剂失去去污能力。(4)①该无色无味气体或是氧气、或是二氧化碳、或是两种气体的混合气体。②用澄清石灰水检验二氧化碳,用NaOH溶液吸收未反应完的二氧化碳,最后通过带火星的小木条检验氧气。
本题难度:一般
5、选择题 下列是物质中,可一次性鉴别乙酸、乙醇、苯及氢氧化钡溶液的是?(?)
A.金属钠
B.水
C.碳酸钠溶液
D.无色的酚酞试液
参考答案:C
本题解析:略
本题难度:简单
|