1、选择题 为了除去粗盐中的Ca2+,Mg2+,SO42-及泥沙,得到纯净的NaCl,可将粗盐溶于水,然后在下列操作中选取必要的步骤和正确的操作顺序( )
①过滤;?②加过量NaOH溶液;?③加适量盐酸;
④加过量Na2CO3溶液;?⑤加过量BaCl2溶液.
A.④②⑤①③
B.④①②⑤③
C.②⑤④①③
D.①④②⑤③
2、填空题 Ⅰ高纯MnCO3是制备高性能磁性材料的主要原料.
实验室以MnO2为原料制备少量高纯MnCO3的操作步骤如下:
(1)制备MnSO4溶液:
在烧瓶中(装置见右图)加入一定量MnO2和水,搅拌,通入SO2和N2混合气体,反应3h.停止通入SO2,继续反应片刻,过滤(已知MnO2+H2SO3=MnSO4+H2O).
①石灰乳作用______.
②若实验中将N2换成空气,测得反应液中Mn2+、SO42-的浓度随反应时间t变化如右图.导致溶液中Mn2+、SO42-浓度变化产生明显差异的原因是______.
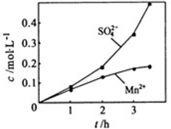
(2)制备高纯MnCO3固体:已知MnCO3难溶于水、乙醇,潮湿时易被空气氧化,100℃开始分解;Mn(OH)2开始沉淀时pH=7.7,请补充由(1)制得的MnSO4溶液制备高纯MnCO3的操作步骤[实验中可选用的试剂:Ca(OH)2、NaHCO3、Na2CO3、C2H5OH].
①______;②______;③检验SO42-是否被洗涤除去;④______;⑤低于100℃干燥.
Ⅱ锌铝合金的主要成分有Zn、Al、Cu、Si等元素.实验室测定其中Cu含量的步骤如下:
①称取该合金样品1.1g,用HCl和H2O2溶解后,煮沸除去过量H2O2,过滤,滤液定容于
250mL容量瓶中.
②用移液管移取50.00mL滤液于250mL碘量瓶中,控制溶液的pH=3~4,加入过量KI溶液(生成CuI和I2)和指示剂,
用0.01100mol?L-1Na2S2O3溶液滴定生成的I2至终点(反应:I2+2S2O32-=2I-+S4O62-),消耗Na2S2O3溶液6.45mL.
(1)判断步骤②滴定终点的方法是______.
(2)计算合金中Cu的质量分数______.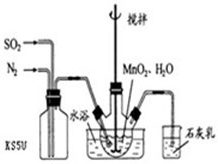
3、实验题 草酸晶体的组成可表示为H2C2O4・xH2O,为测定x值,进行下述实验:
①称取Wg草酸晶体配成100mL水溶液;
②取25. 00mL所配的草酸溶液置于锥形瓶中,加适量稀H2SO4,用浓度为 amol・L-1的KMnO4溶液滴定,所发生的反应为2KMnO4+ 5H2C2O4+3H2SO4=K2SO4+10CO2↑+2MnSO4+8H2O。
试回答:
(1)实验中不需要的仪器是_________(填序号)。还需要补充的仪器是___________(填名称)。
①碱式滴定管②酸式滴定管③天平(带砝码)④100 mL量筒⑤100 mL容量瓶⑥烧杯⑦锥形瓶⑧药匙⑨漏斗
(2)滴定过程中若用去KMnO4溶液VmL,则所配草酸溶液的浓度为_________mol・L-1,由此可计算出x的值为____________。
(3)若滴定终点时,俯视读数,则x值可能会____(填 “偏高”“偏低”或“无影响”)。
(4)为了计算方便,当每次取25. 00mL草酸溶液时,配制适当浓度的标准KMnO4溶液,使在数值上c(H2C2O4)= 0.5V(KMnO4),这样只要测出KMnO4溶液的体积就可以快速得出所配草酸溶液的浓度,试计算标准KMnO4溶液的浓度__________。
4、简答题 A、B两种物质都是H、N、O、Na中的任意三种元素组成的强电解质,A的水溶液呈碱性,B的水溶液呈酸性,请找出A、B可能的两种组合,要求A,溶液中的水的电离程度小于A2溶液中水的电离程度;B1溶液中的水的电离程度小于啦溶液中水的电离程度:
(1)请写出下列各物质的化学式:
A1______,A2______,B1______,B2______.
(2)B1溶液中的水的电离程度小于B2溶液中水的电离程度,其原因是:
______.
5、选择题 某有机物6.4g完全燃烧生成8.8g?CO2和0.4mol?H2O,无其他物质生成,则下列说法中正确的是( )
A.该有机物仅含碳、氢两种元素
B.该有机物中不一定含有氧元素
C.该有机物中碳氢原子个数比为1:4
D.该有机物中碳、氢、氧质量比为3:1:12