1、填空题 在763 K和3.04×104kPa时,用CO与H2合成CH3OH:CO(g)+2H2(g) CH3OH(g)。
CH3OH(g)。
(1)设起始时,n(H2)∶n(CO)=m,平衡时CO转化率为α,CH3OH的体积分数为y,则m、α、y三者的关系是___________。
(2)将下表已知数据代入上述关系,进行计算,将结果填入表中:
?(3)根据表中数据,可得出最佳反应物的配比m是_________,原因是______________。
参考答案:(1)y=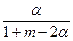 ×100%
×100%
(2)16.67%? 21.43%? 0.56
(3)2当m=2时,平衡气体中CH3OH的体积分数最大
本题解析:(1)设开始时CO为1 mol,则H2为m mol,
由:? CO+?2H2 ?CH3OH
?CH3OH
n始/mol:1?m?0
n变/mol:α?2α?α
n平/mol:1-αm-2α?α
平衡时n(总)=(1+m-2α)mol,
故y=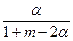 ×100%。
×100%。
(2)直接代入(1)式进行计算得:16.67%、21.43%、0.56。
(3)由(2)知当m=2时,为最佳配比。
本题难度:简单
2、选择题 二氧化氮存在下列平衡:2NO2(气)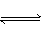 N2O4(气)(正反应为放热反应)在测定NO2的相对分子质量时,下列条件中较为适宜的是( )
N2O4(气)(正反应为放热反应)在测定NO2的相对分子质量时,下列条件中较为适宜的是( )
A.温度130℃、压强3.03×105Pa
B.温度25℃、压强1.01×105Pa
C.温度130℃、压强5.05×104Pa
D.温度0℃、压强5.05×104Pa
参考答案:C
本题解析:化学平衡:2NO2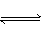 N2O4的正反应是气体体积减小的放热反应,温度较高,压强较低有利于平衡向逆反应方向移动,从而达到准确测定NO2的相对质量分子的目的。
N2O4的正反应是气体体积减小的放热反应,温度较高,压强较低有利于平衡向逆反应方向移动,从而达到准确测定NO2的相对质量分子的目的。
本题难度:简单
3、选择题 下列过程中,需要加快化学反应速率的是(?)
A.钢铁腐蚀
B.食物腐烂
C.塑料老化
D.炼钢
参考答案:D
本题解析:炼钢需要加快反应速率,钢铁腐蚀要减慢反应速率以延长钢铁的使用寿命,食物可放在冰箱中减慢腐败速率,塑料也要减慢其老化速率以延长塑料使用寿命。
点评:生产生活中有些反应要加快速率,有些反应要减慢速率,应区别对待。
本题难度:简单
4、选择题 对于可逆反应mA(g)+nB(g)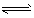 pC(g)+gD(g),若其他条件都不变,只是在反应前加入合适的催化剂,则两种v~t图像如下图;①a1=a2;②a1 <a2 ③b1=b2;④b1<b2;⑤t1>t2;⑥t1=t2;⑦两图中阴影部分面积相等;⑧右图阴影部分面积更大。以上正确的为
pC(g)+gD(g),若其他条件都不变,只是在反应前加入合适的催化剂,则两种v~t图像如下图;①a1=a2;②a1 <a2 ③b1=b2;④b1<b2;⑤t1>t2;⑥t1=t2;⑦两图中阴影部分面积相等;⑧右图阴影部分面积更大。以上正确的为
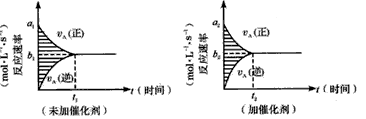
[? ]
A.②④⑤⑦
B.②④⑥⑧
C.②③⑤⑦
D.②③⑥⑧
参考答案:A
本题解析:
本题难度:一般
5、选择题 对于可逆反应:aA(g)+bB(g)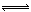 mC(g)+? nD(g);△H<0,下列说法正确的是
mC(g)+? nD(g);△H<0,下列说法正确的是
A.浓度改变平衡必移动
B.增大压强平衡必移动
C.升高温度平衡必移动
D.导入氦气平衡必移动
参考答案:C
本题解析:如果反应前后气体的体积不变,则通过改变压强改变浓度平衡不移动,因此选项A和B均不正确;正方应是放热反应,升高温度平衡一定向逆反应方向移动,C正确;如果容器的容积不变或反应前后气体的体积不变,则通入氦气平衡不移动,D不正确,答案选C。
本题难度:一般