1、填空题 (三选一)【化学―化学与技术】
硫酸是一种重要的化工原料,硫酸工业的“三废”处理之一是对尾气处理,其中一种方法便是用天然海水进行尾气脱硫。
(1)硫酸工业生产的主要设备有_______、________和吸收塔。在吸收塔内装有大量磁环的作用是____________,浓硫酸从塔顶喷下,SO3吸收操作采取_________形式(原理);硫酸工业的尾气主要成分有SO2、O2、N2等。
(2)天然海水主要含有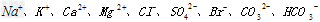 等离子。
等离子。
①天然海水pH约为8,原因是海水中________、_________离子水解所致。
②尾气进入吸收塔内,塔顶喷下大量海水,O2能将?H2SO3、HSO3-?、SO32-?等氧化,试写出其中一个反应的方程式:?________________。
③向氧化后的海水中加入天然海水,其目的是中和、稀释氧化后海水中生成的酸,最终排放出的海水中SO42-浓度与进入吸收塔的天然海水相比,?SO42-浓度________(填序号)。
A.减少 B.增大 C.不变 D.无法判断
2、填空题 (三选一)【化学-物质结构与性质】
以黄铁矿为原料生产硫酸的工艺流程图如下:
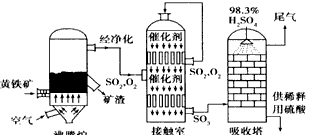
(1)将燃烧黄铁矿的化学方程式补充完整
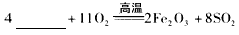
(2)接触室中发生反应的化学方程式是_____________________________
(3)依据工艺流程图判断下列说法正确的是(选填序号字母)___________ 。
a.为使黄铁矿充分燃烧,需将其粉碎
b.过量空气能提高SO2的转化率
c.使用催化剂能提高SO2的反应速率和转化率
d.沸腾炉排出的矿渣可供炼铁
(4)每160 g SO3气体与H2O化合放出260.6 kJ的热量,该反应的热化学方程式是____________________
(5)吸收塔排出的尾气先用氨水吸收,再用浓硫酸处理,得到较高浓度的SO2和铵盐。
①SO2:既可作为生产硫酸的原料循环再利用,也可用于工业制溴过程中吸收潮湿空气中的Br2。SO2吸收Br2的离子方程式是________________________________。
②为测定该铵盐中氮元素的质量分数,将不同质量的铵盐分别加入到 50.00 mL相同浓度的NaOH溶液中,沸水浴加热至气体全部逸出(此温度下铵 盐不分解),该气体经干燥后用浓硫酸吸收完全,测定浓硫酸增加的质量。 部分测定结果: 铵盐质量为10. 00 g和20. 00 g时,浓硫酸增加的质量相同;铵盐质量为30. 00 g 时,浓硫酸增加的质量为0. 68 g;铵盐质量为40.00 g时,浓硫酸的质量不变。 计算:该铵盐中氮元素的质量分数是____%;若铵盐质量为15. 00 g,浓硫酸增加的质量为____________________________ 。(计算结果保留两位小数)
3、选择题 下列关于硫酸工业生产过程的叙述错误的是
[? ]
A.在接触室中使用铁粉作催化剂 ?
B.在接触室中运用热交换技术可充分利用能源 ?
C.把硫铁矿磨成细粉末,可以提高原料的利用率 ?
D.该反应采用450℃~500℃主要是因为该温度下催化剂活性好
4、选择题 下列物质的分子中均含有羟基:①乙醇?②乙酸?③水?④碳酸;其中羟基氢活性最强是的:?
A.①
B.②
C.③
D.④
5、选择题 工业上制取硫酸铜不是直接用浓硫酸与铜反应,而是将铜丝浸入稀硫酸中并不断地从容器下部吹入细小的空气泡,这样做的优点是( )
①节省能源 ②不产生污染大气的SO2 ③提高?H2SO4的利用率 ④提高了Cu的利用率.
A.①②
B.①②③
C.②③④
D.全部