1��ѡ���� ���и���Ӧ�����ӷ���ʽ��,��д��ȷ����(? )
A�� NaOH��Һ�����ᷴӦ: 2H+ + 2OH- = 2H2O
B�� FeCl3��Fe��Ӧ: Fe3+ +Fe = 2Fe2+
C�����������������Ӧ: H+ + SO42- + Ba2+ +OH- = H2O + BaSO4
D������ͭ��ϡ���ᷴӦ: CuO + 2H+ = Cu2+ + H2O
�ο��𰸣�D
���������A. NaOH��Һ�����ᷴӦ:2H+ + 2OH- = 2H2O���ӷ���ʽδ����ӦΪH+ + OH- = H2O,A����
B.?FeCl3��Fe��Ӧ:? Fe3+ +Fe = 2Fe2+��ɲ��غ㣬Ӧ��Ϊ2Fe3+ +Fe = 3Fe2+��B��
C. ���������������Ӧ: H+ + SO42- + Ba2+ +OH- = H2O + BaSO4���������ʵ���ȹ�ϵӦΪ
2H+ + SO42- + Ba2+ +2OH- =2H2O + BaSO4,C����
D������ͭ��ϡ���ᷴӦ: CuO + 2H+ = Cu2+ + H2O����ȷ��
ѡD.
�����Ѷȣ���
2��ѡ���� �ں�ˮ���ۺ������У���ˮ���幤ҵ��һ����Ҫ��ɲ��֣�����һ������Ĺ�������Ԥ��Ũ�����ữ�ĺ�ˮ�У�ͨ������������Ȼ��ʹ���ɵ��������ռ�SO2��Ӧת��Ϊ�������Դﵽ������Ԫ�ص�Ŀ�ģ��й������������̵����»�ѧ�����У�����ȷ���ǣ�������
A����ˮ��Br-�ĵ���ʽΪ��

B����ˮ��ͨ������ʱ������Ӧ�����ӷ���ʽΪ��2Br-+Cl2=Br2+2Cl-
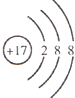
C��Cl-�Ľṹʾ��ͼΪ��
D��SO2�����嵥��ʱ������Ӧ�Ļ�ѧ����ʽΪ��2H2O+SO2+Br2=H2SO3+2HBr
�ο��𰸣�A�������ӵĵ���ʽҪ��[]�ѵ��Ӻ�Ԫ�ط������������������������8�����ӣ������ʽΪ��

����A��ȷ��
B���������������ܷ����û���Ӧ������������ӣ����ӷ�Ӧ����ʽΪ��2Br-+Cl2=Br2+2Cl-����B��ȷ��
C�������Ӻ�����3�����Ӳ㣬�������8�����ӣ������ӽṹʾ��ͼΪ��

����C��ȷ��
D�������ǿ�����ԣ�����������л�ԭ�ԣ�����������塢ˮ�ܷ���������ԭ��Ӧ��������������ᣬ��Ӧ����ʽΪ��2H2O+SO2+Br2=H2SO4+2HBr����D����
��ѡD��
���������
�����Ѷȣ���
3��ѡ���� ����ȷ��ʾ���з�Ӧ�����ӷ���ʽ�ǣ�������
A����Fe��NO3��2ϡ��Һ�м������3Fe2++4H++NO3-�T3Fe3++NO��+2H2O
B��ͭƬ��ŨHNO3��Cu+NO3-+4H+�TCu2++NO��+2H2O
C��̼�������Һ��������NaOH��Һ��ϼ��ȣ�NH4++OH-
NH3��+H2O
D��AlCl3��Һ�еμ�������ˮ��Al3++4NH3?H2O�TAlO2-+4NH4++2H2O
�ο��𰸣�A����Fe��NO3��2ϡ��Һ�м�����������ӷ�ӦΪ3Fe2++4H++NO3-�T3Fe3++NO��+2H2O����A��ȷ��
B��ͭƬ��ŨHNO3��Ӧ�����ӷ�ӦΪCu+2NO3-+4H+�TCu2++2NO2��+2H2O����B����
C��̼�������Һ��������NaOH��Һ��ϼ��ȵ����ӷ�ӦΪHCO3-+NH4++2OH-?��?.?NH3��+2H2O+CO32-����C����
D��AlCl3��Һ�еμ�������ˮ�����ӷ�ӦΪAl3++3NH3?H2O�TAl��OH��3��+3NH4+����D����
��ѡA��
���������
�����Ѷȣ���
4��ѡ���� ���л�ѧ��Ӧ�����ӷ���ʽ��ʾ��ȷ���ǣ�?��
A��̼����ܽ���ϡ�����У�
CO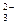 +2H
+2H
 CO
CO ��+H
��+H O
O
B����м��ϡ�������ò���������
2Fe+6H
 2Fe
2Fe +3H
+3H ��
��
C��NaHCO ��Һ��NaOH��Һǡ����ȫ��Ӧ��
��Һ��NaOH��Һǡ����ȫ��Ӧ��
H +OH
+OH
 H
H O
O
D����Ba��OH�� ��Һ����ε���ϡ������ǡ�ó����ԣ�
��Һ����ε���ϡ������ǡ�ó����ԣ�
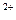 +2OH
+2OH +SO
+SO +2H
+2H
 BaSO
BaSO ��+2H
��+2H O
O