1��ѡ���� �������ӷ���ʽ��ȷ���ǣ�?��
A�����Ȼ�����Һ��ʴӡˢ��·�壺 Cu��Fe3����Cu2����Fe2+
B��̼�������Һ�����NaOH��Һ��Ӧ��Ca2++HCO3��+OH��=CaCO3��+H2O
C��Na2CO3��Һ��ͨ�����CO2��CO32��+CO2+H2O=2HCO3��
D��CH3COOH��Һ��NaOH��Һ��Ӧ��H++OH��=H2O
2��ѡ���� �������ӷ���ʽ����ȷ����?
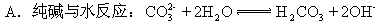

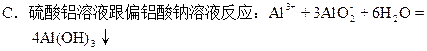
D������ͨ���������������Һ�У�2Cl2+2OH-=3Cl-+ClO-+H2O
3��ѡ���� �������ӷ���ʽ����д��ȷ���ǣ�������
A������ϡ���ᷴӦ��2Fe+6H+=2Fe3++3H2��
B������ʯ��ˮ��ϡ���ᷴӦ��OH-+H+�TH2O
C����������Һ���Ȼ�����Һ��Ӧ��2Ag++2Cl-�T2AgCl��
D����������ˮ��Ӧ��Na+H2O=Na++OH-+H2��
4��ʵ���� ʳ���к���һ������þ���������ʣ��ӵ����е����ʧ��Ҫ���������ʡ�ˮ�֡������е������Լ����ա����ȶ�����ġ���֪��
�����ԣ�IO3-��Fe3����I2����ԭ�ԣ�S2O32-��I��
3I2��6OH��=IO3-��5I����3H2O��KI��I2 KI3
KI3
(1)ijѧϰС��Լӵ��ν�������ʵ�飺ȡһ����ij�ӵ���(���ܺ���KIO3��KI��Mg2����Fe3��)������������ˮ�ܽ⣬����ϡ�����ữ����������Һ��Ϊ3�ݡ���һ����Һ�еμ�KSCN��Һ���Ժ�ɫ���ڶ�����Һ�м�����KI���壬��Һ�Ե���ɫ����CCl4��ȡ���²���Һ���Ϻ�ɫ����������Һ�м�������KIO3����μӵ����Լ�����Һ����ɫ��
�ټ�KSCN��Һ���Ժ�ɫ���ú�ɫ������_____________(�û�ѧʽ��ʾ)��CCl4�����Ϻ�ɫ��������___________(�õ���ʽ��ʾ)��
�ڵڶ�����Һ�м�������KI�����Ӧ�����ӷ���ʽΪ_______________________________________��__________________________________________________________________��
(2)KI��Ϊ�ӵ����ʳ���ڱ�������У����ڿ��������������ã�������������ʧ��
д����ʪ������KI��������Ӧ�Ļ�ѧ����ʽ��_____________________��
��I2����KI��Һ���ڵ��������£����Ƶ�KI3��H2O����������Ϊʳ�μӵ���Ƿ���ʣ�___________ (��ǡ���)����˵������_________________________________________________��
(3)Ϊ����ӵ���(����KI)���ȶ��ԣ��ɼ��ȶ������ٵ����ʧ�������������п�����Ϊ�ȶ�������_______��
A��Na2S2O3
B��AlCl3
C��Na2CO3
D��NaNO2