1��ѡ���� ��һ�����¶Ⱥ��ݻ�Ϊl L���ܱ�������Ͷ��A ��B��C������̬���ʵ�Ũ����ʱ��ı仯�����ͼ��ʾ�����н����в���ȷ����

A��t1ʱ��֮��,���ټ���һ������A,��ƽ��ʱA��ת���ʽ���
B��t1ʱ��֮��,3v(A)��=2v(C)�� ��v �����ʣ�
C��t1ʱ��֮��,�������¶ȣ���������ƽ��Ħ������������÷�ӦA���ĵķ���Ϊ���ȷ�Ӧ
D�����¶Ⱥ��ݻ��̶�����������£���ʼͶ��1molB��3molC��ƽ��ʱA���������Ϊ3/7
�ο��𰸣�C
����������÷�Ӧ�ķ���ʽΪ��2A?B+3C��A��ȷ��t1ʱ��֮��,���ټ���һ������A,�൱��������ѹǿ��ƽ�����淴Ӧ�����ƶ�������ƽ��ʱA��ת���ʽ��ͣ�
B��ȷ��t1ʱ��֮��,��Ӧ�Ѵ�ƽ��״̬���������淴Ӧ����֮��=��ѧ������֮�ȣ���3v(A)��=2v(C)����
C����t1ʱ��֮��,�������¶ȣ���������ƽ��Ħ�������������ڷ�Ӧ����������Ϊ���壬����ϵ���������䣬���Ի������������ʵ�����С�����ɵ�ƽ�����淴Ӧ�����ƶ���������Ӧ�ķ���Ϊ���ȷ�Ӧ��
D��ȷ���¶Ⱥ��ݻ��̶�����������£���ʼͶ��1molB��3molC��ƽ��ʱ����ʼʱͶ��2molA��Ϊ��Чƽ�⣻
�����Ѷȣ�һ��
2������� ��֪NO2��N2O4�����ת���� N2O4  ?2NO2��ij�¶�ʱ����1mol N2O4����ͨ�����Ϊ10L������ܱ������У�����������ɫ����Ӧ����4sʱNO2��Ũ��Ϊ0.04mol/L���پ���һ��ʱ���Ӧ����ƽ�⣬��ʱ������ѹǿΪ��ʼʱ��1.8����
?2NO2��ij�¶�ʱ����1mol N2O4����ͨ�����Ϊ10L������ܱ������У�����������ɫ����Ӧ����4sʱNO2��Ũ��Ϊ0.04mol/L���پ���һ��ʱ���Ӧ����ƽ�⣬��ʱ������ѹǿΪ��ʼʱ��1.8����
��1��ǰ4s����N2O4��Ũ�ȱ仯��ʾ��ƽ����Ӧ�ٶ�Ϊ?mol/L��s
��2����4sʱ�����ڵ�ѹǿΪ��ʼʱ��?��
��3����ƽ��ʱ�����ں�N2O4?mol
��4����ƽ��ʱ������NO2��Ũ��Ϊ?mol/L
��5��ƽ��ʱN2O4��ת����Ϊ??
�ο��𰸣���1��0.005mol/��L��s����2��1.2����3��0.2mol��4��0.16mol/L ��5��80%
���������N2O4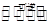 2 NO2
2 NO2
��1����Ӧ����4sʱNO2��Ũ��Ϊ0.04mol/L����v��NO2��="0.04mol/L" / 4s="0.04mol/(L��s)" ��v(N2O4)/v(NO2)=1/2����ǰ4����N2O4Ũ�ȱ仯��ʾ��ƽ����Ӧ����Ϊ0.005mol/(L��s)
��2�����µ��ݣ�ѹǿ����������ʵ��������ȡ���4��ʱ��n(NO2)="0.04mol/L" * 10L = 0.4mol
�μӷ�Ӧ��N2O4Ϊ0.2mol�����ʱ���������������ʵ���Ϊ1mol-0.2mol+0.4mol=1.2mol����ʼ��������ֻ��1mol N2O4���壬����4sʱ�����ڵ�ѹǿΪ��ʼʱ��1.2����
��3��ƽ��ʱѹǿΪ��ʼ��1.8������ƽ��ʱ�������������ʵ���Ϊ1.8mol����μӷ�Ӧ��N2O4Ϊx������(1-x)+2x=1.8?��ã�x=0.8mol������ƽ��ʱ�����ں�N2O4?�����ʵ���Ϊ��1mol-0.8mol=0.2mol��
��4��������ƽ��ʱ�����ں�N2O4?0.8mol���ʴ�ʱ������NO2��Ũ��Ϊ��0.8*2��/10 mol/L =0.16mol/L������ƽ��ʱ������NO2��Ũ��Ϊ0.16mol/L��
��5��ƽ��ʱ���ĵ�N2O4���ʵ���Ϊ��0.8mol ,��ƽ��ʱN2O4��ת����Ϊ��0.8mol/1mol=80% ��
��������ѧ��Ӧ����Ϊ�߿���Ҫ����֮һ����������������Ҫ��ϸߣ�����ȫ��Ҫ�����Կ��淴Ӧ����ѧ��Ӧ���ʵ����֪ʶ���������������գ�����һ���ķ��������뿼���Ѷȣ�����ƽʱӦ����ע�ػ�ѧ��Ӧ����������ݵ�ʵ����ϰ��
�����Ѷȣ�һ��
3��ѡ���� ��֪��I2(aq)��I��(aq) I3��(aq)��ijI2����KI�����Һ�У�c(I3��)���¶ȣ�T���Ĺ�ϵ����ͼ��ʾ���������κ�һ�㶼��ʾƽ��״̬��������˵���У���ȷ����
I3��(aq)��ijI2����KI�����Һ�У�c(I3��)���¶ȣ�T���Ĺ�ϵ����ͼ��ʾ���������κ�һ�㶼��ʾƽ��״̬��������˵���У���ȷ����
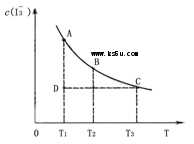
A����Ӧ I2(aq)��I��(aq)  I3��(aq)�ġ�H��0
I3��(aq)�ġ�H��0
B��״̬A��c(I2)��״̬D��С
C��A���Ӧ�ķ�Ӧ���ʴ���C���Ӧ�ķ�Ӧ����
D�������������䣬����Һ�м���KI���壬ƽ����C���ƶ���D��
�ο��𰸣�B
���������
��ȷ�𰸣�B
A������ȷ����ͼ�ó����¶����ߣ�I3�DŨ�ȱ�С��ƽ�������ƶ�����HС��0��
B����ȷ��
C������ȷ��A���Ӧ�ķ�Ӧ���ʲ���C���Ӧ�ķ�Ӧ���ʣ�A���¶ȵͣ�
D������ȷ�������������䣬����Һ�м���KI���壬���������ƶ���ƽ����C���ƶ���A�㣻
�����Ѷȣ�һ��
4��ѡ���� ij�¶��£����һ�����ܱ������н������¿��淴Ӧ��X(g)+Y(g) 2Z(g)+W(s)��������������ȷ����
2Z(g)+W(s)��������������ȷ����
A���ﵽƽ�������W������X��ת�����½�
B��������������ѹǿ����ʱ����Ӧ�ﵽƽ��
C���������¶ȣ����ƽ�ⳣ��������÷�ӦΪ���ȷ�Ӧ
D����Ӧ�����У�������ܶ�ʼ�ղ���
�ο��𰸣�C
���������W�ǹ��壬�ﵽƽ�������W��������ƽ���ƶ���Ӱ�죬A����W�ǹ��壬��Ӧǰ���������ʵ������䣬����ƽ��̬���Ƿ�ƽ��̬������������ѹǿ���䣬B����ƽ�ⳣ������˵��ƽ�������ƶ��������¶ȣ�ƽ�������ȷ�Ӧ�����ƶ���C��ȷ��W�ǹ��壬��Ӧǰ�������������غ㣬�������������䣬���Է�Ӧ������������ܶȼ�С��ƽ��ʱ���䣬D����
���������淴Ӧ�ﵽƽ��ʱ�����ӹ����Һ�������ƽ�ⲻ�ƶ�������Ӧ�в�ȫ�����壬��Ӧ���ݻ��̶����ݻ��н��У���������ܶȲ����״̬Ϊƽ��״̬��
�����Ѷȣ�һ��
5��ѡ���� ��ͼ�DZ�ʾ��2X (g)��Y (g) ?Z (g)��R (g)?�SH<0 �����巴Ӧ���ʣ��ԣ���ʱ�䣨t���Ĺ�ϵ��t1ʱ��ʼ�ı������������ı�������������ߵ���
?Z (g)��R (g)?�SH<0 �����巴Ӧ���ʣ��ԣ���ʱ�䣨t���Ĺ�ϵ��t1ʱ��ʼ�ı������������ı�������������ߵ���

A������Z����
B���Ӵ�ѹǿ
C�������¶�
D��ʹ�ô���
�ο��𰸣�D
�����������ͼ���Կ�����t1ʱ�ı���������Ӧ��������ƽ�ⲻ�ƶ�������Z���ʣ�v��С��ƽ�����ƣ�A�����Ӵ�ѹǿ��v����ƽ�����ƣ�B���������¶ȣ�v����ƽ�����ƣ�C����ʹ�ô�������ͬ�ȳ̶ȵ��������淴Ӧ���ʣ�ƽ�ⲻ�ƶ���ѡD��
��������ѧƽ��ͼ���ǻ�ѧƽ���һ����Ҫ֪ʶ�㣬����߿��������飬�����ڱ���������Ӧѧ�����ͼ��
�����Ѷȣ�һ��