| �߿�ʡ������ | |
|
|
| �߿�ʡ������ | |
|
|
|
�߿���ѧ֪ʶ����������Ӧ������ƽ����йؼ��㡷����ǿ����ϰ��2017�����°棩(��)
 2SO3(g) ��H<0������ͼ���в���ȷ����______ (����ĸ��ţ��� 2SO3(g) ��H<0������ͼ���в���ȷ����______ (����ĸ��ţ���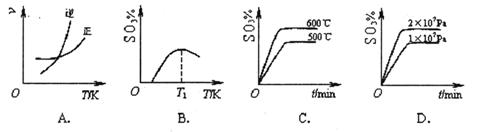 (3)ij�¶���SO2(g)+  O2(g) O2(g)  SO3(g) ��H=-98KJ/mol SO3(g) ��H=-98KJ/mol�ٿ�ʼʱ������̶����ܱ������м���4mol SO2 (g)��1mol O2 (g)���ﵽƽ��ʱ ���ų�196 KJ�����������¶���SO2��ƽ��ת����Ϊ______ ����֪��̬�������ȼ����Ϊ296KJ/mol������S(s)����2 molSO3(g)�Ħ�HΪ____________ (4)����SO42-����BaCl2��Һ������ʱ��BaSO4��Ksp=1.08��10-10���ֽ��������BaCl2��Һ��2.0��10��3mol/L��H2SO4��Һ��ϡ���Ҫ����BaSO4������ԭBaCl2��Һ����СŨ��Ϊ____________ �ο��𰸣���12�֣� ��������� �����Ѷȣ�һ�� 4������� ��12�֣����з�Ӧ��CO(g)+ H2O(g) �ο��𰸣���12�֣���ÿ��3�֣�(1) ��? (2) ���淴Ӧ?�� 0��x��3? (3) �� �����������1������Ӧ�Ƿ��ȷ�Ӧ�����������¶ȣ�ƽ�����淴Ӧ�����ƶ���ƽ�ⳣ����С�� �����Ѷȣ�һ�� 5������� (1)��ѧƽ�ⳣ��K��ʾ���淴Ӧ�Ľ��г̶ȣ�KֵԽ��ʾ���淴Ӧ���е�Խ��ȫ��Kֵ��С���¶ȵĹ�ϵ�ǣ��¶����ߣ�Kֵ?(�һ��������һ����С����������Ҳ���ܼ�С��)�� �ο��𰸣�(1)��������Ҳ���ܼ�С ���������(1)��ѧƽ�ⳣ�����¶��йأ�������ӦΪ���ȷ�Ӧ�������¶ȣ�ƽ�ⳣ������������ӦΪ���ȷ�Ӧ�������¶ȣ�ƽ�ⳣ����С�������¶����ߣ�Kֵ��������Ҳ���ܼ�С�� �����Ѷȣ�һ�� |
| ���� �� С������ӡ�� �������� ���ر��� �����ض����� | |
| ��һƪ���߿���ѧ֪ʶ���ܽᡶ���ʵ�����.. | |
| �����Ŀ | |