1������� Ԫ�����ڱ���Ԫ����������ѧϰ���о�������ʵ�����к���Ҫ�����á��±��г��ˢ١������Ԫ�������ڱ��е�λ�á���ش�
��
����
| ��A
| ��A
| ��A
| ��A
| ��A
| ��A
| ��A
| 0
|
2
| ?
| ?
| ?
| ��
| ?
| ��
| ?
| ?
|
3
| ��
| ��
| ��
| ?
| ?
| ?
| ��
| ��
|
4
| ��
| ?
| ?
| ?
| ?
| ?
| ��
| ?
|
(1)�����Ԫ����(��Ԫ�ط���)����?�����л�ѧ��������õ���?��
�ݺ͢��γɻ�����ĵ���ʽ?
(2)����ЩԪ�ص�����������Ӧ��ˮ�����У�������ǿ����(�ѧʽ)��?
������ǿ����?�����Ե���?��д������֮�����Ӧ�Ļ�ѧ����ʽ??��
?
?
(3)�١��ڡ�������Ԫ�ذ�ԭ�Ӱ뾶�ɴ�С��˳������Ϊ?(��Ԫ�ط���)��
(4) �õ���ʽ��ʾ��Ԫ�����Ԫ���γɻ�����Ĺ���?��
(5) �ڢٺ͢��л�ѧ��������õ���?
(6)�ڢߺ͢��л�ѧ��������õ���?���û�ѧʵ��֤���ķ��������ӷ���ʽ��
����?
���ӷ���ʽ??
�ο��𰸣���1��C? Ar?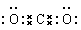
��2�� KOH? HClO4? Al(OH)3? KOH +HClO4��KClO4 +H2O? KOH + Al(OH)3��KAlO2 +2H2O
(3) K��Na��Mg? (4)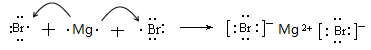 ��5��K?
��5��K?
(6)? Cl?ȡ�����廯����Һ������ˮ����Һ��Ϊ�Ȼ�ɫ����ǽ�����Cl��Br? Cl2 + 2Br-�� 2Cl- + Br2
�����������1������Ԫ�������ڱ��е����λ�ÿ�֪�١������Ԫ�طֱ���Na��K��Mg��Al��C��O��Cl��Br��Ar��Ar��ϡ������Ԫ�أ���ѧ��������á��ݺ͢��γɻ�������CO2�����й��ۼ��Ĺ��ۻ���������ʽ��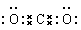 ��
��
��2�������Ի�ǽ�����Խǿ������������ˮ����ļ��Ի�����Խǿ����KOH�ļ�����ǿ��HClO4��������ǿ�� Al(OH)3�������������
��3��ͬ������������ԭ�Ӱ뾶��С��ͬ�������϶���ԭ�Ӱ뾶������������Ԫ�ص�ԭ�Ӱ뾶��С˳����K��Na��Mg��
��4��ʾ��Ԫ�����Ԫ���γɻ��������廯þ���������Ӽ������γɹ��̿ɱ�ʾΪ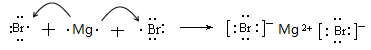 ��
��
��5��ͬ�������϶��£�����������ǿ������K�Ľ�����ǿ��Na�Ľ����ԡ�
��6��ͬ�������϶��£��ǽ���������������Cl�ķǽ�����ǿ��Br�ķǽ����ԡ��ɸ��ݷǽ�����ǿ�ĵ���ת��������ȡ�����廯����Һ������ˮ����Һ��Ϊ�Ȼ�ɫ����ǽ�����Cl��Br�����Ե����ӷ���ʽ��Cl2 + 2Br-��2Cl- + Br2��
�����������ǻ���������Ŀ��飬���ض�ѧ������֪ʶ���̺�ѵ����ͬʱ��ּ�ڿ���ѧ��������û���֪ʶ���ʵ�����������������������ѧ���������������淶����������
�����Ѷȣ�һ��
2������� X��Y��ZΪ���ֶ�����Ԫ�أ����������ڱ��е�λ�ù�ϵ��ͼ��ʾ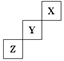 ���ݴ˻ش��������⣺
���ݴ˻ش��������⣺
��1��XԪ�ص�����Ϊ?�����γɵĵ���Ϊ?���÷���ʽ��ʾ���� He?������Ԫ�ص�ij��ԭ���ں�������������������ȣ����ԭ�ӵ�Ħ��������??�����������Ƿ��ص�ͼƬԤ�⣬�����������������������ֵ�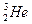 ������ԭ����
������ԭ����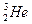 �Ĺ�ϵ��??��
�Ĺ�ϵ��??��
��2��YԪ���γɵ��ʵĵ���ʽ��?��Y���ʵ�������?���ǿ�ڡ����ߡ����ڡ���O2�������ԣ�������Ӧ�Ļ�ѧ����ʽ˵��?��
��3��Ԫ��Z����Ȼ���еĴ�����̬Ϊ?������ţ���ֻ�л���̬����ֻ������̬���ۼ�������̬�����л���̬����ZԪ�ص�ijЩ������ȼ�պ��������صĴ�����Ⱦ������Ҫԭ����?��
��4��YԪ�ء�ZԪ����H2����ʱ�������仯��?����������ȡ����������ȡ�����ǰ�߷��ȣ��������ȡ����ߡ�ǰ�����ȣ����߷��ȡ����������仯�Ĵ�С��ϵΪǰ��?������������������ߡ���������
�ο��𰸣���1������He ��4g/mol ��ͬλ�أ���ÿ��1�֣���2�� ?��1�֣���ǿ�ڣ�1�֣���2F2 + 2H2O =" 4HF" + O2����2�֣���3���ۣ�1�֣�����S��ijЩ������ȼ�պ�����SO2�����γ����꣬Σ��������2�֣���?��4�������ȣ�����ÿ��1�֣���
?��1�֣���ǿ�ڣ�1�֣���2F2 + 2H2O =" 4HF" + O2����2�֣���3���ۣ�1�֣�����S��ijЩ������ȼ�պ�����SO2�����γ����꣬Σ��������2�֣���?��4�������ȣ�����ÿ��1�֣���
���������������ͼ��ʾλ�õĶ�����Ԫ�أ����жϳ�X��Y��Z�ֱ�Ϊ He ��F��S��Heֻ���γɵ�ԭ�ӷ��ӣ���������ͬ����������ͬ������ԭ�ӻ�Ϊͬλ�أ���ɽ�ڸ������ڵ���S��SԪ��ȼ�պ�������Ⱦ������SO2��Ԫ�صķǽ�����Խǿ�����ɵ��⻯��Խ�ȶ����ų�������Խ�ࡣ
�����Ѷȣ���
3��ѡ���� �������е�A��B��C��D��E����Ԫ�أ�ԭ��������������A��D��C��E�ֱ�ͬ���壬AΪ�ǽ���Ԫ�أ���A��B��ԭ������֮�͵���C��ԭ��������C2����D���ĺ����������ȡ�������˵����ȷ����
A��B��Aֻ���γɻ�����BA3?
B��C��ԭ�Ӱ뾶�����Ӱ뾶���ֱ�С��D��ԭ�Ӱ뾶�����Ӱ뾶
C��A��B��C�γɵĻ�������ܴٽ�ˮ�ĵ��룬Ҳ��������ˮ�ĵ���?
D��A��D������C�γ�ԭ�Ӹ�����Ϊ1�U1��2�U1�Ļ������A2C2��D2C2�Ļ�ѧ��������ͬ
�ο��𰸣�C
�����������C��Eͬ���壬����C2������C��O��E��S��C2����D���ĺ����������ȣ�D��Na��A��Dͬ���壬AΪ�ǽ���Ԫ�أ�A��H��A��B��ԭ������֮�͵���C��ԭ��������B��N��A��B��A�γɻ�����NH3��N2H4�ȣ�B��Na��ԭ�Ӱ뾶����O��Na+���Ӱ뾶С��O2-�뾶��C��A��B��C�γɵĻ�����ΪHNO3��HNO2�ܴٽ�ˮ�ĵ��룬NH4NO3��NH4NO2������ˮ�ĵ��룻D��H2O2��ѧ�������Ǽ��Լ��ͷǼ��Լ���Na2O2�Ļ�ѧ�����������Ӽ��ͷǼ��Լ���
�����Ѷȣ�һ��
4��ѡ���� ���¼���װ������ȷ���� ?
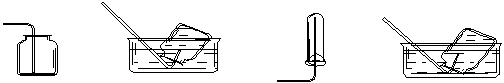
A.CO2���ռ�
B.NO���ռ�
C.O2���ռ�
D.NH3���ռ�
�ο��𰸣�AB
������������������CO2���ܶȴ��ڿ����ģ�����Ӧ���������ſ������ռ���A��ȷ��NO���ױ���������NO2������ֻ������ˮ���ռ���B��ȷ��O2���ܶȴ��ڿ����ģ�����Ӧ���������ſ������ռ���C��ȷ��������������ˮ��Ӧ���������ſ������ռ���D����ȷ����ѡAB��
���㣺���鳣�������ռ��������ж�
����������������ռ������ǣ�1.��ˮ���������ڲ�������ˮ�����塣����������������2.�����ſ������������ڱȿ����ܶȴ�����ˮ�����壬���������̼��������3�������ſ������������ڱȿ����ܶ�С������ˮ�����壬���簱����
�����Ѷȣ���
5��ѡ���� ���ֶ�����Ԫ�ص�ԭ�Ӱ뾶����Ҫ���ϼ����±���
Ԫ�ش���
| X
| Y
| Z
| W
|
ԭ�Ӱ뾶/pm
| 160
| 143
| 70
| 66
|
��Ҫ���ϼ�
| +2
| +3
| +5��+3��-3
| -2
|
������������ȷ����
A��X��YԪ�صĽ�����X<Y
B��X�����ڿ�����ȼ�տ����γɻ�����X3Z2
C�� X��Y��������������û���Ӧ
D��һ�������£�W���ʿ��Խ�Z���ʴ����⻯�����û�����
�ο��𰸣�A
�������������Ԫ�ص���Ҫ���ϼۺ�ԭ�Ӱ뾶��֪��X��þ��Y��Al��Z��N��W��O��ͬ�����������ҽ��������������Խ�������þ��������A����ȷ��þ�����ڵ�����ȼ�գ����ɵ���þ��B��ȷ���ƺ�ˮ��Ӧ��þ������CO2��ȼ�գ�C����ȷ���������ԺͰ�����Ӧ���ɵ�����D��ȷ����ѡA��
�����Ѷȣ�һ��