1、填空题 (10分)农村还有些家庭直接用河水或池塘水或井水龙头作为生活饮用水,一般是把水担回家倒入水缸,加明矾使水澄清,加漂白粉进行消毒,煮沸消除暂时硬度,明矾的化学式为?,写出它溶于水后生成胶体的离子方程式:?。漂白粉的成分是?,它在自然条件下能产生次氯酸,次氯酸的氧化性很强,能杀死病菌。写出漂白粉在空气中生成次氯酸的化学方程式:?。煮沸时形成水垢的成份是?(填化学式)
2、填空题 (9分)实验室要配制100mL? 0.5mol・L-1的NaCl溶液,试回答下列各题。
(1)经计算,应该用托盘天平称取NaCl固体_________g。
(2)若用NaCl固体配制溶液,需使用的玻璃仪器有_________________?______________
(3)配制过程有以下操作:A.移液,B.称量,C.洗涤,D.定容,E.溶解,F.摇匀。其正确的操作顺序应是_____________________________ (填序号)。
(4)下列操作会导致所得溶液浓度偏低的是______________________________(填序号)。
A.定容时仰视容量瓶刻度线? B.定容时俯视容量瓶刻度线
C.将溶解冷却的溶液转入容量瓶后就直接转入定容操作
D.定容后,把容量瓶倒置摇匀后发现液面低于刻度线,便补充几滴水至刻度处
3、实验题 实验室以空气(O2体积分数20%)为原料,在无碳、无水的环境下,用下图A装置制备臭氧(3O2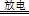 2O3)。
2O3)。
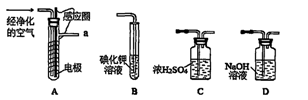
(1)空气通入A装置之前,应先后通过上述装置中的?、?(填装置序号)。
(2)臭氧与碘化钾溶液反应为:2KI+O3+H2O=2KOH+I2+O2。将a处气体通入装置B,溶液中的现象为?。
(3)为测定O2转化为O3的转化率,将装置B中的溶液全部转入另一容器中,加入CC14,经萃取、分液、蒸馏、冷却、称重,得I2固体0.254g。
①萃取操作所用玻璃仪器的名称?。
②若实验时通入空气1.12L(标准状况),O2的转化率为?。
③测定时需在A、B装置间连接装置D,原因是?。
(4)工业上分离O3和O2,可将混合气体液化后再分离,下列分离方法合理的是?(填序号)。
A.过滤 B.分馏 C.分液 D.萃取
(5)臭氧可用于含CN一碱性电镀废水的处理。第i步:CN一转化为OCN-;第ii步:OCN一继续转化为CO32一及两种单质气体。若第ii步转化时,O3与OCN-物质的质量之比为3∶2,该步反应的离子方程式为?。
4、选择题 下列实验装置图(有些图中部分夹持仪器未画出)不能达到其实验目的的是?