|
�߿���ѧ֪ʶ��������ԭ���ԭ������Ƶ����̣�2017�����°棩(ʮ)
2017-11-05 23:32:32
��Դ:91������
����:www.91exam.org �� �� �� ��
|
1��ѡ���� ������������ȷ����
[? ]
A������ԭ������������IJ��ϱ��������ֽ���
B����ͭ��п���缫������ͭ��Һ��ɵ�ԭ�����ͭ�Ǹ���
C����������������������ʱ��������Һ�Ӵ������ȱ���ʴ
D��ͭпԭ��ع���ʱ������13?gп���ܽ⣬��·�о���0.4?mol����ͨ��
�ο��𰸣�D
���������
�����Ѷȣ�һ��
2��ѡ���� A��B��C���ǽ�����A�л���Cʱ��A�ȸ�ʴ��A��B���ԭ���ʱ��AΪ��ص���������A��B��C���ֽ����Ļ��˳��Ϊ �� �� A��A��B��C B��A��C��B C��B��A��C D��B��C��A
�ο��𰸣�C
�����������
�����Ѷȣ���
3������� ��10�֣�Q��W��X��Y��Z��5�ֶ�����Ԫ�أ�ԭ������������Q��W��ɵĻ���������Ȼ������Ҫ�ɷ֣�W��Y��X��Y��ɵĻ������ǻ������ų��Ĵ�����Ⱦ�Y��Z���γ�ԭ�Ӹ�����Ϊ1�U1��l�U2���������ӻ����
��1��W��Ԫ�����ڱ��е�λ����?����?�塣
��2����ҵ�ϳ�XQ3�Ƿ��ȷ�Ӧ�����д�ʩ�У����ܼӿ췴Ӧ���ʣ��������ԭ����������?������д��ţ�
A�������¶�
B���������
C����XQ3��ʱ�����ȥ
D������Ӧ��ϵ��ѹǿ
| ��3��2.24 L����״����XQ3��200 mL l mol/L QXY3��Һ���պ�������Һ������Ũ�ȴӴ�С��˳����?���������ӷ��ű�ʾ��
��4��WQ4Y��Y2�ķ�Ӧ�ɽ���ѧ��ת��Ϊ���ܣ��乤��ԭ������ͼ��ʾ��a���ĵ缫��Ӧ��?��
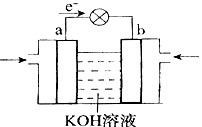
��5����֪��W��s��+Y2��g��=WY2��g����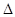 H=��393.5kJ/mol H=��393.5kJ/mol
WY��g��+ Y2��g��=WY2��g���� Y2��g��=WY2��g����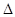 H=��238.0kJ/mol���� 24g W��һ������Y2��Ӧ���ų�����362.5 kJ�����ò���ɷּ����ʵ���֮��Ϊ?�� H=��238.0kJ/mol���� 24g W��һ������Y2��Ӧ���ų�����362.5 kJ�����ò���ɷּ����ʵ���֮��Ϊ?��
��6��X��Z��ɵ�һ�����ӻ��������ˮ��Ӧ�������ּ�÷�Ӧ�Ļ�ѧ����ʽΪ?��
�ο��𰸣���1���ڶ����ڡ��ڢ�A�塣?��2��D?��3��c(NO3-)��c( H+)��c(NH4+)��c(OH-)
��4��CH4 �C 8e- + 10OH- = CO32- + 7H2O?��5��CO2��CO? 1��8.24
��6��Na3N + 4H2O =" 3NaOH" + NH3.H2O
���������Q��W��ɵĻ���������Ȼ������Ҫ�ɷ֣�����Q��H��W��C���������ų��Ĵ�����Ⱦ����Ҫ��̼��������͵�����������X��N��Y��O��Y��Z���γ�ԭ�Ӹ�����Ϊ1�U1��l�U2���������ӻ����˵��Z����Ԫ�ء�
��2�����ĺϳ��Ƿ��ȵġ������С�Ŀ��淴Ӧ�������¶ȣ�������ƽ��������Ӧ������У���������ƽ��״̬����XQ3��ʱ�����ȥ�ή�ͷ�Ӧ���ʣ���ȷ�Ĵ���D��
��3��0.1molNH3��0.2molHNO3��Ϻ������������Һ�к��е�������NH4NO3��HNO3������������Һ������Ũ�ȴӴ�С��˳����c(NO3-)��c( H+)��c(NH4+)��c(OH-)��
��4�����ݵ��ӵ����������֪a�Ǹ�����Ӧͨ����飬����a���ĵ缫��Ӧ��CH4 �C 8e- + 10OH- = CO32- + 7H2O��
��5�����������Ȼ�ѧ����ʽ�ϲ��ɵõ�W��s��+1/2Y2��g��=WY��g����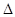 H=��155.5kJ/mol�� H=��155.5kJ/mol��
���24gC��ȫȼ�շų���������787kJ������ȫȼ�շų���������311 kJ����ʵ�ʷų�362.5
kJ�����Բ�����CO��CO2�Ļ�������ʮ�ֽ��淨�ɼ���CO��CO2�����ʵ���֮����

��6��X��Z�ֱ���N��Na���仯�ϼ۷ֱ��ǣ�3�ۺͣ�1�ۣ������仯ѧʽΪNa3N����Ӧ�ķ���ʽΪNa3N + 4H2O =" 3NaOH" + NH3.H2O��
�����Ѷȣ�һ��
4������� (9��)����������ԭ��Ӧ��2Ag��(aq)��Cu(s)===Cu2��(aq)��2Ag(s)��Ƶ�ԭ�������ͼ��ʾ��
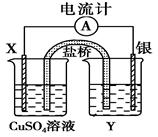
��ش��������⣺
(1)�缫X�IJ�����______���������ҺY��____________��
(2)���缫Ϊ��ص�________���������ĵ缫��ӦΪ__________________��X�缫�Ϸ����ĵ缫��ӦΪ____________________________________________________��
(3)���·�еĵ����Ǵ�________�缫����________�缫��
�ο��𰸣�(9��)? (1)ͭ(1��)? AgNO3��Һ(1��)��(2)��(1��)��
2Ag����2e��===2Ag��(2��)? Cu��2e��===Cu2����(2��)
(3)X(Cu) (1��)��Y(Ag) (1��)
���������������ɵ�������ԭ��Ӧ��֪��Cu���ϼ����ߣ������������������缫��ӦʽΪCu��2e��===Cu2���� �����ӻ��ϼ۽��ͣ�����ԭ����������Ӧ�������缫�����Ե缫��ӦΪ2Ag����2e��===2Ag���������ҺY��AgNO3��Һ�����·�еĵ��ӴӸ�����ͭ����������������
�����Ѷȣ�һ��
5������� ��12�֣�NOx������β���е���Ҫ��Ⱦ��֮һ��
��1��NOx���γ����꣬д��NO2ת��ΪHNO3�Ļ�ѧ����ʽ�� ��
��2����������������ʱ������N2��O2��Ӧ����֪�������£�N2��g��945 kJ/mol ��O2��g��498 kJ/mol ��NO��g��630 kJ/mol
д���÷�Ӧ���Ȼ�ѧ����ʽ: ��
��3��������β��ϵͳ��װ�ô�ת����������Ч����NOX���ŷš�
�ٵ�β���п�������ʱ��NOX�ڴ�ת�����б���ԭ��N2�ų���д��NO��CO��ԭ�Ļ�ѧ����ʽ�� ��
�ڵ�β���п�������ʱ����ת�����еĽ�������������NOX�����Ρ�����������˳�����£�12MgO <2oCaO <38SrO<56BaO��ԭ���� ����֪��Ԫ�صĽ���������ǿ�������������NOX��������������ǿ����
��4��ͨ��NOx�������ɼ��NOx�ĺ������乤��ԭ��ʾ��ͼ����:

��Pt�缫�Ϸ������� ��Ӧ(���������ԭ��)��
��д��NiO�缫�ĵ缫��Ӧʽ: ��
�ο��𰸣���1��3NO2+2H2O=2HNO3+NO����2�֣���2��N2(g)+O2��g��=2NO(g) ��H=+183KJ/mol����2�֣�
��3���١�2NO+2CO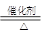 N2+2CO2 ��2�֣� N2+2CO2 ��2�֣�
�ڡ���Mg��Ca��Sr��Ba����������֪�����Ǿ����ڵڢ�A�壬ͬһ�������϶��£�ԭ�Ӱ뾶��������������ǿ����2�֣� ��4���١���ԭ�� ��2�֣� �ڡ�NO+O2--2e-=NO2����2�֣�
�����������1��NO2����ˮ���������NO����Ӧ�Ļ�ѧ����ʽΪ3NO2+2H2O=2HNO3+NO��
��2�����ڷ�Ӧ�ȣ���ѧ���������յ������뻯ѧ���γ�ʱ�ų��������IJ�ֵ����÷�Ӧ�ķ�Ӧ��=945 kJ/mol��498 kJ/mol��2��630 kJ/mol����183kJ/mol�����Ը÷�Ӧ���Ȼ�ѧ����ʽΪN2(g)+O2��g��=2NO(g) ��H=+183KJ/mol��
��3���ٵ�β���п�������ʱ��NOX�ڴ�ת�����б���ԭ��N2�ų���CO������ΪCO2������NO��CO��ԭ�Ļ�ѧ����Ϊ2NO+2CO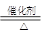 N2+2CO2�� N2+2CO2��
��Ԫ�صĽ�����Խǿ�������������NOX������������Խǿ������Mg��Ca��Sr��Ba����������֪�����Ǿ����ڵڢ�A�壬ͬһ�������϶��£�ԭ�Ӱ뾶��������������ǿ�����Խ����������NOX��������������ǿ��
��4����������Pt�缫ͨ�룬���Pt�缫��������ԭ����������õ����ӣ�������ԭ��Ӧ��
��NiO�缫�Ǹ���ͨ��NO��NOʧȥ���ӷ���������Ӧ���缫��ӦʽΪNO+O2--2e-=NO2��
���㣺���鵪��������������Լ�ԭ���ԭ����Ӧ��
�����Ѷȣ�һ��
| 
 H=��393.5kJ/mol
H=��393.5kJ/mol Y2��g��=WY2��g����
Y2��g��=WY2��g���� H=��238.0kJ/mol���� 24g W��һ������Y2��Ӧ���ų�����362.5 kJ�����ò���ɷּ����ʵ���֮��Ϊ?��
H=��238.0kJ/mol���� 24g W��һ������Y2��Ӧ���ų�����362.5 kJ�����ò���ɷּ����ʵ���֮��Ϊ?��