1、选择题 以下各粒子中,所有原子都满足最外层为8电子结构的是(?)
A.SiF4
B.BF3
C.SF6
D.PCl5
参考答案:A
本题解析:共价化合物中元素的化合价的绝对值之和和元素原子的最外层电子数之和满足8,即说明该原子满足8电子稳定结构。所以选项A是正确的。
本题难度:一般
2、填空题 A、B、C、D、E、F均为短周期主族元素,且原子序数依次增大。短周期元素中C的原子半径最大,B、E同族,E的最外层电子数是电子层数的2倍,A的最高价氧化物水化物为H2AO3,D是地壳中含量最高的金属元素。
(1)A的元素符号是________,C2B2的电子式为________。
(2)B、C、D、F的离子半径由大到小的顺序是________(用离子符号表示)。
(3)E和F相比,非金属性强的是________(用元素符号表示),下列事实能证明这一结论的是________(用符号填空)。
①常温下E的单质呈固态,F的单质呈气态 ②气态氢化物的稳定性:F>E ③E和F形成的化合物中,E显正价 ④F单质能与E的氢化物发生置换反应 ⑤E和F的氧化物的水化物的酸性强弱 ⑥气态氢化物的还原性:E>F
(4)把CDB2溶液蒸干所得的固体物质为________(填化学式)。
(5)C和F可组成化合物甲,用惰性电极电解甲的水溶液,电解的化学方程式为__________________________。
(6)A、B、C三种元素组成的常见化合物乙的溶液中,离子浓度由大到小的顺序为________,pH=10的乙溶液中由水电离产生的c(OH-)=________mol・L-1。
参考答案:(1)C 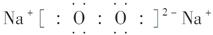
(2)Cl->O2->Na+>Al3+
(3)Cl ②③④⑥
(4)NaAlO2
(5)2NaCl+2H2O 2NaOH+H2↑+Cl2↑
2NaOH+H2↑+Cl2↑
(6)c(Na+)>c (CO32―)>c(OH-)>c(HCO3―)>c(H+) 10-4
本题解析:根据提供信息,A为C,B为O,C为Na,D为Al,E为S,F为Cl。(2)O2-、Na+、Al3+核外两个电子层,Cl-核外三个电子层,根据具有相同电子层结构的粒子,核电荷数越大,粒子半径越小,则离子半径大小为Cl->O2->Na+>Al3+。(3)S、Cl同周期,非金属性:Cl>S。①常温下单质的状态不能证明非金属性强弱;②气态氢化物越稳定,非金属性越强;③元素形成的化合物中显负价,说明得电子能力强,从而证明非金属性强;④非金属性强的元素对应的单质氧化性更强;⑤根据元素最高价氧化物的水化物酸性证明非金属性强弱,题中未标明最高价,不能证明;⑥气态氢化物还原性越弱,非金属性越强。
(6)Na2CO3溶液中由于CO32―水解溶液显碱性,pH=10的Na2CO3溶液中水的电离得到促进,由水电离出的c(OH-)=10-4 mol/L。
点拨:本题考查元素推断,考查考生对物质结构、元素周期律的理解能力。难度中等。
本题难度:一般
3、选择题 下列微粒的结构示意图中,表示氟离子的是
A.
B.
C.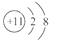
D.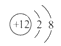
参考答案:A
本题解析:氟离子的质子数为9,核外电子排布为两层,分别为2、8,故答案为A
本题难度:一般
4、选择题 下列说法正确的是
A.第ⅦA族元素的非金属性比第ⅥA族元素的强
B.第三周期元素的简单阳离子半径从左到右逐渐减小
C.第ⅤA族元素非金属氧化物对应的水化物的酸性从上到下依次减弱
D.依据元素周期表、周期律推测尚未发现的第七周期第ⅦA族元素应为非金属元素
参考答案:B
本题解析:A、应该是同周期第ⅦA族元素的非金属性比第ⅥA族元素的强,A不正确;B、由于核外电子排布相同的微粒,其微粒半径随原子序数的增大而减小,因此第三周期元素的简单阳离子半径从左到右逐渐减小,B正确;C、同主族自上而下非金属性逐渐降低,因此第ⅤA族元素非金属元素最高价氧化物对应的水化物的酸性从上到下依次减弱,C不正确;D、依据元素周期表、周期律推测第七周期第ⅦA族元素应为金属元素,D不正确,答案选B。
本题难度:一般
5、选择题 六种短周期元素(a、b、c、d、e、f)的原子序数依次增大。其中a与e同主族,b与f同主族,e与f同周期;常温下a、e的单质状态不同;d的核电荷数是b的最外层电子数的2倍;单质f是一种重要的半导体材料。由此可推知
A.a、c两种元素只能组成化学式为ca3的化合物
B.b、c、d分别与a形成的化合物,沸点由高到低依次为:d>c>b
C.原子半径由大到小的顺序是 e>f>b>c>a
D.元素的非金属性由强到弱的顺序是 d>c>f>b
参考答案:C
本题解析:单质f是一种重要的半导体材料,即为硅。b为碳。d的核电荷数是b的最外层电子数的2倍,d是氧;常温下a、e的单质状态不同,说明分别是氢和钠,则c为氟。A.a、c两种元素只能组成化学式为HF,错误;B.b、c、 d分别与a形成的化合物分别是CH4,HF,H2O,根据常温下的状态可知,水的沸点是最高的,另外HF中存在氢键比甲烷的沸点高,故沸点由高到低依次为:d>c>b,正确。C.原子半径由大到小的顺序是Na>Si>C>F>O,正确。D.元素的非金属性由强到弱的序是 F>O >C>Si ,错误。
本题难度:一般