1��ѡ���� �������������ݹ�-���Ͻ�ֱ�Ͷ��������ϡ���������������������Һ�У�����ʾ�����������Ҳ��������������Һ��Ӧ�ų���������ַ�Ӧ��ò���������������Ϊ3��7����ͬ״���£�����úϽ��й���������ʵ���֮��Ϊ��������
A��3��7
B��7��3
C��2��1
D��1��1
�ο��𰸣���ԭ������к���xmolSi��ymolAl��
�費�����ᷴӦ��ֻ��NaOH��Һ��Ӧ��
��-���Ͻ�Ͷ��������ϡ�����У�������Ӧ2Al+6HCl=2AlCl3+3H2����
�������������ʵ���Ϊ��n��H2��=1.5n��Al��=1.5ymol��
��-���Ͻ�Ͷ������������������Һ�У�
2Al+2NaOH+2H2O=2NaAlO2+3H2��
1?3
y? 1.5y
Si+2NaOH+H2O=Na2SiO3+2H2��
1? 2
x?2x
�������������ʵ���Ϊ��n��H2��=2xmol+1.5ymol��
���������֪��1.5y����2x+1.5y��=3��7
��֮�ã�x��y=1��1��
��ѡD��
���������
�����Ѷȣ�һ��
2��ѡ���� ��MgCl2��AlCl3��Ϊn mol�Ļ����Һ�������е�NaOH��Һ������������NaOH�����ʵ��������ɳ��������ʵ����Ĺ�ϵ��ȷ���ǣ����ӣ������ʣ�����pH���±���
����
| Mg2+
| Al 3+
| ����
| Al(OH)3
|
��ʼ����pH
| 8.93
| 3.56
| ��ʼ�ܽ�pH
| 8.04
|
��ȫ����pH
| 10.92
| 4.89
| ��ȫ�ܽ�pH
| 12.04
|
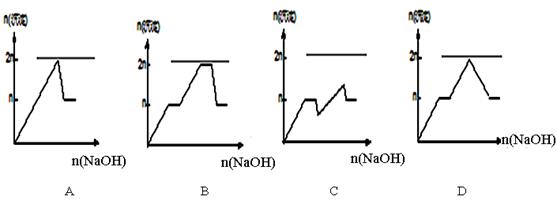
�ο��𰸣�C
�������������Mg2����Al3����ʼ����ʱ��pHֵ��֪����MgCl2��AlCl3�Ļ����Һ�е�NaOH��Һ����������������ʼ������������������ʼ�ܽ�ʱMg2����û�п�ʼ�γɳ�������pH��8.93ʱMg2����ʼ�γɳ�������pH��10.92ʱMg2����ȫ������ʱ����������û����ȫ�ܽ⡣��pH����12.04ʱ����������ȫ�ܽ⣬��˷��Ϸ�Ӧ���̵�ͼ��Ӧ����C����ѡC��
�����Ѷȣ�һ��
3��ѡ���� ���������ܸ�þ��Ӧ�������������ǣ�?��
A��������Һ
B������������Һ
C���Ȼ����Һ
D��̼������Һ
�ο��𰸣�AC
���������þ�ǻ��ý�����������ˮ��������Һ��Ӧ������������Ŀ�������ĸ�ѡ���У�Aѡ��Ϊ����Һ��Mg+2HCl====MgCl2+H2����Cѡ�����Ȼ��ˮ������ԣ������þ������Ӧ������������Ӧ�����ӷ���ʽΪMg+2 ====Mg2++2NH3��+H2����
====Mg2++2NH3��+H2����
�����Ѷȣ���
4��ѡ���� 14gͭ�����Ͻ���������ijŨ�ȵ����ᷴӦ�����ų���������1.12L����״���£�������ϣ�ͨ��ˮ��ǡ��ȫ�������գ���Ͻ���ͭ������Ϊ (? )
A��9.6g
B��6.4g
C��3.2g
D��1.6g
�ο��𰸣�C
���������n(O2) =" 1.12/22.4" =" 0.05mol" �� 0.05mol O2��Ӧ�õ�0.05��4 = 0.2mol����
��NO��NO2��O2��Ӧ��ʧȥ0.2mol���ӣ���Cu��Ag��HNO3��Ӧ��ʧȥ0.2mol���ӣ���ʧ�����غ㣩�������У�2��n(Cu) + n(Ag) = 0.2mol���������غ�ã��У�64��n(Cu) + 108��n(Ag) =" 14g" �����n(Cu) = 0.05mol����m(Cu) = 64��0.05 =" 3.2g" ��ѡC
����������������û�ѧ����ʽ����⣬������̽���ܸ��ӣ�������������غ����ʧ�����غ㣬����ܺõļ��㡣
�����Ѷȣ���
5��ѡ���� ��ȡ�������ۣ���һ�ݼ���������Ũ����������Һ���ڶ��ݼ���������ϡ���ᣬ��Ҫ�ų�����������壨��ͬ��ͬѹ�£���������������֮��Ϊ������ ?��
A��1:2
B��1:3
C��3:2
D��1:1
�ο��𰸣�D
����������������ἰǿ����Һ����������ԭ��Ӧ�ų���������Ӧ����������ԭ����������������������H+�������ˮ�У��õ��ӱ���ԭ���ɵģ�������������ԭ��Ӧ�еá�ʧ����������ȵ�ԭ�ɿ�����⡣
�������ᷴӦʱ����Al��Al3+������ŨNaOH��Ӧʱ��Al��AlO2-��ÿĦ����ʧȥ3Ħ���ӡ�����������������H+(�����ˮ��)�õ��ӱ���ԭ��2H++2e=H2��,����������ԭ��Ӧ�е�ʧ����������ȵ�ԭ��Ȼ�ų������������ȣ���ô��������Ӧ�����ĵ��������ʵ���һ����ȣ�������Ҳ��ȣ���ӦѡD��
�����Ѷȣ�һ��