1、选择题 常见镍氢电池的某极是储氢合金LaNi5H6(LaNi5H6中各元素化合价均为零),电池反应通常表示为:LaNi5H6+6NiO(OH)?

?LaNi5+6Ni(OH)2,下列说法正确的是( )
A.放电时储氢合金作正极
B.放电时负极反应:LaNi5H6+6OH--6e-=LaNi5+6H2O
C.充电时阳极周围c(OH-)增大
D.充电时储氢合金作阴极
参考答案:A.放电时,LaNi5H6中H元素被氧化,为电池的负极,故A错误;
B.放电时,LaNi5H6被氧化生成H2O,电极反应式为LaNi5H6+6OH--6e-=LaNi5+6H2O,故B正确;
C.充电时,阳极发生反应6Ni(OH)2+6OH-=6NiO(OH)+6e-+6H2O,c(OH-)减小,故C错误;
D.充电时,应发生LaNi5+6H2O+6e-=LaNi5H6+6OH-,储氢合金作阴极,故D正确.
故选BD.
本题解析:
本题难度:一般
2、选择题 蓄电池放电时是起原电池的作用,在充电时起电解池的作用。下式是爱迪生蓄电池分别在充电、放电时的反应: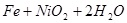 ?
?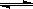 ?
?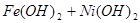 ,下列有关爱迪生电池的各种推断中错误的是(?)。
,下列有关爱迪生电池的各种推断中错误的是(?)。
A.放电时铁做负极,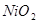 做正极
做正极
B.充电时阴极上的电极反应为: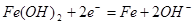
C.放电时,电解质溶液中的阴离子是向正极方向移动
D.蓄电池的两个电极必须浸入在碱性溶液中
参考答案:C
本题解析:根据电池总反应可知,放电时,Fe被氧化生成Fe(OH)2,电极反应式为Fe-2e-+2OH-=Fe(OH)2。正极NiO2得电子被还原生成Ni(OH)2,电极反应式为NiO2+2H2O+2e-=Ni(OH)2+2OH-。充电时电能转化为化学能,电极反应与原电池电极反应相反,以此解答该题。
放电时,Fe被氧化生成Fe(OH)2,为原电池的负极,NiO2是正极,故A正确;充电时阴极发生还原反应,Fe(OH)2被还原生成铁,电极反应为Fe(OH)2+2e-=Fe+2OH-,故B正确;放电时,电解质溶液中的阳离子是向正极方向移动,故C错误;该蓄电池在碱性条件下进行,电解质溶液应为碱性溶液,如用酸性电解质,则会破坏电池,故D正确,答案选C。
点评:该题是高考中的常见题型,属于中等难度的试题,试题贴近高考,有利于激发学生的学习兴趣。该题的关键是明确原电池和电解池的工作原理,然后结合题意灵活运用即可。答题注意根据电池总反应能正确书写电极反应式,为解答此类题目的关键,也是易错点。
本题难度:一般
3、选择题 有一种锂电池,它是用金属锂和石墨作电极材料,电解质溶液是由四氯化铝锂( LiAlCl4)溶解在亚硫酰氯 (SOCl2)中形成的,电池总反应方程式为:8Li+3SOCl2==6LiCl+Li2SO3 +2S。下列有关叙述中,正确的是
[? ]
A.金属锂做电池的正极,石墨做电池的负极
B.电池工作过程中,亚硫酰氯(SOCl2)被还原为Li2SO3
C.电解质溶液中混入水,对电池反应无影响
D.电池工作过程中,金属锂提供的电子与正极区析出硫的物质的量之比为4:1
参考答案:D
本题解析:
本题难度:一般
4、填空题 铅蓄电池是常用的化学电源,其电极材料分别是Pb和PbO2,电解液为硫酸。工作时该电池总反应式为
Pb+PbO2+2H2SO4==2PbSO4+2H2O。根据上述情况判断:
(1)蓄电池的负极材料是____。工作时,正极反应为____。
(2)工作时,电解质溶液的pH___(填“增大”、“减小”或“不变”)。
(3)工作时,电解质溶液中的阴离子移向____极。电流方向从____极流向____极。
参考答案:(1)Pb; PbO2+2e-+4H++SO42- == PbSO4+2H2O
(2)增大
(3)负; 正; 负
本题解析:
本题难度:一般
5、填空题 (1)在原电池中,较活泼的金属极上发生______,是______极;较不活泼的金属上发生______,是______极.
(2)氢氧燃料电池是符合绿色化学理念的新型发电装置.如图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定.请回答:
①氢氧燃料电池中能量转化主要形式是______;
②负极反应式为______.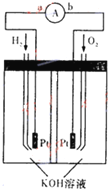
参考答案:(1)原电池中活泼金属做负极,失电子发生氧化反应,较不活泼的金属做阴极,得到电子发生还原反应;故答案为:氧化反应;负极;还原反应;正极;
(2)①氢氧燃料电池是原电池,实现了化学能转化为电能;
②负极上是氢气失去电子发生氧化反应,电解质溶液是氢氧化钾,所以电极反应为:H2+2OH-+2e-=2H2O;
故答案为:H2+2OH-+2e-=2H2O.
本题解析:
本题难度:一般