1、选择题 下列说法正确的是(?)
A.钾的密度比水小,能像钠一样浮在水面上
B.锂的密度比煤油大,能像钠一样保存在煤油中
C.钠、钾常温下都是固体,钠钾合金也是固体
D.同钠一样,铯也柔软,可用手按在玻璃片上,用小刀切割
参考答案:A
本题解析:Li、Na、K的密度都比水的密度小,Li、K的密度比Na的还小,A选项正确。
碱金属元素中,Li的密度最小。将Li放入煤油中,Li会浮在液面上,煤油起不到隔绝空气的作用――不能将Li放在煤油中保存。B选项错误。
碱金属常温下都是固体,Na、K也是,但Na―K合金是液态。C不正确。
同钠一样,碱金属腐蚀性很强,不可直接用手拿放。D选项不正确。
本题难度:简单
2、实验题 实验目的:探究过氧化钠与水反应后的溶液滴加酚酞试液先变红后退色的原因。
[分析与猜想]
(1)根据过氧化钠与水反应的原理:2Na2O2 + 2H2O =" 4NaOH" + O2↑,往过氧化钠固体完全溶解反应后的溶液中滴加酚酞本应只会变红而不会退色,而实验中发现酚酞变红后又退色。由此提出如下的猜想:
A.氧气有漂白性
B.氢氧化钠有漂白性
C.?
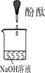
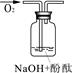
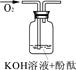
[实验与判断] 请完成下列表格:
实验编号
| 1
| 2
| 3
|
实验装置
| 
| 
| 
|
验证猜想
| ??
| ? C?
| ??
|
实验现象
| 溶液变红后不退色
|
实验说明
| 1、2的实验中NaOH溶液是用?(填“氢氧化钠固体”、“氧化钠固体”、“过氧化钠固体”)溶于水配制的。
|
?
(2)根据以上实验分析发现:过氧化钠与水反应过程中,钠元素形成了稳定的化合物,溶液中还生成了一种不很稳定、具有漂白性的物质X,X的化学式是?。
(3)可用右图装置对溶液中不很稳定的物质进行探究,在①处装入的物质是?(填选项,下同),②处装入的物质是?。
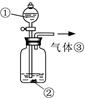
A.酚酞试剂? B.过氧化钠与水反应后的溶液
C.二氧化锰? D.氢氧化钠固体配制的溶液
(4)气体③是?,过氧化钠与水反应的化学方程式没有写出X来,原因是?。
参考答案:(1)氧气和氢氧化钠共同作用具有漂白性? B? A?氢氧化钠固体(各1分共3分)
(2)H2O2
(3)B C (各1分)
(4)O2(1分)? H2O2不稳定,已分解
本题解析:(1)结合A、B,C的猜想是氧气和氢氧化钠共同作用具有漂白性,所以实验1对应的是B,实验3对应的是A;氢氧化钠溶液是用氢氧化钠固体配制的,因为氧化钠固体空气中易变质,造成所配溶液?不纯,过氧化钠固体与水作用除生成氢氧化钠外还会有氧气生成,给实验带来干扰
(2)钠元素形成了稳定的化合物即氢氧化钠,另一种不很稳定、具有漂白性的物质X应是过氧化氢,?其化学式为H2O2
(3)过氧化氢在二氧化锰作催化剂的条件下分解产生氧气,氧气 可用带火星的木条检验,所以①处装
入的物质过氧化钠与水反应后的溶液,选B,②处装入的物质是二氧化锰,选C。
(4)气体③是氧气,因为过氧化氢不稳定,分解产生氧气,所以在书写过氧化钠与水的反应方程式时不写出
本题难度:一般
3、选择题 测定Na2CO3和NaHCO3混合物中Na2CO3质量分数的实验方案不合理的是(? )
A.取a克混合物充分加热,减重b克
B.取a克混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得b克固体
C.取a克混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,增重b克
D.取a克混合物与足量Ba(OH)2溶液充分反应,过滤、洗涤、烘干,得b克固体
参考答案:C
本题解析:A选项,NaHCO3受热易分解生成碳酸钠、水和二氧化碳,所以通过加热分解利用差量法即可计算出Na2CO3质量分数,故A不选;B选项,Na2CO3和NaHCO3均可与盐酸反应生成水、二氧化碳和氯化钠,所以bg固体是氯化钠,利用守恒法可计算出Na2CO3质量分数,故B不选;C选项,混合物与足量稀硫酸充分反应,也会生成水和二氧化碳,所以逸出的气体是二氧化碳,但会混有水蒸气,即碱石灰增加的质量不是二氧化碳的质量,不能测定含量,故C选;D选项,Na2CO3和NaHCO3都与Ba(OH)2反应,反应的方程式为CO32-+Ba2+=BaCO3↓、HCO3-+OH-+Ba2+=H2O+BaCO3↓,因此最后得到的固体是BaCO3,所以可以计算出Na2CO3质量分数,故D不选。
本题难度:一般
4、选择题 某溶液中含有①NO3- ②HCO3- ③SO32- ④CO32- ⑤SO42-等五种阴离子.?向其中加入少量的Na2O2固体后,溶液中离子浓度基本保持不变的是(假设溶液体积无变化)
[? ]
A.①?
B.①②④
C.①③⑤?
D.①③④⑤
参考答案:A
本题解析:
本题难度:一般
5、选择题 已知锂和镁的单质及其化合物在很多性质上具有相似性,由此可以推断下列关于锂及其化合物的叙述中,正确的是
A.LiOH加热时,不会分解
B.Li2CO3加热时,不会分解
C.Li在氧气中燃烧生成Li2O2
D.Li 与稀硫酸反应生成Li2SO4
与稀硫酸反应生成Li2SO4
参考答案:D
本题解析:略
本题难度:一般