| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学试题《离子方程式的书写及正误判断》考点预测(2017年强化版)(十)
参考答案:D 本题解析:A、次氯酸为弱酸,不能拆开,错误;B、氢离子、氢氧根离子反应有水分子生成,错误;C、电荷不守恒,错误;D、用氢氧化钠检验氯化铵溶液中的铵根离子,离子反应为NH4++OH- 本题难度:一般 2、选择题 下列离子方程式正确的是 |
参考答案:B
本题解析:A、磁性氧化铁溶于稀硝酸中发生氧化还原反应,即3Fe3O4+28H++NO3-=9Fe3++NO↑+14H2O,A错误;B、NaHSO4溶液与Ba(OH)2溶液反应至中性的离子方程式为2H++SO42-+Ba2++2OH- = BaSO4↓+2H2O,B正确;C、用石墨电极电解氯化镁溶液:2Cl-+Mg2++2H2O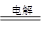 Cl2↑+H2↑+Mg(OH)2↓,C错误;D、铅蓄电池放电时的负极铅失去电子,发生氧化反应:Pb+SO42--2e-=PbSO4,D错误,答案选B。
Cl2↑+H2↑+Mg(OH)2↓,C错误;D、铅蓄电池放电时的负极铅失去电子,发生氧化反应:Pb+SO42--2e-=PbSO4,D错误,答案选B。
考点:考查离子方程式的正误判断
本题难度:一般
3、选择题 能正确表示下列化学反应的离子方程式的是
A.氢氧化钡溶液与盐酸的反应 2OH-+2H+= 2H2O
B.澄清的石灰水与稀盐酸反应 Ca(OH)2 + 2H+= Ca2+ + 2H2O
C.铜片插入硝酸银溶液中 Cu + Ag+= Cu2+ + Ag
D.碳酸钙溶于稀盐酸中 CaCO3+2H+=Ca2++H2O+CO2
参考答案:D
本题解析:A错,离子方程式是化学计量数也应为最简整数比;B错,澄清石灰水要拆成离子形式;C错,电荷未守恒;D正确;
本题难度:一般
4、填空题 (6*1分)某溶液中含有SO42-、CO32-、Cl-三种阴离子。如果每次只检验一种离子,要↑
(1)先检验CO32-,加入 试剂(或溶液),反应的离子方程式为 ;
(2)然后检验SO42,加入 试剂(或溶液),反应的离子方程式为 ;
(3)最后检验Cl-,加入 试剂(或溶液),反应的离子方程式为 。
参考答案:见解析。
本题解析:试题分析:.因为要求每次只检验其中一种离子,应注意试剂添加顺序。(1)先检验CO32-,加入稀硝酸,反应的离子方程式为2H++CO32-=CO2↑+H2O;(2)然后检验SO42,加入Ba(NO3)2溶液,反应的离子方程式为Ba2++SO42-=BaO4↓;(3)最后检验Cl-,加入AgNO3溶液,反应的离子方程式为Ag++Cl-=AgCl↓;
考点:了解离子反应的概念、离子反应发生的条件。了解常见离子的检验方法。
点评:本题考查常见离子的检验,当溶液中存在多个离子需要检验时,就注意离子间的相互干扰,检验试剂的添加要有一定顺序。
本题难度:一般
5、选择题 下列离子方程式书写正确的是( )
A 铜与盐酸反应:Cu +2H+ Cu2+ + H2↑
B 硫酸与氯化钡溶液反应:Ba2+ + SO42- BaSO4↓
C 金属钠与水反应:2Na + 2H+ 2Na+ + H2↑
D 氯化亚铁与氯水反应:Fe2+ + Cl2 Fe3++2Cl-
参考答案:B
本题解析:在金属活动顺序表中铜排在氢的后面,不能置换酸中的氢,A不正确。C中水应该用化学式不是,正确的是2Na+2H2O=2Na++2OH-+H2↑。D中没有配平,正确的是2Fe2+ + Cl2 2Fe3++2Cl-,所以答案是B。
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高中化学知识点讲解《物质的量》.. | |