|
高中化学知识点归纳《化学反应速率》高频考点强化练习(2017年最新版)(二)
2017-11-11 01:30:33
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
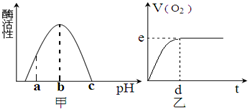
1、选择题 为研究H2O2酶对反应2H2O2=2H2O+O2↑的影响,通过实验可得到如下两个曲线.图甲是室温下H2O2酶的活性受pH影响的曲线,图乙表示在最合适温度及pH=b条件下H2O2分解产生的O2的体积随时间的变化.若反应过程中改变某一初始条件(其他条件不变),以下叙述正确的是( )
A.温度升至100℃,e点不移,d点右移
B.H2O2用量增加时,e点不移,d点左移
C.pH=c时,e点为0
D.pH=a时,e点下移,d点左移
| 
参考答案:A、温度升至100℃酶基本失去活性,H2O2分解速率减慢,但整个过程产生的O2的体积恒定,即e点不移,d点右移,故A正确;
B、双氧水用量增加则分解产生的氧气的量也会增加,所以e点上移,d点右移,故B错误;
C、当pH=c时,酶的催化活性为0,即不起催化作用,反应速率减慢,但是e点绝不为0,故C错误;
D、当pH=a时酶的催化活性不如pH=b时的催化活性高,即pH=a时分解速率较慢,但是不影响生成氧气的体积,所以e点不动,d点右移,故D错误.
故选A.
本题解析:
本题难度:简单
2、选择题 在10L容器中进行如下反应:N2+ 3H2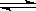 ?2NH3,3秒钟后, H2的物质的量减少了0.18mol,用H2的物质的量浓度的变化表示3秒钟内的平均反应速率为(?) ?2NH3,3秒钟后, H2的物质的量减少了0.18mol,用H2的物质的量浓度的变化表示3秒钟内的平均反应速率为(?)
A.0.006mol/(L・s)
B.0.004mol/(L・s)
C.0.003mol/(L・s)
D.0.009 mol/(L・s)
参考答案:A
本题解析:反应速率通常用单位时间内浓度的变化量来表示,3s内氢气的浓度减少了
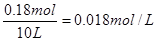 ,所以用氢气表示的反应速率为 ,所以用氢气表示的反应速率为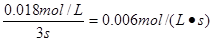 ,因此答案选A。 ,因此答案选A。
本题难度:一般
3、填空题 (10分)运用甲烷自热来制取氢气是目前较为先进的技术。其涉及的反应如下:
①CH4(g)+2H2O(g)=CO2(g)+4H2(g) △H1=+165.0 kJ/mol 反应活化能Ea1="243.9" kJ/mol
②CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H2=-802.6 kJ/mol 反应活化能Ea2="125.6" kJ/mol
(1)2H2(g) + O2(g)= 2H2O(g)△H3= kJ/mol;
(2)下面能正确表示氢气和氧气反应生成水的能量变化示意图的是 (填字母序号)。
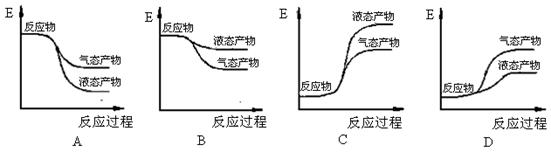
(3)运用甲烷自热来制取氢气是目前较为先进的技术。在同一反应系统同时通入甲烷、氧气和水蒸气,发生如上反应①和反应②,则反应开始时,反应①的反应速率 反应②的反应速率(填“>”、“<”或“=”),理由是 ;从能量角度分析,在该制氢过程中通入适量氧气发生反应②的目的是 ;
参考答案:(1)-483.8 (2分); (2)A (2分)
(3)<(2分);反应①的活化能比反应②的活化能高;(2分)
甲烷与氧气反应放热,为反应①提供所需能量(2分)
本题解析:(1)由盖斯定律可知:2H2(g) + O2(g)= 2H2O(g)△H3=-1/2△H1+1/2△H2="-483.8" kJ/mol;(2)氢气和氧气反应生成水为放热反应,故反应物总能量大于生成物总能量,且气态水变液态水为放热过程,故A项正确;由题干可知反应①的活化能比反应②的活化能高,故反应①的反应速率<反应②的反应速率;反应①为吸热,反应②为放热,故从能量角度分析,在该制氢过程中通入适量氧气发生反应②的目的是甲烷与氧气反应放热,为反应①提供所需能量。
考点:化学反应能量变化。
本题难度:困难
4、选择题 可逆反应:X(g)+3 Y(g) 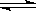 2 R(g)+2W(g)在4种不同情况下的反应速率分别如下,其中表示该反应速率最快的是(?) 2 R(g)+2W(g)在4种不同情况下的反应速率分别如下,其中表示该反应速率最快的是(?)
A.v(X) = 0.15 mol・(L・S)-1
B.v(Y) = 0.60 mol・(L・S)-1
C.v(R) = 8.0 mol・(L・min)-1
D.v(W) = 0.45 mol・(L・S)-1
参考答案:D
本题解析:在比较化学反应速率时,应该先统一单位,再以同一种物质为标准比较。此题若就以反应物X作为标准,根据反应速率与方程式系数的关系,B选项所描述的Y的速率转换成X,有V(x)=0.2mol・(L・S)-1.C选项V(x)=0.133mol・(L・S)-1.D选项V(x)=0.225mol・(L・S)-1.所以反应最快的是D.
本题难度:简单
5、选择题 把0.6 mol X气体和0.4 mol Y气体混合于容积为2 L的容器中,使其发生如下反应:3X(g)+Y(g) nZ(g)+2W(g)。5 min末生成0.2 mol W,若测知以Z浓度变化表示的平均反应速率为0.01 mol・(L・min)-1,则n的值为(?) nZ(g)+2W(g)。5 min末生成0.2 mol W,若测知以Z浓度变化表示的平均反应速率为0.01 mol・(L・min)-1,则n的值为(?)
A.4
B.3
C.2
D.1
参考答案:D
本题解析:以Z浓度变化表示的平均反应速率为0.01 mol・(L・min)-1,则5 min末生成Z的物质的量是0.01 mol・(L・min)-1×2L×5min=0.1mol。则根据变化量之比是相应的化学计量数之比可知,n=1,答案选D。
点评:该题是基础性试题的考查,侧重对学生基础知识的巩固和检验,难度不大。该题的关键是明确反应速率和化学计量数的关系,然后结合题意灵活运用即可。
本题难度:简单
| 