1、填空题 如图是一些重要工业生产的转化关系(反应条件略去):
请完成下列问题:
(1)若D是单质,且与A属于同一主族,则.
①反应的化学方程式是______.
②D的原子结构示意图是______.
③D单质的一种重要用途是______.
(2)若B为黄色固体,D为固体化合物,则
①该反应的化学方程式是______.
②生产该工业品的工厂应建在离______较近的地方.
③实验室检验C的方法是______.
(3)若B是一种有刺激性气味的气体,则
①B的分子形状是______.
②实验室进行此实验时,常看到有大量白烟产生,请说明产生大量白烟的原因______.
③化合物C在一定体积的容器中,在一定条件下发生反应,测得容器内气体的压强略小于原来的
,请写出该反应的化学方程式______.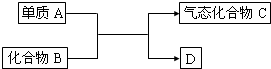
参考答案:(1)D与A同主族,A能置换出D,且该反应是重要反应,则分析元素周期表,可知A是C,D是Si,即2C+SiO2?高温?.?2CO+Si.Si的原子结构示意图是
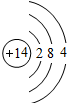
,硅单质的一种重要用途是制半导体材料,故答案为:2C+SiO2?高温?.?2CO+Si;

;制半导体材料;
(2)①化合物B为黄色固体,中学阶段的黄色固体化合物有AgI、硫铁矿等,能用于工业生产的只能是用黄铁矿生成浓硫酸,即A是氧气,B是FeS2,C是SO2,因此化学方程式为4FeS2+11O2?高温?.?2Fe2O3+SO2,故答案为:4FeS2+11O2?高温?.?2Fe2O3+SO2↑;
②该反应用于工业生产硫酸,由于浓硫酸是腐蚀品,运输成本较高,且危险性大,因此建厂时应该选择在使用浓硫酸密集的地方,即工业区集中的消费中心,故答案为:消费中心;
③因为氯气和二氧化硫都能使品红试液褪色,所以利用二者化学性质的差别,实验室检验二氧化硫通常采用:将气体C通入品红溶液中,溶液褪色,将溶液加热,又恢复红色,
故答案为:将气体C通入品红溶液中,溶液褪色,将溶液加热,又恢复红色;
(3)①该反应为工业生产的转化关系,又实验室做该实验有白烟,结合中学阶段氨气与挥发性酸相遇会产生白烟的知识,可知该反应是工业上氨气催化氧化制取硝酸的反应,即
4NH3+5O2催化剂.△4NO+6H2O,因此B是NH3,C是NO.氨气分子是三角锥形,故答案为:三角锥形;
②实验室进行此反应,NO会被过量氧气氧化为NO2,进而与水反应生成硝酸,硝酸与氨气反应生成硝酸铵而产生大量白烟,即:生成的NO气体被氧气氧化生成NO2,NO2与水反应生成的硝酸与NH3反应而产生大量白烟,故答案为:生成的NO气体被氧气氧化生成NO2,NO2与水反应生成的硝酸与NH3反应而产生大量白烟;
③NO在密闭容器中一定条件下可以分解为二氧化氮和一氧化二氮,发生的反应为3NO=NO2+N2O,由于存在2NO2?N2O4而容器内气体的压强略小于原来的23.
故答案为:3NO=NO2+N2O.
本题解析:
本题难度:一般
2、推断题 X、Y、Z、W为含有相同电子数的分子或离子,均由原子序数小于10的元素组成,X有5个原子核。通常状况下,W为无色液体。
已知:X+Y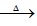 Z+W
Z+W
(1)Y的电子式是_________________________。
(2)液态Z和W的电离相似,都可电离出电子数相同的两种离子,液态Z的电离方程式是_________________________________。
(3)用图示装置制备NO并验证其还原性。有下列主要操作:

a.向广口瓶内注入足量热NaOH溶液,将盛有铜片的小烧杯放入瓶中。
b.关闭止水夹,点燃红磷,伸入瓶中,塞好胶塞。
c.待红磷充分燃烧,一段时间后打开分液漏斗旋塞,向烧杯中滴入少量稀硝酸。
①步骤c后还缺少的一步主要操作是__________________________。
②红磷充分燃烧的产物与NaOH溶液反应的离子方程式是__________________。
③步骤c滴入稀硝酸后烧杯中的现象是________________________。反应的离子方程式是__________________。
(4)一定温度下,将1 mol N2O4置于密闭容器中,保持压强不变,升高温度至T1的过程中,气体由无色逐渐变为红棕色。温度由T1继续升高到T2的过程中,气体逐渐变为无色。若保持T2,增大压强,气体逐渐变为红棕色。气体的物质的量n随温度T变化的关系如图所示。
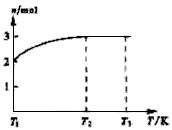
①温度在T1-T2之间,反应的化学方程式是_________________________。
②温度在T2-T3之间,气体的平均相对分子质量是(保留1位小数)______________。
参考答案:(1)
(2)2NH3(l)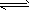 NH2-+NH4+
NH2-+NH4+
(3) ①打开止水夹,通入少量氧气;②P2O5+6OH-=2PO43-+3H2O;③Cu片逐渐溶解,有无色气泡产生,溶液由无色变为蓝色;3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
(4) ①2NO2 N2O4;②30.7
N2O4;②30.7
本题解析:
本题难度:一般
3、填空题 (8分)下图中A~J均代表无机物或其水溶液,其中B、D、G是单质,B是地壳中含量最高的金属元素,G是气体,D是应用最广泛的金属。根据图示回答问题:
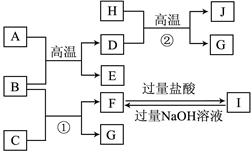
(1)反应②的化学方程式是?;
(2)J与氢碘酸反应的离子方程式是?;
(3)要使溶液F中的一种金属元素全部以沉淀的形式析出,最适宜加入的反应物是?(填化学式);I→F的离子方程式为?。
参考答案:(1)3Fe + 4H2O(g)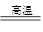 ?Fe3O4 + 4H2
?Fe3O4 + 4H2
(2)Fe3O4 +2I-+8H+ === 3Fe2+ + I2 + 4H2O
(3)CO2 ?Al3+ + 4OH-=== AlO2-+ 2H2O
本题解析:由题目所给信息可直接判定B为铝,它与A发生铝热反应得到应用最广泛的金属D为铁,同时得到E为氧化铝;
依据铁的性质可知在高温下它可和水蒸气反应生成J为Fe3O4 和G氢气;
铝与C置换出氢气G,同时得到F为偏铝酸盐,它与I之间可以通过加酸或加碱转化。
本题难度:一般
4、简答题 (13分) 化合物A相对分子质量为86,碳的质量分数为55.8%,氢为7.0%,其余为氧。A的相关反应如下图所示:
化合物A相对分子质量为86,碳的质量分数为55.8%,氢为7.0%,其余为氧。A的相关反应如下图所示:

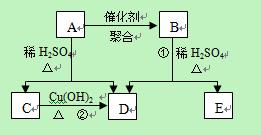

 已知R-CH=CHOH(烯醇)不稳定,很快转化为R-CH2CHO。
已知R-CH=CHOH(烯醇)不稳定,很快转化为R-CH2CHO。

 根据以上信息回答下列问题:
根据以上信息回答下列问题:

 (1)A的分子式为?;
(1)A的分子式为?;
 (2)反应②的化学方程式是?;
(2)反应②的化学方程式是?;

 (3)A的结构简式是?
(3)A的结构简式是?
 ;(4)反应①的化学方程式是?;
;(4)反应①的化学方程式是?;

 (5)A的另一种同分异构体,其分子中所有碳原子在一条直线上,它的结构简式为?。
(5)A的另一种同分异构体,其分子中所有碳原子在一条直线上,它的结构简式为?。
参考答案:(13分)

 (1)C4H6O2?(2分)
(1)C4H6O2?(2分)

 (2)CH3CHO+2Cu(OH)2
(2)CH3CHO+2Cu(OH)2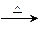 CH3COOH+Cu2O↓+2H2O?(3分)
CH3COOH+Cu2O↓+2H2O?(3分)

 (3)
(3)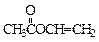 ?(2分)
?(2分)

(4)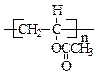 +nH2O
+nH2O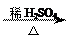
 + nCH3COOH?(3分)
+ nCH3COOH?(3分)

 (5)
(5)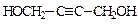 ? (其他合理答案也给分)?(3分)
? (其他合理答案也给分)?(3分)
本题解析:略
本题难度:一般
5、推断题 A、B、C、D四种化合物,其中A、C、D焰色反应均为黄色,而B的焰色反应为紫色,A、C和盐酸反应均得到D,将固体C加热可得到A,若在A的溶液中通入一种无色无味气体,又可制得C,若B的溶液滴加到硫酸亚铁溶液会先后出现白色沉淀→灰绿色沉淀→红褐色沉淀E。试推断 A:________、B:________、C:_________、D:_________、E:_________
参考答案:A:Na2CO3;B:KOH;C:NaHCO3;D:NaCl;E:Fe(OH)3
本题解析:
本题难度:一般