1、填空题 A、B、C、D、E各物质的转化关系如图所示.
(1)当A为空气中含量最高的单质气体时,A是______(写化学式).
写出下列反应的化学方程式,并回答有关问题:
①E→C:______;
②实验室制备B:______.能不能用浓硫酸做B的干燥剂?______(填“能”或“不能”).
(2)当A为淡黄色固体单质时,A是______(写化学式).写出下列反应的化学方程式:
①C→D:______;
②E与木炭反应:______.
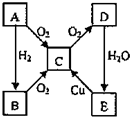
参考答案:(1)当A为空气中含量最高的单质气体时,应为N2,则C为NO,B为NH3,D为NO2,E为HNO3,故答案为:N2;
①E→C的反应为稀硝酸与Cu的反应,反应的方程式为3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O,故答案为:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O;
②实验室应氯化铵与氢氧化钙在加热条件下反应制备氨气,反应的化学方程式为2NH4Cl+Ca(OH)2 △.CaCl2+2NH3↑+2H2O,氨气是碱性气体,不能与浓硫酸做干燥剂,
故答案为:2NH4Cl+Ca(OH)2 △.CaCl2+2NH3↑+2H2O;不能;
(2)当A为淡黄色固体单质时,A是S,B是H2S,C是SO2,D是SO3,E是H2SO4,故答案为:S;
①C→D的反应为SO2在催化剂条件下反应生成SO3,反应的方程式为2SO2+O2催化剂
本题解析:
本题难度:简单
2、实验题 (13分)已知X为中学化学中一种常见的盐,F为淡黄色固体;M、N为常见的金属,N的氧化物可作耐火材料,可用它来制造耐火坩埚和耐高温试验仪器;H为气体单质,D为无色气体,D在空气中会出现红棕色。各物质的转化关系如下图(部分反应物已略去)。
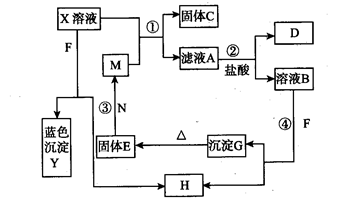
请回答下列问题:
(1)E的化学式为_______________(2分)。
(2)将M丝插入盛有X溶液的试管中,反应一段时间后的现象是_______________(2分)。
(3)在反应①②③④中属于置换反应的是__________(填序号)(2分)。
(4)反应②的离子方程式为______________________________________________(2分)。
(5)用石墨作电极电解50mL X溶液,观察到A电极表面有红色的固态物质生成,B电极有无色气体生成;电解一段时间后,取出A电极,洗涤、干燥、称量,电极增重1.6g。请回答下列问题:
①写出电解时的阳极反应式________________________________________(2分)。
②电解后溶液的pH为_______________________________(3分)(假设电解前后溶液体积不变)。
参考答案:(1)Fe2O3(2分)? (2)铁丝上附有红色物质,溶液颜色变浅(2分)
(3)(1)(3)(2分)? (4)2Fe2++NO3-+4H+=3Fe3++NO↑+2H2O(2分)
(5)①4OH--4e-=O2+2H2O(2分)?②0(3分)
本题解析:F为淡黄色固体,可能为硫或Na2O2,它可与溶液B或溶液X均产生无色气体H及沉淀Y(蓝色沉淀必定为Cu(OH)2)或G,可判定F为Na2O2,H为氧气,X为铜盐;
由“N的氧化物可作耐火材料,可用它来制造耐火坩埚和耐高温试验仪器”知道N必为铝,不溶于水的氢氧化物G加热脱水生成氧化物E,E与铝可生成另一常见金属M,可知这属于铝热反应,铝与氧化物E:Fe2O3置换出M:铁单质:③2Al+Fe2O3 Al2O3+2Fe
Al2O3+2Fe
铁与铜盐M发生置换出C:铜和滤液A:亚铁盐溶液,加入盐酸后生成NO(D为无色气体,D在空气中会出现红棕色,说明D一定为NO,在空气中被氧化为红棕色的NO2),说明A必定为硝酸盐:②2Fe2++NO3-+4H+=3Fe3++NO↑+2H2O,从而可知X为硝酸铜,A为硝酸亚铁,B为硝酸铁溶液;
(1)Fe2O3
(2)铁与硝酸铜发生置换反应:①Fe+CuSO4=FeSO4+Cu,故铁丝上附有红色物质,溶液颜色由蓝色转变了浅绿色
(3)反应④:2Na2O2+2H2O=4NaOH+O2↑? FeCl3+3NaOH=Fe(OH)3↓+3NaCl,①②③④属于置换反应的是①③
(4)2Fe2++NO3-+4H+=3Fe3++NO↑+2H2O
(5)总电解反应式为:2Cu(NO3)2+2H2O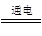 2Cu+O2↑+4HNO3
2Cu+O2↑+4HNO3
①阳极上有氧气生成:4OH--4e-=O2↑+2H2O
②由总反应式可知,铜为1.6g,同时得到n(HNO3)=0.05mol,c(HNO3)=0.05mol/0.05L=1mol/L
c(H+)=1mol/L,pH=0
本题难度:一般
3、填空题 A、B、C、D、E、F六种物质的转化关系如图所示(反应条件和部分产物未标出).
(1)若A为短周期金属单质,D为短周期非金属单质(一种黑色固体),且所含元素的原子序数A是D的2倍,原子的最外层电子数D是A的2倍,化合物F的浓溶液与单质A、D在一定条件下反应都有红棕色气体生成,则A在周期表中的位置为:______,B的电子式为:______,F的浓溶液与D在加热条件下反应的化学方程式为:______.
(2)若A是常见变价金属的单质,D、F是气态单质,且反应①②均在水溶液中进行.则反应②的离子方程式是______.
(3)若A、D、F都是短周期非金属元素单质,且?A、D所含元素同主族,A、F所含元素同周期,B是制作光导纤维的基本原料,则B是______,C是______,F是______.(填化学式)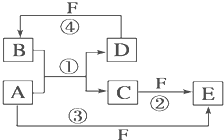
参考答案:(1)D为短周期非金属单质(一种黑色固体)可以推断为C,且所含元素的原子序数A是D的2倍,原子的最外层电子数D是A的2倍,则A为Mg,B为CO2,C为MgO,E为硝酸镁;化合物F的浓溶液与单质A、D在一定条件下反应都有红棕色气体生成,说明生成二氧化氮气体,则浓溶液F为浓硝酸;A在周期表中的位置:第三周期,ⅡA族;二氧化碳的电子式为::O::C::O:;F的浓溶液与D在加热条件下反应的化学方程式:C+4HNO3?加热?.?CO2↑+4NO2↑+2H2O,
故答案为:第三周期,ⅡA族;::O::C::O:;C+4HNO3?加热?.?CO2↑+4NO2↑+2H2O;
(2)若A是常见变价金属的单质,D、F是气态单质,反应①②均在水溶液中进行.说明A+B→C+D是置换反应,推断A为Fe,B为盐酸,D为氢气,C为氯化亚铁,F为Cl2;反应②的离子方程式是氯化亚铁和氯气发生的氧化还原反应,离子方程式为:2Fe2++Cl2=2Fe3++2Cl-;故答案为:2Fe2++Cl2=2Fe3++2Cl-;
(3)若A、D、F都是短周期非金属元素单质,且 A、D所含元素同主族,A、F所含元素同周期,B是制作光导纤维的基本原料,推断,B为SiO2,A为C,D为Si,C为CO,
E为CO2,F为O2;
故答案为:B、SiO2;C、CO;F、O2
本题解析:
本题难度:简单
4、推断题 已知B是常见的金属单质,E为常见的气态非金属单质,H常温下为无色液体,C的浓溶液在加热时才与D反应。根据下列框图所示,试回答:
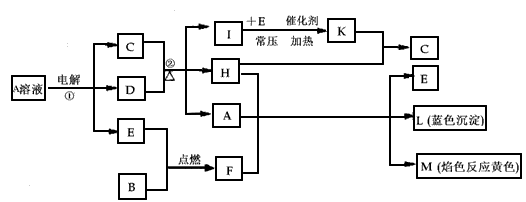
(1)F的电子式为________,所含化学键为____________;
(2)反应①的离子方程式为_________________;
(3)每生成1 mol K,反应放出98.3 kJ的热量,该反应的热化学方程式为________________;
(4)反应②的化学方程式为__________________;
(5)化合物F与Na2S溶液反应,生成NaOH和S单质,试写出该反应的离子方程式为_________________。
参考答案:(1)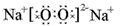 ; 离子键,非极性共价键;
; 离子键,非极性共价键;
(2)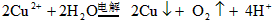 ;
;
(3)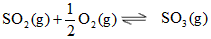 ;
;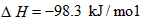 ;
;
(4)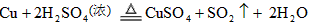 ;
;
(5)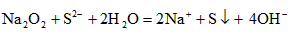 。
。
本题解析:
本题难度:一般
5、选择题 有A、B、C、D、E、F六瓶不同物质的溶液,它们各是NH3?H2O、Na2CO3、MgSO4、NaHCO3、HNO3和BaCl2溶液中的一种.为了鉴别它们,各取少量溶液进行两两混合,实验结果如右表所示.表中“↓”表示生成微溶物或沉淀,“↑”表示生成气体,“-”表示观察不到明显现象,空格表示实验未做.试推断其中F是( ? )
A.Na2CO3溶液
B.BaCl2溶液
C.MgSO4溶液
D.NaHCO3溶液
