1、简答题 已知A、B均是由两种短周期元素组成的化合物,A中某元素的质量分数为75%,C、J是同周期元素的气态氢化物,X为无色液体,D具有两性.反应生成的水均已略去.它们有如下图所示的关系.
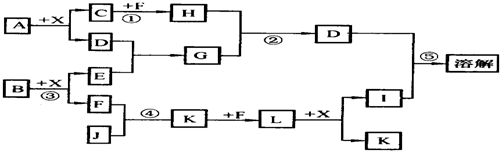
(1)写出化学式:A.______,B.______,C.______.
(2)反应③中每生成lmolF,转移电子的数目为:______.
(3)反应④的化学方程式为:______.
(4)写出离子方程式分别为:反应②______;
反应⑤______.
(5)反应①中,每1.00g?C与足量的F作用,恢复到25℃放出55.6kJ热量,写出反应①的热化学方程式.______.
参考答案:1.X为无色液体,推断X为H2O;
2.D具有两性,可知D为Al2O3或Al(OH)3,而Al2O3要经过氢氧化铝脱水或铝直接与氧气化合而得,图中显然不具备这样的条件,因此D为Al(OH)3,D由A反应而来,A中含铝元素;
3.因为D遇I溶解,可知I为强酸或强碱,但I由J一路反应而来,又有J为第二周期元素的气态氢化物,因此J为非金属氢化物,I为强酸,而L+X生成I+K,只有硝酸的生成(3NO2+H2O=2HNO3+NO)符合这一模式,L为NO2,K为NO,由NO+F到NO2,F为O2.顺便也可知J中含氮元素,J为NH3;
4.因为C也为第二周期元素的气态氢化物,而第二周期元素的气态氢化物一般只研究碳与氮元素的氢化物(若C为HF,则A为AlF3,不合题意;而硼的性质一般不做研究,否则要给提示或条件),J为NH3,所以C为烃类,A为碳与铝的化合物,结合给出的质量分数,A为Al4C3,它与水发生水解反应时,碳元素的价态不变,因此产物C为甲烷(CH4),它与F(氧气)反应除水之外的产物H为CO2.A+X=C+D反应方程式:Al4C3+12H2O→4Al(OH)3+3CH4↑;
5.因为H与G反应生成D(Al(OH)3),G由D反应来,因此G为偏铝酸盐,E为强碱,因为E由短周期元素化合物B与水反应来,所以E为NaOH,G为NaAlO2,因为B+水生成NaOH+O2,所以B为Na2O2.综上所述判断出的各物质为:A为Al4C3 ;B为Na2O2;C为CH4;D为Al(OH)3;E为NaOH;F为O2;G为NaAlO2;H为CO2;I为HNO3;为NH3;K为NO;LNO2;X为H2O;
(1)依据分析推断得到A、B、C分别为:Al4C3、Na2O2、CH4,故答案为:Al4C3;Na2O2;CH4;
(2)反应③为2Na2O2+2H2O=4NaOH+O2;反应中过氧化钠自身氧化还原反应,氧元素化合价从-1价变化为0价,-2价,反应中每生成lmolF(O2)转移电子物质的量为2mol,转移电子数为1.204×1024,故答案为:1.204×1024;
(3)反应④是氨气的催化氧化反应,反应的化学方程式为:4NH3+5O2催化剂.△4NO+6H2O,故答案为:4NH3+5O2催化剂.△4NO+6H2O;
(4)反应②是二氧化碳气体通入偏铝酸钠溶液中发生的反应,反应的离子方程式为:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-或AlO2-+CO2+2H2O=2Al(OH)3↓+HCO3-;反应⑤是氢氧化铝在硝酸中溶解的反应,反应的离子方程式为:Al(OH)3+3H+=Al3++3H2O,
故答案为:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-或AlO2-+CO2+2H2O=2Al(OH)3↓+HCO3-;Al(OH)3+3H+=Al3++3H2O;
(5)反应①是甲烷燃烧生成二氧化碳和水的反应,每1.00g?CH4与足量的F(O2)作用,恢复到25℃水为液体,放出55.6kJ热量;依据化学方程式计算1mol甲烷燃烧放热为889.6KJ;
反应的热化学方程式为:CH4(g)+2O2(g)?点燃?.?CO2(g)+2H2O(l)△H=-889.6kJ?mol-1,
故答案为:CH4(g)+2O2(g)?点燃?.?CO2(g)+2H2O(l)△H=-889.6kJ?mol-1.
本题解析:
本题难度:一般
2、选择题 A、B、C、D、E是原子序数逐渐增大的5种短周期元素,A与B组成的化合物BA4是具有温室效应的气体之一,B与D、C与D组成的化合物是机动车排出的大气污染物,D和E能形成原子个数比为1:1和1:2的两种离子化合物.下列说法不正确的是( )
A.B在元素周期表中的位置是第二周期IVA族
B.工业合成CA3的反应是放热反应,增大压强能加快反应速率,又能提高原料转化率
C.气态氢化物的沸点:C>D
D.C和E组成的一种离子化合物,能与水反应生成两种碱
参考答案:C
本题解析:
本题难度:一般
3、选择题 某固体粉末甲中可能含有K2CO3、KNO3、NaNO2、K2SO3、Na2SO4、FeO、Fe2O3中的若干种,某同学为确定该固体粉末的成分,取甲进行连续实验,实验过程及现象如下:
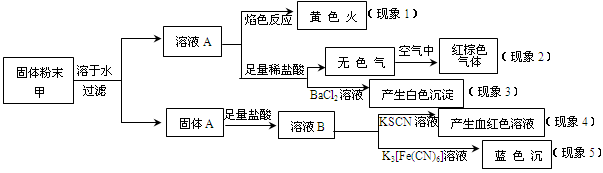
该同学得出的结论正确的是
A.根据现象1可推出该固体粉末中含有钠元素,但不含钾元素
B.根据现象2可推出该固体粉末中一定含有NaNO2
C.根据现象3可推出该固体粉末中一定含有Na2SO4
D.根据现象4和现象5可推出该固体粉末中一定含有FeO和Fe2O3
参考答案:D
本题解析:钠的焰色反应为黄色,故一定含钠元素,观察钾的焰色反应须透过钴玻璃,避免钠的干扰,故无法确定是否含钾,故A错误;红棕色为NO2,则原混合物中可能含有硝酸钠或NaNO2或两者都存在,故B错误;C.K2SO3,在酸性条件下发生氧化还原反应生成SO42-,加入氯化钡生成硫酸钡沉淀,则不一定含硫酸钠,可能有K2SO3,故C错误;溶液B加KSCN溶液呈血红色,说明含有Fe3+,加铁氰化钾显蓝色,证明含亚铁离子,所以该固体含有FeO和Fe2O3.故D正确;故选D。
本题难度:一般
4、填空题 下图为一些物质间的相互转变关系,反应①在工业上可用来生产化合物C,反应⑤在工业上可生产化合物J(Na2FeO4),反应①、②、④和⑤均是在水溶液中进行的反应.常温下,D、E、G均是气体,B是无色液体;F的水溶液可作为杀菌消毒剂;H是一种铁矿石的主要成分,它由两种元素组成,且其中铁元素的质量分数为70%。
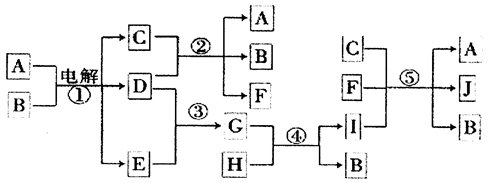
请回答下列问题:
(1)工业上利用反应①生产化合物C,得到化合物C的电极名称是______________。
(2)化合物F中阴离子的电子式为_______________。
(3)反应②的化学方程式为____________________。
(4)反应⑤的离子方程式为_________ __________________。
__________________。
(5)高铁酸钠(Na2FeO4)既能杀菌消毒又是一种“绿色环保高效”的净水剂,其原因为:?
①_______________________________________________________。
②_______________________________________________________。
参考答案:
本题解析:略
本题难度:简单
5、填空题 (10分)由Fe2O3、CuO、A1中的几种物质组成的混合粉末,取样品进行下列实验(部分产物略去):
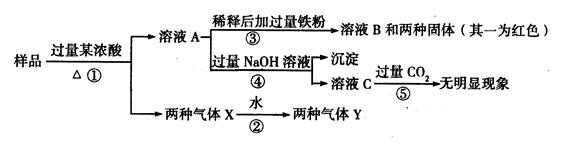
(1)混合气体Y中两种气体的化学式是?,反应①中生成混合气体X的化?
学方程式是?。
(2)通过上述实验及其现象说明,一定不含有的物质是?,不能确定是否含有的物质是?;
(3)为进一步确定样品中的未知物质,可以用上述反应过程中的溶液,设计一个简单的后续实验就可以确定,方法是?。
参考答案:(1)NO、CO2(2分)? C+4HNO3(浓)?CO2↑+4NO2↑+2H2O(2分)
(2)A1(2分)? Fe2O3(2分)
(3)取溶液A少许,向其中加入KSCN溶液,若溶液变红色,说明样品中含有Fe2O3;若溶液不变红色,说明样品中没有Fe2O3(2分)
本题解析:略
本题难度:简单