1������� �Т١��ڡ��ۡ��ܡ��ݡ��ޡ��ߡ��ࡢ�ᡢ��ʮ��Ԫ�أ�ԭ�������������ᡢ��ڵ������ڣ������Ϊ������Ԫ�ء�
��1�����ڡ��ߡ�������Ԫ�������ڱ������λ������
?
������γɵ�Һ�廯�����dz������ܼ������Ԫ�������ڱ��е�λ����?����Ԫ�ص�������ĵ���ʽ��?��������γɵĻ������д��ڵĻ�ѧ����?����ڡ��ߡ�������Ԫ������������Ӧ��ˮ��������������ǿ��˳����?(�û�ѧʽ��ʾ)���ߡ�������Ԫ���γɵ������Ӱ뾶��С˳����?(�����ӷ�����)��
��2�����ס����������������Ϊ����������Ԫ������ɵĵ��ʻ���Ҽס��ҡ���Ϊ��ɫ���壬��Ϊ����ɫ���塣������ͼ��ʾת����ϵ�Ʋ⣺
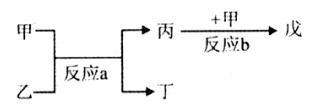
��д����Ӧa�Ļ�ѧ����ʽ��?��
��д�����붡��Ӧ�Ļ�ѧ����ʽ��??��
��3������ͼ��A��B��C��D��E�ֱ�������10��Ԫ����ɵĵ��ʻ��
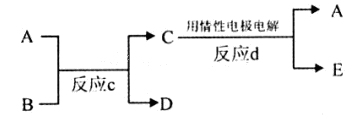
������Ӧc����A�����ص����������B��ˮ��Һ������A�Ǻ�ɫ�������ʣ�E�Ǿ��л���ɫ�����塣��Ӧd�������ĵ缫��ӦʽΪ��?��
������Ӧc���ڸ����½��еġ�����B�ǰ���ɫ���壬������C��һ�����Ի������Ӧc�Ļ�ѧ����ʽΪ?��
�ο��𰸣���1���������ڵڢ�A����2�֣�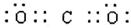 ��1�֣�
��1�֣�
���ۼ���1�֣�H2CO3��H2SO4��HClO4����1�֣�S2�D��Cl�D��1�֣�
��2����4NH3��5O2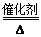 4NO��6H2O��2�֣�
4NO��6H2O��2�֣�
��3NO2��H2O=2HNO3��NO��2�֣�
��3��?��Cu2����2e�D=Cu��2�֣�
��2Al��Fe2O3 2Fe��Al2O3��2�֣�
2Fe��Al2O3��2�֣�
�����������1���ڵ�ԭ��������������1���ɢ������ڱ��е�λ�ÿ�֪���ڴ��ڵڶ����ڣ��ߢദ�ڵ������ڣ�������γɵ�Һ�廯�����dz�������Ҫ�ܼ����û�����ΪSC2��CCl4���ɢڢߢ��λ�ÿ�֪����Ϊ̼����Ϊ��Ϊ�ȣ�������γɵ�Һ�廯����ΪCCl4��Sԭ��ԭ����3�����Ӳ㣬����������Ϊ6���������ڱ��е������ڵڢ�A�壻������̼������̼ԭ������ԭ��֮���γ�2�Թ��õ��Ӷԣ�����ʽΪ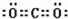 ��CCl4��̼ԭ��������֮���γ�1�Թ��õ��Ӷԣ�Ϊ���ۼ����ǽ�����C��S��Cl������������Ӧˮ���������ǿ����˳����HClO4��H2SO4��H2CO3��S2����Cl�����Ӳ�ṹ��ͬ���˵����Խ�����Ӱ뾶ԽС�������Ӱ뾶S2����Cl������Ϊ���������ڵڢ�A�壻�����ۼ���HClO4��H2SO4��H2CO3��S2����Cl����
��CCl4��̼ԭ��������֮���γ�1�Թ��õ��Ӷԣ�Ϊ���ۼ����ǽ�����C��S��Cl������������Ӧˮ���������ǿ����˳����HClO4��H2SO4��H2CO3��S2����Cl�����Ӳ�ṹ��ͬ���˵����Խ�����Ӱ뾶ԽС�������Ӱ뾶S2����Cl������Ϊ���������ڵڢ�A�壻�����ۼ���HClO4��H2SO4��H2CO3��S2����Cl����
��2����Ϊ����ɫ���壬����ΪNO2����ӦbΪNO+O2��NO2���ɷ�Ӧa��֪�������ҷ�Ӧ���ɱ����ʼ�ΪO2���ʱ�ΪNO����ӦaΪNH3+O2��NO+H2O����ΪNH3����ΪH2O��
�ٷ�Ӧa�Ļ�ѧ����ʽΪ��4NH3+5O2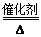 4NO+6H2O���ʴ�Ϊ��4NH3+5O2
4NO+6H2O���ʴ�Ϊ��4NH3+5O2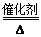 4NO+6H2O��
4NO+6H2O��
��NO2��H2O��Ӧ����HNO3��NO����Ӧ����ʽΪ��3NO2+H2O=2HNO3+NO�����ʴ�Ϊ��3NO2+H2O=2HNO3+NO����
��3����A�Ǻ�ɫ�������ʣ�AΪCu��E�Ǿ��л���ɫ�����壬��EΪCl2����Ӧd������������ԭ��Ӧ����ͭ���ӷŵ�����Cu����Ӧd�������缫��ӦʽΪ��Cu2��+2e���TCu��
�ʴ�Ϊ��Cu2��+2e���TCu��
������Ӧc���ڸ����½��еģ�����C��һ�����Ի����ΪAl2O3������B�ǰ���ɫ���壬ΪFe2O3����ӦcΪ���ȷ�Ӧ��AΪAl��DΪFe��EΪO2����Ӧc�ķ���ʽΪ��Fe2O3+2Al 2Fe+Al2O3���ʴ�Ϊ��Fe2O3+2Al
2Fe+Al2O3���ʴ�Ϊ��Fe2O3+2Al 2Fe+Al2O3��
2Fe+Al2O3��
�����Ѷȣ�һ��
2��ѡ���� X��Y��Z��W��ԭ������������������ֶ�����Ԫ�أ�A��B��C��D��F���������е����ֻ�����Ԫ����ɵĻ����E����ZԪ���γɵĵ��ʣ�0.1 mol��L��1 D��Һ��pHΪ13(25 ��)������������ͼת����ϵ��������˵����ȷ����(����)��
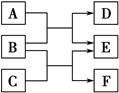
A��ԭ�Ӱ뾶W>Z>Y>X
B��0.1 mol��L��1 F��Һ���������ܵ����ʵ�������0.1 mol��L��1 D��Һ���������ܵ����ʵ���
C��0.1 mol B������C��ȫ��Ӧ��ת�Ƶ�����0.1NA
D��ZԪ�ص��������Ϊ��6
�ο��𰸣�C
�����������0.1 mol��L��1 D��Һ��pHΪ13(25 ��)����DΪһԪǿ���EΪ���ʣ�����Ƴ�DΪNaOH��A��B�ֱ�ΪNa2O2��H2O�е�һ�֣��ٽ��B��C��ӦҲ�ɵõ�����E������ȷ��A��B��C��D��E��F�ֱ�ΪH2O��Na2O2��CO2��NaOH��O2��Na2CO3����֪��X��Y��Z��W�ֱ�ΪH��C��O��Na����Ԫ�ء�ԭ�Ӱ뾶��Na>C>O>H��A�����Z(��)Ԫ��û�У�6�ۣ�D�����0.1 mol Na2O2������CO2��ȫ��Ӧ��ת��0.1 mol���ӣ�C��ȷ����Һ��CO32������ˮ�⣬��������Ŀ���ӣ���Bѡ��δ������Һ�����������������Ŀ����Bѡ�����
�����Ѷȣ�һ��
3������� ��8�֣�ͼ��A��K������ѧ��ѧ�г������ʡ�A��һ���ᣬE��F��Iͨ��״���������壬����E�д̼�����ζ��X��Y�dz����Ľ������ʣ�JΪ���ɫ�������μӷ�Ӧ��ˮ�Լ����ɵ�ˮ��ͼ�о�����ȥ��
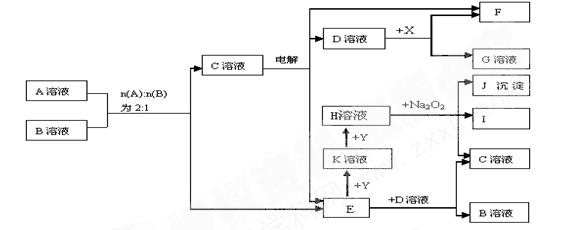
��ش��������⣺
��1��E�ĵ���ʽΪ? _____________��? J�Ļ�ѧʽΪ?��
��2��д������Һ��ٷ�Ӧ�����ӷ���ʽ����������������������������?��
��3��д��D��Һ��ط�Ӧ�����ӷ���ʽ ?__________��
��4��д��A��B �� C��E�Ļ�ѧ����ʽ? ______? __��
�ο��𰸣�����8�֣�
��1��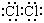 ����1�֣�Fe(OH)3����1�֣�?
����1�֣�Fe(OH)3����1�֣�?
��2��2Fe3+ + Fe = 3Fe2+��2�֣�
��3��2Al + 2H2O + 2OH- = 2AlO2- + 3H2����2�֣�
��4��2HCl + NaClO =" NaCl" + H2O + Cl2����2�֣�
�����������
�����Ѷȣ�һ��
4������� ��֪A��B��C�����ֳ����ĵ��ʣ�����AΪ���壬B��CΪ���壻D�ı�����Һ�����ˮ�м�����У���Һ�ʺ��ɫ��B��C��Ӧʱ�ɹ۲쵽��ɫ���棬����K������ˮ����ɫ��ҺE������֮��ת����ϵ��ͼ��ʾ��
��1��д��D��A��Ӧ�����ӷ���ʽ��
D+A��______��
��D��Һ�еμ����軯�أ���Һ��Ϊ��ɫ��������ӷ���ʽ��______��
��2��д����F�м���NaOH���ڿ����з����������ķ�Ӧ�Ļ�ѧ����ʽ���漰�����仯����______��______��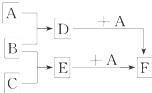
�ο��𰸣�A��B��C�����ֳ����ĵ��ʣ�����AΪ���壬B��CΪ���壻D�ı�����Һ�����ˮ�м�����У���Һ�ʺ��ɫ��D���Ȼ�����A��B���ǵ��ʣ���A�ǹ��壬����A������B��������B��C��Ӧʱ�ɹ۲쵽��ɫ���棬����K������ˮ����ɫ��ҺE����C��������E���Ȼ��⣬���������Ӧ�����Ȼ���������F���Ȼ�������
��1���Ȼ���������Ӧ�����Ȼ����������ӷ�Ӧ����ʽΪ��2Fe3++Fe�T3Fe2+�������Ӻ����軯����Һ��Ӧ����������ʹ��Һ��Ѫ��ɫ�����ӷ�Ӧ����ʽΪ��Fe3++3SCN-�TFe��SCN��3��
�ʴ�Ϊ��2Fe3++Fe�T3Fe2+��Fe3++3SCN-�TFe��SCN��3��
��2���Ȼ��������������Ʒ�Ӧ���ɰ�ɫ�����������������������������ȶ����ױ������������ɺ��ɫ������������Ӧ����ʽΪ��FeCl2+2NaOH�TFe��OH��2��+2NaCl��4Fe��OH��2+O2+2H2O�T4Fe��OH��3��
�ʴ�Ϊ��FeCl2+2NaOH�TFe��OH��2��+2NaCl��4Fe��OH��2+O2+2H2O�T4Fe��OH��3��
���������
�����Ѷȣ���
5������� A��B��C��D��E��F?�dz������ʣ�����?A?���������Ӧ����㷺�Ľ�����Ԫ��?D?�ǵؿ��к������Ľ���Ԫ�أ�D?Ԫ�غ�?E?Ԫ�������ڱ������ڣ�G��H��l��J��K��L?�dz������������?G?�ڳ���������ɫҺ�壬H?�Ǻ�ɫ���壬������������ת����ϵ��ͼ��ʾ��
��ش��������⣺
��1��Ԫ��?A?��Ԫ�����ڱ��е�λ��Ϊ______�����ڣ�______���壩��
��2��д��?K?�ĵ���ʽ______��
��3��д��?H?��?D?��Ӧ�Ļ�ѧ����ʽ______��
��4��D?��������������Һ��Ӧ����д���÷�Ӧ�����ӷ���ʽ��______��
��5��д��?A?��?G?��Ӧ�Ļ�ѧ����ʽ______��
��6��K?��?E?��Ӧʱ������������______���÷�Ӧ�Ļ�ѧ����ʽΪ______��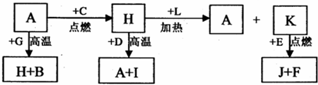
�ο��𰸣�A��B��C��D��E��F �dz������ʣ����� A ���������Ӧ����㷺�Ľ����ж�ΪFe��Ԫ�� D �ǵؿ��к������Ľ���Ԫ���ж�ΪAl��G��H��l��J��K��L �dz������������ G �ڳ���������ɫҺ���ж�ΪH2O��H �Ǻ�ɫ������ת����ϵ�ж�ΪFe3O4��˵��CΪO2��A��Fe��+G��H2O��=H��Fe3O4��+B��H2��������GΪH2O��HΪFe3O4��BΪH2��H��Fe3O4��+D��Al��=A��Fe��+I��Al2O3��������H+L=A+K��֪��LΪΪCO��KΪCO2��D Ԫ�غ� E Ԫ�������ڱ������ڣ����K+E=J+F�ƶ�EΪMg��JΪMgO��FΪC��
��?l?��Ԫ�� A ΪFe����Ԫ�����ڱ��е�λ��Ϊ���������ڣ�VIII�壬�ʴ�Ϊ���ģ�VIII��
��?2?�� K ΪCO2��������̼�ĵ���ʽΪ��
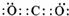
���ʴ�Ϊ��
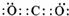
��
��?3?�� H ��Fe3O4���� D ��Al����Ӧ�Ļ�ѧ����ʽ��3Fe3O4+8Al??����?.??4A12O3+9Fe���ʴ�Ϊ��3Fe3O4+8Al ?����?.? 4A12O3+9Fe��
��?4?��D ��������������Һ��Ӧ����д���÷�Ӧ�����ӷ���ʽ��2Al+2OH-+2H2O=2A1O2-+3H2�����ʴ�Ϊ��2Al+2OH-+2H2O=2A1O2-+3H2����
��?5?��A ��Fe���� G��H2O�� ��Ӧ�Ļ�ѧ����ʽΪ��3Fe+4H2O?��?g?��?����?.??Fe3O4+4H2 ���ʴ�Ϊ��3Fe+4H2O �� g ��?����?.? Fe3O4+4H2 ��
��?6?��K��CO2�� �� E��Mg�� ��Ӧʱ����������Ϊ��þ������ȼ�գ�������ҫ�۵İ⣬��ƿ�ڻ�ƿ�׳��ְ�ɫ����ͺ�ɫ��������Ӧ�Ļ�ѧ����ʽΪ2Mg+CO2?��ȼ?.? 2MgO+C��
�ʴ�Ϊ��þ������ȼ�գ�������ҫ�۵İ⣬��ƿ�ڻ�ƿ�׳��ְ�ɫ����ͺ�ɫ������2Mg+CO2?��ȼ?.? 2MgO+C��
���������
�����Ѷȣ�һ��