1、选择题 取等质量的钠进行下列实验,其中生成氢气最多的是(?)
A.将钠投入足量的水中
B.将钠用耐热塑料薄膜包好并刺一些小孔,再放入足量的水中
C.将钠投入足量的稀硫酸中
D.将钠用铝箔包好并刺一些小孔,再放入足量的水中
参考答案:D
本题解析:将等质量的钠投入足量的水和稀硫酸中,发生反应的反应分别为2Na+2H2O====2NaOH+H2↑,2Na+2H2SO4====Na2SO4+H2↑,实质均为钠与氢离子反应生成氢气,由于钠的质量相同,A、B、C三者放出的氢气的量相等;将钠用铝箔包好并刺一些小孔,再放入足量的水中,首先是钠与水反应生成NaOH和氢气,铝与NaOH溶液反应生成氢气,故生成氢气要比上述三种情况多,选D。
本题难度:一般
2、选择题 下列物质分别加入小苏打溶液中,即无沉淀又无气体生成的是
①Ca(OH)2②CaCl2?③NaHSO4?④Na2O2?⑤Na?⑥NaOH
A.④⑥
B.②⑥
C.①③
D.①⑤
参考答案:B
本题解析:小苏打溶液与Ca(OH)2溶液反应产生沉淀;与NaHSO4溶液反应产生气体;与Na2O2固体反应放出气体;与Na反应放出气体。答案选B。3的性质
点评:本题考查元素化合物性质的基础题,难度小,可以帮助学生夯实基础。
本题难度:一般
3、简答题 在呼吸面具和潜水艇中可用过氧化钠作为供氧剂.某化学探究学习小组选用适当的化学试剂和实验用品,A是用大理石和稀盐酸制取CO2的装置,用下图中实验装置,进行实验来证明过氧化钠可作供氧剂.
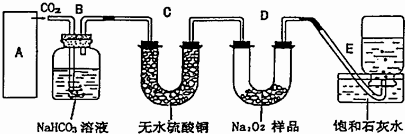
(1)B装置的作用是______,写出该装置中发生反应的离子方程式______;
(2)C装置内的现象是______;
(3)写出D装置中发生反应的化学方程式______;
(4)若无C装置,D装置可能发生的干扰反应的化学方程式为______;
(5)为了检验E中收集到的气体,在取出集气瓶后,______.
参考答案:(1)用稀盐酸与大理石反应制得的二氧化碳中含有氯化氢气体,B中饱加入和NaHCO3溶液除去二氧化碳中的氯化氢;溶液中NaHCO3与HCl反应生成二氧化碳,其反应的离子方程式为:HCO3-+H+=H2O+CO2↑,
故答案为:除去CO2中的混有的HCl;HCO3-+H+=H2O+CO2↑;
(2)C装置中的无水硫酸铜遇到水会生成蓝色的硫酸铜晶体,故答案为:无水硫酸铜固体由白色变为蓝色;
(3)D装置中为过氧化钠与二氧化碳反应,其反应的化学方程式为:2Na2O2+2H2O=4NaOH+O2↑,故答案为:2Na2O2+2H2O=4NaOH+O2↑;
(4)若无C装置,则前面溶液中挥发出来的水蒸气进入D与过氧化钠反应;所以其反应方程式为:2Na2O2+2H2O=4NaOH+O2↑,故答案为:2Na2O2+2H2O=4NaOH+O2↑;
(5)一般用带火星的木条检验氧气,其操作为:立即将带火星的木条放在试管口,看木条是否复燃,故答案为:立即将带火星的木条放在试管口,看木条是否复燃.
本题解析:
本题难度:一般
4、填空题 取等物质量浓度的NaOH溶液两份,每份为50ml。向其中通入一定量的CO2,随后分别取溶液10ml,将其稀释成100ml,并分别向稀释后的溶液中逐滴加入0.1mol/L的HCI溶液,产CO2的体积(标准状况)与加入盐酸体积之间的关系如图所示(设分别为A、B两种情况)。
 回答下列问题:
回答下列问题:
 ?(1)在(A)情况下,溶质为(写化学式)?,其物质的量之比为?,在标准状况下,通人CO2气体的体积为? ?。
?(1)在(A)情况下,溶质为(写化学式)?,其物质的量之比为?,在标准状况下,通人CO2气体的体积为? ?。
 ?(2)在(B)情况下,溶质为(写化学式)?,其物质的量之比为?,在标准状况下,通人CO2气体的体积为? ?。
?(2)在(B)情况下,溶质为(写化学式)?,其物质的量之比为?,在标准状况下,通人CO2气体的体积为? ?。
 ?(3)原NaOH溶液的物质的量浓度为? ?。
?(3)原NaOH溶液的物质的量浓度为? ?。
参考答案:①NaOH、Na2CO3







 ?3:1 ?33.6
?3:1 ?33.6
②Na2CO3、NaHCO3?1:1 ?112
③ 0.75mol/L
本题解析:根据题意和图像综合分析,在(A)情况下,溶质为NaOH、Na2CO3在(B)情况下,溶质为Na2CO3、NaHCO3
本题难度:简单
5、选择题 分别用等质量的金属钠进行下列实验,其中生成氢气的体积(同温同压)最大的是
A.将钠投入到足量水中
B.将钠用铝箔包好并刺一些小孔,再放入足量水中
C.将钠放入足量稀硫酸中
D.将钠放入足量氢氧化钠溶液中
参考答案:B
本题解析:略
本题难度:简单