1、选择题 已知某温度下AgCl(s)的溶度积常数Ksp=1×10-10.在该温度下,向50mL?0.018mol/L的AgNO3溶液中加入50mL?0.02mol/L的盐酸,生成沉淀(混合后溶液的体积变化忽略不计).下列说法正确的是( )
A.AgCl的溶解性为难溶,则该物质不溶于水
B.沉淀生成后,溶液中Ag+的浓度1×10-5?mol/L
C.沉淀生成后,溶液的pH为2
D.沉淀生成后,溶液中NO3-的浓度1.8×10-2?mol/L
2、选择题 在常温时的下列溶液中,BaSO4的溶解度最大的是
[? ? ]
A.40?mL?1?mol/L的BaCl2溶液
B.30?mL?2?mol/L的Ba(OH)2溶液
C.10?mL纯水
D.50?mL?0.1?mol/L的H2SO4溶液
3、选择题 已知:在25℃时,?H2O H++OH- ?KW=10-14 ?
H++OH- ?KW=10-14 ?
CH3COOH H++CH3COO- ?Ka=1.8×10-5?
H++CH3COO- ?Ka=1.8×10-5?
KSP[Mg(OH)2]=1.8×10-11?
?KSP[Zn(OH)2]=1.2×10-17、
KSP[Cd(OH)2]=2.5×10-14?
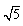 ?=2.2 下列说法正确的是
?=2.2 下列说法正确的是
[? ]
A.醋酸钠水解的平衡常数Kh随温度升高而减小
B.0.5mol・L-1醋酸钠溶液pH为m,其水解的程度(已水解的醋酸钠与原有醋酸钠的比值)为a;1mol・L-1醋酸钠溶液pH为n,水解的程度为b,则m<n?、?a>b ?
C.醋酸钠的水解的平衡常数Kh=?KW?Ka ?
D.在某溶液中含Mg2+、Cd2+、Zn2+三种离子的浓度均为0.01mol・L-1?,向其中加入固体醋酸钠,使其浓度为0.9mol・L-1,以上三种金属离子中只有Zn2+?能生成沉淀
4、简答题 用菱锌矿(主要成分为碳酸锌,还含有Fe2+、Fe3+、Mg2+、Ca2+、Cu2+等)制备氯化锌的一种流程如下:
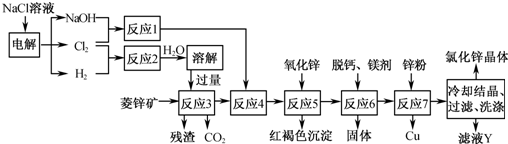
(1)在反应3前要将菱锌矿研磨,其目的是______.
(2)反应4将Fe2+氧化为Fe3+,该反应的离子方程式为______.
(3)加入氧化锌调节pH=4.5,反应5的离子方程式为______、______.
(4)锌粉不在反应4之前加入的原因是______.
(5)若用石墨作电极电解滤液Y,则可以得到参与本流程反应的物质有______.
5、填空题 (1)100℃时纯水Kw=1×10-12?mol2?L-2在该温度下,将1mL?0.001mol?L-1的NaOH溶液的pH为______,若加水稀释至100L,则溶液的pH为______.
(2)室温下,pH=1的稀硫酸a?L与pH=12的苛性钠b?L混合后溶液的pH=2,忽略溶液混合前后体积变化,则a:b=______.
(3)已知25℃时100g水中溶有0.74g的Ca(OH)2即达到饱和,则该条件下Ca(OH)2离子积为Ksp=______.