1、选择题 科学家成功开发便携式固体氧化物燃料电池,它以丙烷气体为燃料.电池中的一极通入空气,另一极通入丙烷气体,电解质是固态氧化物,在熔融状态下能传导O2-.下列对该燃料电池的说法不正确的是( )
A.在熔融电解质中,O2-由负极移向正极
B.该电池的总反应是:C3H8+5O2=3CO2+4H2O
C.电路中每通过5mol电子,约有5.6L标准状况下的丙烷被完全氧化
D.通丙烷的电极为电池负极,发生的电极反应为:C3H8-20e-+10O2-=3CO2+4H2O
参考答案:A.在熔融电解质中,O2-由正极移向负极,故A错误;
B.丙烷燃料电池的总反应式与丙烷燃烧的方程式相同,都为C3H8+5O2=3CO2+4H2O,故B正确;
C.n(C3H8)=5.6L22.4L/mol=0.25mol,C3H8被氧化为CO2,根据化合价的变化可知,转移电子的物质的量为0.25mol×[3×4-(-8)]=5mol,也可根据电极反应式判断,故C正确;
D.电池工作时,丙烷在负极被氧化,电极方程式为C3H8-20e-+10O2-=3CO2+4H2O,故D正确.
故选A.
本题解析:
本题难度:简单
2、选择题 氢氧燃料电池以H2为还原剂,O2为氧化剂,电极为多孔镍,电解液为30%的KOH溶液,下列有关叙述正确的是
[? ]
①负极质量减轻 ②负极反应为4OH--4e-=O2↑+2H2O ③负极反应为H2+2OH--2e-=2H2O
④工作时正极区pH升高,负极区pH降低?⑤工作时溶液中阴离子移向正极?
A.①③④
B.②③⑤
C.④⑤
D.③④
参考答案:D
本题解析:
本题难度:一般
3、填空题 电解原理在化学工业中有广泛应用。右图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:
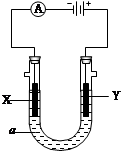
(1)X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时同时在两边各滴入几滴酚酞试液,则
①电解池中X极上的电极反应式为 ,
在X极附近观察到的现象是 。
②Y电极上的电极反应式为 ,
检验该电极反应产物的方法是 。
③总反应的化学方程式 。
(2)X、Y都是惰性电极,电解CuSO4溶液,当电路中通过0.4mol 电子时,析出铜的同时在另一个电极可得 L O2 (标准状况下)
参考答案:(1)① 2H+ + 2e_= H2↑ 电极表面有气泡产生,电极附近的溶液呈红色
②2Cl--2e- =Cl2↑;用镊子夹持湿润的淀粉KI试纸靠近Y电极出气口,若试纸变蓝,则产物为CI2。
③2NaCl+2H2O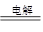 2NaOH+H2↑+Cl2↑ (2) 2.24L
2NaOH+H2↑+Cl2↑ (2) 2.24L
本题解析:(1)①根据装置图可知,X和电源的负极相连,则X是阴极,溶液中的氢离子放电,所以X电极的电极反应式是2H+ + 2e_= H2↑。氢离子放电,破坏了阴极周围水的电离平衡,从而使阴极周围溶液显碱性,则实验现象是电极表面有气泡产生,电极附近的溶液呈红色。
②Y电极是阳极,溶液中的Cl-放电,则Y电极上的电极反应式为2Cl--2e- =Cl2↑;氯气具有氧化性,能使湿润的淀粉KI试纸变蓝,据此可以检验氯气,即用镊子夹持湿润的淀粉KI试纸靠近Y电极出气口,若试纸变蓝,则产物为CI2。
③总反应的化学方程式为2NaCl+2H2O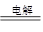 2NaOH+H2↑+Cl2↑。
2NaOH+H2↑+Cl2↑。
(2)OH-放电的电极反应式是4OH--4e-=2H2O+O2↑,则根据电子的得失守恒可知,生成氧气的物质的量是0.1mol,在标准状况下的体积是2.24L。
考点:考查电解原理应用的有关判断以及电极反应式的书写和计算
点评:该题是高考中的常见题型,属于中等难度的试题。试题基础性强,侧重对学生能力的培养和解题方法的指导与训练,有助于培养学生的逻辑推理能力和规范的答题能力。该题的关键是明确电解池的工作原理,然后结合题意灵活运用即可。
本题难度:一般
4、填空题 (14分)

I.我国即将建成自己的载人空间站。载人航天器的生态系统中,不仅要求分离去除CO2,还要求提供充足的O2。
⑴某种电化学装置可实现如下转化:2CO2=2CO+O2,CO可用作燃料。已知该反应的某极反应为:4OH--4e-=O2↑+2H2O,则另一极反应为:?。
⑵有人提出,可以设计某温度下的反应:2CO=2C+O2(△H>O、△S<O)来消除CO的污染。请你判断该温度下上述反应是否能发生并说明理由是?。
Ⅱ.大气固氮属于自然固氮,合成氨是目前人工固氮的主要方法。科学家一直致力“人工固氮”新方法的研究。
⑴有关大气固氮(以N2+O2?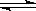 ?2NO为例)、人工固氮(以N2+3H2
?2NO为例)、人工固氮(以N2+3H2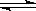 ?2NH3为例)反应的平衡常数
?2NH3为例)反应的平衡常数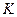 的值如下表。
的值如下表。
反应
| N2+02 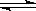 2NO? 2NO?
| N2+3H2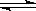 2NH3 2NH3
|
温度/℃
| ?27
| 2000
| 100
| 400
|
K
| ?3.84×10-31
| ?0.1
| 3.4×109
| 2.0x104
|
下列说法正确的是?。(填字母)
a.大气固氮与人工固氮都是放热反应
b.人类模拟大气固氮无现实意义
c.寻找在常温下合成氨的高效催化剂是目前人工固氮的新方向
d.在常温下,人工固氮非常容易进行
⑵已知:N2(g)+3H2(g) 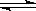 ?2NH3(g)?
?2NH3(g)?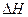 =-92.4kJ・mol-1
=-92.4kJ・mol-1
2H2(g)+02(g)="2H20(1)?" 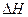 ="-571.6" kJ・mol-1
="-571.6" kJ・mol-1
据报道,在常温、常压、光照、催化剂的条件下,N2可以与水反应,则反应 N2(g)+3H20(1)=2NH3(g)+3/2O2(g)的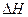 =?KJ・mol-1。
=?KJ・mol-1。
⑶某研究小组在673 K、30 MPa下,在体积为 的密闭容器中进行反应:N2(g)+3H2(g)
的密闭容器中进行反应:N2(g)+3H2(g) 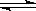 2NH3(g),其
2NH3(g),其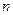 (H2)和
(H2)和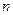 (NH3)随时间变化的关系如图所示。
(NH3)随时间变化的关系如图所示。

①下列叙述正确的是?。(填字母)
A.点a的正反应速率比点b的大
B.点c处反应达到化学平衡状态
C.若t3时由673 K升至773 K,则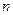 (H2)将增大
(H2)将增大
②从开始到平衡时反应的平均速率(以H2的浓度变化表示)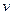 (H2)=?。
(H2)=?。
③若开始时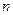 (N2)=
(N2)=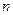 (H2),则反应的平衡常数
(H2),则反应的平衡常数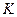 =?(用代数式表示)。
=?(用代数式表示)。
参考答案:14分I.(1)2CO2+4e-+2H2O=2CO+4OH-?(2)不能,这是个焓增熵减的变化
Ⅱ.(1)bc (2)+765.0 kJ・mol-1 (3)① AC ② 3n2/(2Vt2) ?mol/(L・s)
③n22V2/[(n3-n2/2)×(n3-3n2/2)3]
本题解析:略
本题难度:一般
5、选择题 下列关于右图装置的说法正确的是
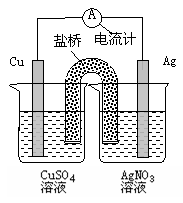
A.银电极是负极
B.铜电极上发生的反应为Cu-2e-=Cu2+
C.外电路中的电子是从银电极流向铜电极。
D.该装置能将电能转化为化学能
参考答案:B
本题解析:A项:银电极是正极,故错;C项:外路电子从铜电极流向银电极,故错;D项:原电池装置,化学能转化为电能,故错。故选B。
点评:本题考查学生原电池的工作原理,注意教材知识的灵活应用,属于基础知识的综合考查,难度不大。
本题难度:简单