1、填空题 为体现绿色世博、低碳世博、科技世博,上海世博会已经开始使用中国自己生产的燃料电池汽车,该车以氢气和空气中的氧气为燃料,KOH为电解质溶液,真正实现了“零排放”.该电池的负极反应式为______,从能量角度分析氢气用作燃料电池与直接燃烧相比主要优点是______.
参考答案:碱性氢氧燃料电池的负极为通入氢气的一极,发生氧化反应,电极反应为H2-2e-+2OH-=2H2O,原电池具有能量利用率高的特点,而燃烧时化学能转变为热能和光能.
故答案为:H2-2e-+2OH-=2H2O;燃料电池的能量转换效率高.
本题解析:
本题难度:一般
2、选择题 (2009河北石家庄一模,29)最新研制的一种由甲醇和氧气以及强碱作电解质溶液的新型手机电池。下列有关此电池的叙述错误的是(?)
A.正极电极反应:O2+2H2O+4e-====4OH-
B.负极电极反应:CH3OH+8OH--6e-====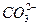 +6H2O
+6H2O
C.电池在使用过程中电解质溶液的pH升高
D.当外电路通过0.6 mol电子时,理论上消耗甲醇3.2 g
参考答案:C
本题解析:A、B项正确,所以电池在使用过程中消耗OH-,电解质溶液的pH降低。
本题难度:一般
3、选择题 用惰性电极分别电解下列各物质的水溶液,一段时间后,向剩余电解质溶液中加入适量相应的溶质能使溶液恢复到电解前浓度的是()
A.AgNO3
B.Na2SO4
C.CuCl2
D.KCl】
参考答案:C
本题解析:四种电解类型分别是:
(1)分解水型:含氧酸、强碱、活泼金属的含氧酸盐(如NaOH、H2SO4、K2SO4等)的电解。
阴极:4H++4e-=2H2↑? 阳极:4OH--4e-=O2↑+2H2O?总反应:2H2O 2H2↑+O2↑
2H2↑+O2↑
阴极产物:H2;阳极产物:O2。 电解质溶液复原加入物质:H2O。
pH变化情况:原来酸性的溶液pH变小,原来碱性的溶液pH变大,强酸(含氧酸)强碱的正盐溶液pH不变。
(2)分解电解质型:无氧酸(除HF外)、不活泼金属的无氧酸盐(氟化物除外)的电解,如HCl、CuCl2等。
阴极:Cu2++2e-=Cu? 阳极:2Cl--2e-=Cl2↑?总反应:CuCl2 Cu+Cl2↑
Cu+Cl2↑
阴极产物:酸为H2,盐为金属;阳极产物:卤素等非金属单质。
电解液复原加入物质为原溶质,如电解CuCl2溶液,需加CuCl2。
pH变化情况:如电解无氧酸溶液pH变大但不会超过7;如为盐溶液的电解则视无氧酸根的情况而定。
(3)放氢生碱型:活泼金属的无氧酸盐(氟化物除外)溶液的电解,如NaCl、MgBr2等。
阴极:2H++2e-=H2↑ 阳极:2Cl--2e-=Cl2↑?总反应:2NaCl+2H2O 2NaOH+H2↑+Cl2↑
2NaOH+H2↑+Cl2↑
阴极产物:碱和H2;阳极产物:卤素等非金属单质。电解饱和食盐水的产物分别为NaOH和H2以及Cl2。
电解液复原加入物质为卤化氢。电解饱和食盐水,要使电解质溶液复原需加入HCl。
pH变化情况:电解液pH显著变大
(4)放氧生酸型:不活泼金属的含氧酸盐溶液的电解,如CuSO4、AgNO3等。
阴极:2Cu2++4e-=Cu? 阳极:4OH--4e-=O2↑+2H2O?总反应:2CuSO4+2H2O  2Cu+O2↑+2H2SO4
2Cu+O2↑+2H2SO4
阴极产物:析出不活泼金属单质;阳极产物是该盐对应的含氧酸和氧气,本例中分别是Cu以及H2SO4、O2.
电解液复原加入物质为不活泼金属的氧化物(金属价态与原盐中相同)。如电解CuSO4溶液,复原需加入CuO。
pH变化情况:溶液pH显著变小。
点评:该题是高考中的常见题型,属于中等难度的试题。试题综合性强,侧重对学生基础知识的巩固和训练,主要是考查学生对电解原理的熟悉了解程度,有利于调动学生的逻辑推理能力和发散思维能力,提高学生灵活运用基础知识解决实际问题的能力。该题的关键是明确电解的工作原理,然后结合题意灵活运用即可。
本题难度:简单
4、选择题 某种熔融碳酸盐燃料电池以Li2CO3、K2CO3为电解质、以CH4为燃料时,该电池工作原理见下图。下列说法正确的是
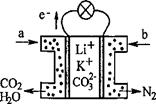
A.a为CH4,b为CO2
B.CO32