1������� ��1���Ȼ���ˮ��Һ��______�ԣ�ԭ����______�������ӷ���ʽ��ʾ������AlCl3��Һ�������գ����õ�����Ҫ���������______���ѧʽ����
��2����������ˮʱ����ˮ�⣬��ˮ������ӷ���ʽΪ______��������������Һʱ���Լ���������______���ѧʽ����������ˮ�⣮
��3����֪��C��s��+O2��g���TCO2��g����H=-393.5kJ/mol
CO��g��+
O2��g���TCO2��g����H=-283kJ/mol
��1mol?C��s����O2��g����Ӧ����CO��g�����Ȼ�ѧ����ʽΪ______��
�ο��𰸣���1���Ȼ�����ǿ��������ˮ��Һ��ˮ�������ԣ�ˮ�����ӷ���ʽΪ��Al3++3H2O?Al��OH��3+3H+����������ˮ�����ɵ��Ȼ���ӷ��õ�ˮ����������������������������ֽ�������������
�ʴ�Ϊ���ᣬAl3++3H2O?Al��OH��3+3H+��Al2O3��
��2����������ˮʱ����ˮ�⣬��ˮ������ӷ���ʽΪS2-+H2O?HS-+OH-��HS-+H2O?H2S+OH-��������������Һʱ���Լ���������������������ˮ�⣻
�ʴ�Ϊ��S2-+H2O?HS-+OH-��HS-+H2O?H2S+OH-��NaOH��
��3����C��s��+O2��g���TCO2��g����H=-393.5kJ/mol
��CO��g��+12O2��g���TCO2��g����H=-283kJ/mol
���ݸ�˹���ɢ�-�ڵõ�C��s��+12O2��g��=CO��g����H=-110.5kJ/mol��
�ʴ�Ϊ��C��s��+12O2��g��=CO��g����H=-110.5kJ/mol��
���������
�����Ѷȣ�һ��
2������� ��1����25�桢101kPa�£�1g����ȼ������CO2��Һ̬ˮʱ����55��6kJ�����ʾ����ȼ���ȵ��Ȼ�ѧ����ʽΪ_____________________________��
��2���������·�Ӧʽ��
A��Na+(g)��Cl-(g)��NaCl(s)����H
B��Na(s)��1/2Cl2(g)��NaCl(s)����H1
C��Na(s)��Na(g)����H2
D��Na(g)��e-��Na+(g)����H3
E��1/2Cl2(g)��Cl(g)����H4
F��Cl(g)��e-��Cl-(g)����H5
д����H1���H����H2����H3����H4����H5֮��Ĺ�ϵʽ__________________________
��3���±��е����ݱ�ʾ�ƻ�1 mol��ѧ�������ĵ�����(�����ܣ���λΪkJ��mol-1)��
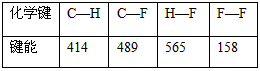
���ݼ������ݼ������·�Ӧ�ķ�Ӧ�ȡ�H��
CH4��g��+4F2��g��==CF4��g��+4HF��g�� ��H=______________________
�ο��𰸣���1��CH4(g)+2O2(g)=CO2(g)+2H2O(l) ��H��-889.6kJ��mol-1
��2����H1����H+��H2+��H3+��H4+��H5
��3��-1928kJ/mol
���������
�����Ѷȣ�һ��
3��ѡ���� ��֪�Ȼ�ѧ����ʽC2H2��g��+
O2��g��=2CO2��g��+H2O��g������H=-1256kJ/mol������˵����ȷ���ǣ�������
A����Ȳ��ȼ����Ϊ1256kJ/mol
B����ת��10mol���ӣ�������2.5mol?O2
C��������2molҺ̬ˮ�����H=-2512kJ/mol
D�����γ�4mol̼�����õ��Ӷԣ���ų�������Ϊ2512kJ
�ο��𰸣�B
���������
�����Ѷȣ�һ��
4��ѡ���� ��֪��H2��g��+F2��g���T2HF��g����H=-270kJ������˵����ȷ���ǣ� ? ��
A��1������������1���������ӷ�Ӧ����2����������ӷų�270kJ
B��1mol������1mol������Ӧ����2molҺ̬������ų�������С��270kJ
C����ͬ�����£�1mol������1mol�����������ܺʹ���2mol���������������
D��2mol����������ֽ��1mol��������1mol�ķ����ų�270kJ����
�ο��𰸣�C
���������
�����Ѷȣ���
5��ѡ���� ����ͼʾ���Ӧ�������������

A��ͼ1��ʾ����μӵ�0.1 mol��L��1ij����Һ�õ��ĵζ����ߣ�����֪Ũ������ζ�δ֪Ũ�ȸü�ʱ���ѡȡ��̪��ָʾ����
B��ͼ2��ʾ�Ѵ�ƽ���ij��Ӧ����t0ʱ�ı�ijһ������Ӧ������ʱ��仯����ı������һ���Ǽ��������
C��ͼ3��ʾ��ҵ����CO�����״��ķ�ӦCO(g)��2H2(g) CH3OH(g)���÷�Ӧ�Ħ�H=��91kJ/mol��
CH3OH(g)���÷�Ӧ�Ħ�H=��91kJ/mol��
D��ͼ4��ʾ���ʵ���֮��Ϊ2��3��þ�����ֱ������ϡ���ᷴӦʱ��������������(V)��ʱ��(t)�Ĺ�ϵ��