1������� �����������Ļ������ڹ�����ռ����Ҫ��λ���ϳɰ���ҵ�У��ϳ�����ÿ����2 mol NH3���ų�92��4 kJ������
��1������ʼʱ�������ڷ���2 mol N2��6 mol H2����ƽ���ų�������ΪQ����Q 184��8kJ���>������<����=������һ�������£����ܱպ��ݵ������У��ܱ�ʾ��Ӧ�ﵽ��ѧƽ��״̬���� ��
a��3v��(N2)=v��(H2�� b��2v��(H2)= v��(NH3��
c����������ܶȱ��ֲ��� d��c(N2)��c(H2)��c(NH3)=1��3��2
��ҵ�������ص�ԭ������NH3��CO2Ϊԭ�Ϻϳ�����[CO(NH2)2]����Ӧ�Ļ�ѧ����ʽΪ
2NH3 (g)+ CO2 (g�� CO(NH2)2 (l��+ H2O (l)��
CO(NH2)2 (l��+ H2O (l)��
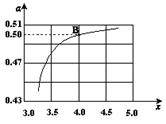
��2����һ���¶Ⱥ�ѹǿ�£���ԭ�����е�NH3��CO2�����ʵ���֮�ȣ���̼�ȣ�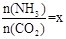 ����ͼ�ǰ�̼�ȣ�x����CO2ƽ��ת���ʣ������Ĺ�ϵ��������x����������ԭ���� ��
����ͼ�ǰ�̼�ȣ�x����CO2ƽ��ת���ʣ������Ĺ�ϵ��������x����������ԭ���� ��
��3��ͼ�е�B�㴦��NH3��ƽ��ת����Ϊ ��
��4����֪�� 3Cl2+2NH3��N2+6HCl
2������� ��ҵ��������淋�����ͼ��ͼ��
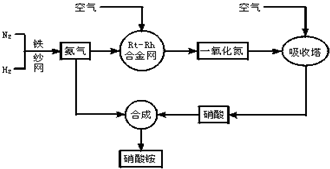
��ش��������⣺
��1��д��������ڹ�ũҵ�����е���Ҫ����______����дһ����
��2����֪N2��g��+3H2��g���T2NH3��g������H=-92kJ?mol-1����ش�
����500�桢200atm��������������һ�ܱ������г���1molN2��3molH2����ַ�Ӧ�ų�������______���������������=����92.4kJ��������______��
��Ϊ��Ч���������ת���ʣ�ʵ���������˲�ȡ�Ĵ�ʩ��______
A�������¶�?B�����ʺϴ������Ե��ʵ�����?C������ѹǿ
D������ѹǿ?E��ѭ�����úͲ��ϲ��䵪��?F����ʱ�Ƴ���
��3����֪����Ͻ���δԤ��Ҳ�ᷢ�ȣ�д�����������Ļ�ѧ����ʽ��______���÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽK=______�����¶�����ʱ��Kֵ______������С����Ӱ�죩����ԭ����______��
��4����һ���¶Ⱥ�ѹǿ���ܱ������У���ƽ��ʽ��Ϊ8.5��H2��N2��ϣ����÷�Ӧ�ﵽƽ��ʱ�����ƽ��������ƽ��ʽ��Ϊ10����ʱN2��ת����Ϊ______��
3������� д�������Ȼ�ѧ����ʽ��
(1)2mol Cu(s)������O2(g)��Ӧ����CuO(s)���ų� 314 kJ����____________��
(2)1mol N2(g)������O2(g)��Ӧ����NO(g)�������� 68 kJ������______________��
(3)��״���£�12 g̿���������в���ȫȼ������һ����̼���ų�110. 35 kJ������________________��
4������� ����ѧ֪ʶϵͳ���������ڶԻ�ѧ����Ľ�һ����ʶ�����⡣
����1����ѧ��Ӧ����ײ���ۣ���Ӧ����Ӽ�����ײ�Ƿ�Ӧ���еı�Ҫ��������������ÿ����ײ��������Ӧ��ֻ��������ײ���ܷ�����ѧ��Ӧ����������ѧ��Ӧ����ײ��֮Ϊ��Ч��ײ��
����2����ѧ��Ӧ�Ĺ���̬���ۣ���ѧ��Ӧ������ͨ������ײ������ɵģ������ڷ�Ӧ�ﵽ������Ĺ����о���һ���������Ĺ���̬��
����3����ѧ��Ӧ�������仯(��H)�뷴Ӧ���������ļ����йء�������ѧ��̬��298K��1.01��105Pa���£����ȶ��ĵ��ʷ�����Ӧ����1mol������ķ�Ӧ�Ƚиû�����������ȣ���H����
�����������ϻش��������⣺
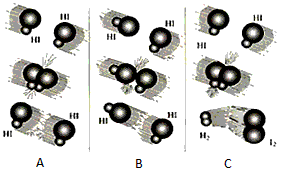
��1����ͼ��HI�ֽⷴӦ��HI����֮��ļ�����ײʾ��ͼ������������Ч��ײ���� __________________��ѡ�A������B����C������
��2����ͼ��1molNO2��CO��Ӧ����CO2��NO�����������仯ʾ��ͼ����д��NO2��CO��Ӧ���Ȼ�ѧ����ʽ�� ___________________________________________��
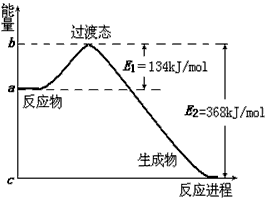
��3�� �±��Dz��ֻ�ѧ���ļ�������
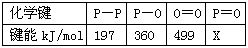
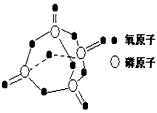
��֪����ȼ����Ϊ2378.0 kJ/mol��������ȫȼ�յIJ���ṹ(P4O10)���ϣ��ң�ͼ��ʾ�����ϱ���X��
_______________________________��
��4����ͼΪ����Ԫ�ص��⻯��a��b��c��d������������ʾ��ͼ��
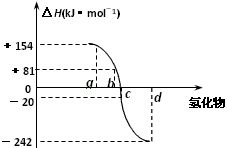
������ɣ��ǽ���Ԫ�ص��⻯����ȶ������⻯��������ȣ���H��֮��Ĺ�ϵ��_____________________________________��
5��ѡ���� ����NaOH 20.0 g��ϡ��Һ��������ϡ���ᷴӦ���ų�28.7 kJ������������ȷ��ʾ�÷�Ӧ�к��ȵ��Ȼ�ѧ����ʽ�� �� ��
A��NaOH +HCI
B��NaOH�� aq��+HC1�� aq��
C��NaOH��1��+HCl��1��
D��NaOH�� aq��+HCl�� aq��