1、填空题 CO2、SO2、NOx 是对环境影响较大的气体,控制和治理CO2、SO2、NOx 是解决温室效应、减少酸雨和光化学烟雾的有效途径。
(1)下列措施中,有利于降低大气中的CO2、SO2、NOx 浓度的有?(填字母)
a.减少化石燃料的使用,开发新能源
b.使用无氟冰箱,减少氟里昂排放
c.多步行或乘公交车,少用专车或私家车
d.将工业废气用碱液吸收后再排放
(2)为了降低汽车尾气对大气的污染,有关部门拟用甲醇替代作为公交车的燃料。写出用合成气(CO和H2)生产甲醇的化学方程式?,已知该反应合成1 mol液态甲醇吸收热量131.9 kJ, 2H2 (g) + CO(g) + 3/2O2g) =CO2 (g) +2H20 (g)?△H =-594.1 kJ・mol-1,请写出液态甲醇燃烧生成二氧化碳和水蒸气的热化学方程式??。
(3)有人设想以下图所示装置用电化学原理将CO2、SO2转化为重要化工原料。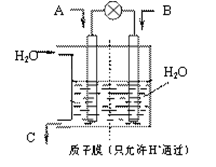
若A为CO2,B为H2,C为CH3OH,则通入CO2的一极为?极;若A为SO2,B为O2,C为H2SO4。则负极的电极反应式为??;
(4)①在研究氮的氧化物的转化时,某小组查阅到以下数据:17℃、1.01×105 Pa时,
2NO2(g) 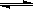 ?N2O4(g)?△H <0的平衡常数 K=13.3,则该条件下密闭容器中N2O4和NO2的混合气体达到平衡时,若 c (NO2) =" 0.0300" mol・L-1,
?N2O4(g)?△H <0的平衡常数 K=13.3,则该条件下密闭容器中N2O4和NO2的混合气体达到平衡时,若 c (NO2) =" 0.0300" mol・L-1,
c (N2O4)=??(保留两位有效数字);
②改变上述体系的某个条件,达到新的平衡后,测得混合气体中 c (NO2) =" 0.04" mol・L-1, c (N2O4) =" 0.007" mol・L-1,则改变的条件为?;
参考答案:(1)acd?(2分)
(2)CO+2 H2=CH3OH(2分)
2CH3OH(l) + 3O2(g) = 2CO2(g) + 4H2O(g)? ΔH =-1452 kJ・mol-1(3分)
(3)正(1分); SO2+2H 2O-2e― = SO42-+ 4H+ ?(2分);
(4)①0.012 mol・L-1?(2分)②升高温度(2分)
本题解析:(1)使用无氟冰箱,减少氟里昂排放,是抑制臭氧层破坏的,b不正确,其余都是正确的,答案选acd。
(2)根据已知的反应物和生成物可知,方程式为CO+2H2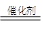 CH3OH。反应①CO(g)+2H2(g)
CH3OH。反应①CO(g)+2H2(g)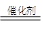 CH3OH(l)?△H =+131.9 kJ・mol-1,和反应②2H2 (g) + CO(g) + 3/2O2g) =CO2 (g) +2H20 (g)?△H =-594.1 kJ・mol-1,所以根据盖斯定律可知,(②-①)×2即得到 2CH3OH(l) + 3O2(g) = 2CO2(g) + 4H2O(g),所以反应热△H =(-594.1 kJ・mol-1-131.9 kJ・mol-1)×2=-1452 kJ・mol-1。
CH3OH(l)?△H =+131.9 kJ・mol-1,和反应②2H2 (g) + CO(g) + 3/2O2g) =CO2 (g) +2H20 (g)?△H =-594.1 kJ・mol-1,所以根据盖斯定律可知,(②-①)×2即得到 2CH3OH(l) + 3O2(g) = 2CO2(g) + 4H2O(g),所以反应热△H =(-594.1 kJ・mol-1-131.9 kJ・mol-1)×2=-1452 kJ・mol-1。
(3)在反应中碳元素的化合价降低,所以CO2是氧化剂,得到电子,因此CO2在正极通入。SO2失去电子,在负极通入,电极反应式为SO2+2H 2O-2e― = SO42-+ 4H+ 。
(4)①根据平衡常数表达式可知,c (N2O4)=13.3×0.03002=0.012 mol・L-1。
②此时平衡常数是0.007÷0.042=4.375,即平衡常数减小。由于正反应是放热反应,所以改变的条件是升高温度,平衡向逆反应方向移动。
本题难度:一般
2、选择题 一种由甲醇(CH3OH)和氧气以及氢氧化钠做电解质溶液的新型电池,其两极的电极反应式为: 2CH3 OH+16OH-
参考答案:
本题解析:
本题难度:困难
3、选择题 我国知名企业比亚迪公司开发了具有多项专利的锂钒氧化物二次电池,其成本较低,对环境无污染,能量密度远远高于其它材料电池,电池总反应为:V2O5+xLi  LixV2O5。下列说法中,正确的是?(?)
LixV2O5。下列说法中,正确的是?(?)
A.锂在放电时做正极材料,充电时为阳极材料
B.电池在放电时,Li+向负极移动
C.该电池充电时阳极的反应为:LixV2O5 -xe-=V2O5 + xLi+
D.V2O5只是锂发生反应的载体,不参与电池反应
参考答案:C
本题解析:放电时锂做负极,充电时锂是阴极,A错误;放电时,阳离子向正极移动,B错误;充电时阳极发生氧化反应,C正确;V2O5在反应中有化合价的变化,所以不能做反应的载体,D错误。答案选C。
点评:在原电池中较活泼的金属作负极,失去电子,发生氧化反应。电子经导线传递到正极上,所以溶液中的阳离子向正极移动,阴离子向负极移动。正极得到电子,发生还原反应,据此可以进行有关的判断。电解中最关键的是准确判断出电极上离子的放电顺序。在判断电解产物时,首先判断阳极电极材料。如果是活性电极,则电极本身失去电子。如果是惰性电极,则溶液中的阴离子失去电子。而阴极是溶液中的阳离子得到电子,所以需要熟练记住常见离子的放电顺序。
本题难度:简单
4、选择题 下列装置属于原电池的是( )
A.
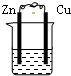
酒精
B.

CuCl2溶液
C.
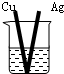
AgNO3溶液
D.

?稀硫酸? 稀硫酸
参考答案:A、乙醇不是电解质溶液且不能自发进行氧化还原反应,故A错误;
B、原电池必须有两个活泼性不同的电极,该装置两个电极材料相同,故A错误;
C、符合原电池的构成条件,故C正确;
D、没有形成闭合回路,故D错误.
故选C.
本题解析:
本题难度:简单
5、选择题 下列选项错误的是
[? ]
A.在NH4Cl晶体中含有离子键和共价键
B.设想把“H2+ Cl2=2HCl”设计成燃料电池,用于工业制盐酸,并进行发电
C.某反应△H >0,△S >0,该反应是个非自发反应
D.25℃时,NaNO2溶液的pH =8,c(Na+) -c(NO2-)= 9.9×10-7mol/L
参考答案:C
本题解析:
本题难度:一般