1、填空题 现有如下两个反应:
A、NaOH + HCl =" NaCl" + H2O
B、2FeCl3+Cu =2FeCl2+CuCl2
(1)根据两反应本质,判断能否设计成原电池:A、?, B、__________(选择“能”或“不能”);
(2)如果不能,说明其原因?
________________________________________________________________;
(3)如果可以,则写出正、负极材料、电极反应式及电解质溶液名称:
负极材料________,电极反应式为?,正极材料?,电极反应式为?,
电解质溶液名称是?。
参考答案:(1)(A)不能?(B)能?(2)(A)的反应为非氧化还原反应,没有电子转移
(3) 负极:铜,Cu-2e- =Cu2+,正极:碳棒,2Fe3+ +2e- = 2Fe2+ :氯化铁溶液
本题解析:(1)氧化还原反应中有电子的转移,所以只有氧化还原反应才能设计成原电池。A不是氧化还原反应,不能设计成原电池。B是氧化还原反应,可以设计成原电池。
(2)见(1)中的分析
(3)根据方程式可知,铜是还原剂失去电子。氯化铁是氧化剂,铁离子得到电子,所以根据原电池的工作原理可知,负极材料应该是铜,电极反应式是Cu-2e- =Cu2+。正极材料可以是金属性弱于铜的金属,也可以是能够导电的非金属,例如碳棒,电极反应式是2Fe3+ +2e- = 2Fe2+ 。而根据方程式可知电解质溶液应该是氯化铁溶液。
点评:该题是中等难度的试题,试题难易适中,注重基础知识的考查,侧重能力的培养和解题方法的指导,有利于培养学生的逻辑思维能力和创新思维能力,提高学生分析问题、特别是灵活运用基础知识解决实际问题的能力。该题的关键是明确原电池的工作原理。
本题难度:一般
2、填空题 (8分)如图所示的原电池中,回答下列问题
(1)负极材料
(2)写出电极反应式:正极: ;负极: 。
(3)写出电极反应总反应式
(4)电子由 极流向 极(填写Zn或Cu)
参考答案:(1)Zn (2分) (2)2H++2e-=H2 (1分) Zn-2e-=Zn2+ (1分)
Zn+2H+=Zn2++H2 (2分) (4)Zn Cu (2分)
本题解析:考查原电池的有关判断和应用。在原电池中较活泼的金属作负极,失去电子,发生氧化反应,所失去的电子经导线传递到正极上。锌比铜活泼,所以锌是负极,失去电子。铜是正极,溶液中的氢离子在正极得到电子,发生还原反应生成氢气。
本题难度:一般
3、选择题 氢氧燃料电池以 H2 为还原剂, O2为氧化剂,电极为多孔镍,电解液为 30% 的 KOH 溶液,下列有关叙述正确的是 ( )
①负极反应为 4OH-→O 2+ 2H 2 O+ 4 e-?
②负极反应为 H 2+ 2OH-→ 2H 2 O+ 2 e-?
③工作时正极区 pH 升高,负极区 pH 降低 ?
④工作时溶液中阴离子移向正极?
A.③④
B.②③
C.②④
D.①④
参考答案:B
本题解析:略
本题难度:简单
4、填空题 (7分)用导线将锌片、铜片连接后浸入稀硫酸溶液中,构成了原电池,此电池的负极是?,正极的电极反应式是?,负极的电极反应式是?,总电极反应式是?。
参考答案:(共7分)?Zn?1分,2H++2e-==H2 2分?Zn-2e-==Zn2+2分, Zn+2H+= Zn2+ + H2?2分
本题解析:略
本题难度:简单
5、填空题 (16分)(1)把一块纯净的锌片插入盛有稀硫酸的烧杯里,可观察到锌片逐渐溶解,并有气体产生,再平行地插入一块铜片(如图甲所示),可观察到铜片上?(填“有”或“没有”)气泡产生,再用导线把锌片和铜片连接起来(如图乙所示),可观察到铜片上(填“有”或“没有”)?气泡产生。
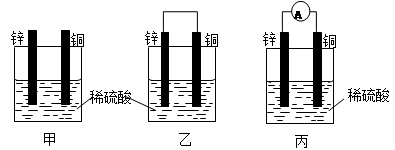
(2)用导线连接灵敏电流表的两端后,再与溶液中的锌片和铜片相连(如图丙所示),观察到灵敏电流表的指针发生了偏转,说明了导线中有电流通过。从上述现象中可以归纳出构成原电池的一些条件是??,
有关的电极反应式:锌片?;铜片?。
图丙所示原电池中,电子流向为?。
(3)图乙、图丙是一个将 ?能转化为 ?能的装置,人们把它叫做原电池。
参考答案:(1)没有(2分),有(2分);
(2)两电极要插入电解质溶液,并用导线连接形成回路?(2分)
Zn-2e-=Zn2+(2分),2H+ + 2e- =H2↑(2分),从锌通过导线流向铜(2分)
(3)化学(2分),电能(2分)
本题解析:考查原电池的应用及其判断。铜在金属活动顺序表中排在氢的后面,所以和稀硫酸不反应。当用导线和锌相连并插入稀硫酸中,则构成原电池,锌是负极,失去电子,发生氧化反应。铜是正极,电子经导线传递到正极,所以溶液中的阳离子向正极移动,即氢离子在正极得到电子,发生还原反应,生成氢气。电极反应式为负极:Zn-2e-=Zn2+;正极:2H+ + 2e- =H2↑。根据以上分析可知,构成原电池的条件是活泼性不同的金属或金属与非金属,导线相连,并且要插入电解质溶液中。原电池是把化学能转化为电能的装置。
本题难度:一般