1��ѡ���� X��Y��Z��R��W��5�ֶ�����Ԫ�أ�ԭ�����������������ǿ�������ӻ�����Z2Y���ۻ�����RY3��XW4����֪Y��Rͬ���壬Z��R��Wͬ���ڣ�����˵������ȷ���ǣ�������
A��ԭ�Ӱ뾶��Z��R��W
B��X2W6�����и�ԭ�Ӿ�����8���ӽṹ
C����̬�⻯��е㣺HmY��HnR
D��Y��Z��R����Ԫ����ɵĻ�����ˮ��Һһ���Լ���
�ο��𰸣����ӻ�����Z2Y��Z�Ļ��ϼ�Ϊ+1�ۣ�Y�Ļ��ϼ�Ϊ-2�ۣ��ֱ�Ϊ��A��͢�A��Ԫ�أ���֪Y��Rͬ���壬���γɹ��ۻ�����RY3����RΪSԪ�أ�YΪOԪ�أ�Z��R��Wͬ���ڣ���ZΪNaԪ�أ�X��Y��Z��R��W��5�ֶ�����Ԫ�أ�ԭ����������������W��ClԪ�أ�����XW4��֪XΪCԪ�أ�
A��ͬ����Ԫ�ش�����ԭ�Ӱ뾶��С��Z��R��Wͬ���ڣ��ֱ�ΪNa��S��Cl��ԭ��������������ԭ�Ӱ뾶��С����A��ȷ��
B��X2W6����ΪC2Cl6��ÿ��Cԭ���γ�4�����ۼ���Cԭ�����������8�����ȶ��ṹ��Cl�γ�1�����ۼ�������������ҲΪ8����B��ȷ��
C��HmYΪH2O������������е�ϸߣ�������̬�⻯��е㣺HmY��HnR����C��ȷ��
D��Y��Z��R����Ԫ����ɵĻ�������Na2SO3��Na2SO4�ȣ�����Һ�ֱ�ʼ��Ժ����ԣ���D����
��ѡD��
���������
�����Ѷȣ���
2������� ��ѡ��3�����ʽṹ�����ʡ���10�֣�
Ѫ�����к���C��O��N��Fe����Ԫ�ء��ش��������⣺
��1��C��N��O��H����Ԫ���е縺����С����?����Ԫ�ط��ϣ���д����̬Feԭ�ӵĺ�������Ų�ʽ?��
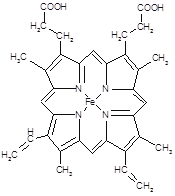
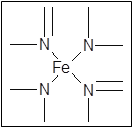
��2����ͼ��ʾΪѪ�쵰�ͼ��쵰�Ļ��Բ��֨D�DѪ���صĽṹʽ��Ѫ������Nԭ�ӵ��ӻ���ʽ��?������ͼ�ķ������á��������Fe2������λ����
 ?
?
��3��NiO��FeO�ľ���ṹ���;����Ȼ��Ƶ���ͬ��Ni2+��Fe2+�����Ӱ뾶�ֱ�Ϊ69 pm��78 pm�����۵�NiO ________ FeO(���������)��
��4��N��H�γɵĻ�������(N2H4)���������ȼ�ϣ�ȼ��ʱ�����ķ�Ӧ�ǣ�
2N2H4(l)+ N2O4(l)��3N2(g)+ 4H2O(g)?��H����1038.7kJ/mol
���÷�Ӧ����4mol N��H�����ѣ����γɵ�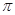 ����___________mol��
����___________mol��
��5�����ݵȵ���ԭ����д��CN���ĵ���ʽ?��1 mol O22+�к��еĦм���ĿΪ?��
��6�����Цġ��á�������ͬ������������ͼ��ʾ����þ��徧���������е���ԭ����Ϊ?���ġ������־�������ԭ�ӵ���λ��֮��Ϊ?��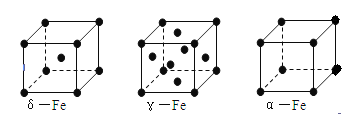
�ο��𰸣���1��H��[Ar]3d64S2?��2��sp2��sp3��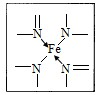 ��3����?��4��3
��3����?��4��3
��5��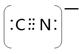 ��2NA?��6��4��4:3
��2NA?��6��4��4:3
�����������1��ͬ����Ԫ�ش�����Ԫ�صĵ縺�����������е縺��C��N��O��H�ĵ縺����С������ԭ��������26�����ݺ�������Ų����ɿ�֪����̬Feԭ�ӵĺ���۵����Ų�ʽΪ[Ar]3d64S2����2���γ�˫����Nԭ�ӿռ乹��Ϊƽ�棬����Ϊsp2�ӻ����γɵ�����Nԭ�ӣ���NH3�ӻ���ͬ����֪Ӧ����sp3�ӻ���Nԭ���������5�����ӣ�ֻ��Ҫ�γ�3�������ɴﵽ�ȶ��ṹ������ͼ���γ�˫����Nԭ���γ�������������Ȼ��һ��Ϊ��λ�����ɱ�ʾΪ ��
��
��3��NiO��FeO�ľ���ṹ���;����Ȼ��Ƶ���ͬ��˵�����߶������Ӿ��壬���Ӿ�����۵������Ӽ���ǿ���йأ��������������Խ�࣬���Ӱ뾶ԽС�����Ӽ�Խǿ���۵�Խ�ߣ�����Ni2+�����Ӱ뾶С��Fe2+�����Ӱ뾶�������۵���NiO��FeO��
��4��N2H4�к���4��N��H���������ݻ�ѧ����ʽ��֪������Ӧ����4mol N��H�����ѣ����Ȼ����1.5mol�����������к��е�������������������1���Ҽ���2��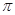 ������˷�Ӧ���γɵ�
������˷�Ӧ���γɵ�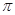 ����1.5mol��2��3mol��
����1.5mol��2��3mol��
��5���۵�������ԭ�����ֱ���ȵ��ǵȵ����壬CN-�뵪����Ϊ�ȵ����壬����ݵ������ӵĵ���ʽд��CN-�ĵ���ʽ����CN-�����ӣ��������ӵ���ʽ����д�������������ʽΪ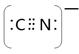 ��O22+�뵪��Ҳ��Ϊ�ȵ����壬��1 mol O22+�к��еĦм���ĿΪ2NA��
��O22+�뵪��Ҳ��Ϊ�ȵ����壬��1 mol O22+�к��еĦм���ĿΪ2NA��
��6���þ��徧���������е���ԭ����Ϊ8�� +6��
+6��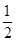 =4���ġ������־�������ԭ�ӵ���λ���ֱ�Ϊ8��6������λ��֮��Ϊ8��6=4��3��
=4���ġ������־�������ԭ�ӵ���λ���ֱ�Ϊ8��6������λ��֮��Ϊ8��6=4��3��
�����Ѷȣ�һ��
3��ѡ���� ����������NF3����һ����ɫ��ζ�����壬���ǰ���NH3���ͷ���F2����һ��������ֱ�ӷ�Ӧ�õ��ģ�4NH3��3F2��NF3��3NH4F �������й�NF3��������ȷ����
A��NF3�����ӻ������������
B��NF3�Ļ�ԭ�Ա�NH3ǿ
C��NF3�������Ա�F2ǿ��������
D��NF3�е�N�ʣ�3��
�ο��𰸣�D
���������NF3�ǹ��ۻ����A����ȷ��NF3�е�Ԫ�صĻ��ϼ��ǣ�3�ۣ��仹ԭ�Ա�NH3����B����ȷ�����ݷ���ʽ��֪��NF3������ԭ�����������Ա�F2����C����ȷ��������ȷ�Ĵ�ѡD��3���й��ж�
�������������е��Ѷȵ����⣬���������ǿ��ע�ػ���������������������ѵ��������������ѧ���������������ʹ���˼ά���������ѧ����Ӧ��������֪ʶ��Ǩ��������
�����Ѷȣ�һ��
4��ѡ���� ���������У�ֻ�������Ӽ��Ļ������ǣ�������
A��NaOH
B��MgCl2
C��KBr
D��H2O
�ο��𰸣�BC
���������
�����Ѷȣ���
5��ѡ���� ���е���ʽ�д�����ǣ�������
A��

B��
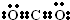
C��

D��

�ο��𰸣�C
���������
�����Ѷȣ�һ��