1、选择题 20℃时,饱和KCl溶液的密度为1.174 g・cm-3,物质的量浓度为4.0 mol・L-1,则下列说法中不正确的是
A.20℃时,饱和KCl溶液与等质量的水混合后物质的量浓度大于2.0 mol・L-1
B.20℃时,将29.8 gKCl溶于87.6 g水中可得饱和溶液
C.20℃时,密度小于1.174 g・cm-3的KCl溶液是不饱和溶液
D.将此溶液蒸发部分水,再恢复到20℃时,溶液中各离子的浓度不变
参考答案:A
本题解析:饱和KCl溶液与等质量的水混合后,水的密度小于氯化钾溶液,所以体积大于氯化钾溶液,所以混合后物质的量浓度小于2.0 mol・L-1A错。根据公式ω=Mc/1000ρ即可求出B对,对于氯化钾溶液密度与质量分数成正比,所以C正确。D蒸发部分水有晶体析出,剩下溶液在该温度下仍然是饱和溶液,所以咯离子的浓度不变,答案D正确。
本题难度:一般
2、选择题 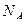 表示阿伏加德罗常数。下列说法正确的是
表示阿伏加德罗常数。下列说法正确的是
A.7.8gNa2O2中含有的阴离子数目为0.2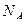
B.标准状况下,2.24 L CHCl3的分子数为0.1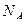
C.1 L 0.1mol/L Al2(SO4)3溶液中,Al3+的数目为0.2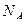
D.9.2g NO2和N2O4的混合气体中含有的氮原子数为0.2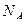
参考答案:D
本题解析:略
本题难度:简单
3、选择题 假设R元素无同位素,元素R原子的质量数为A,Rm-的核外电子数为x,则W g Rm-离子所含中子的物质的量为
A.(A-x+m)mol
B.(A-x-m)mol
C.W/A(A-x+m)mol
D.W/A(A-x-m)mol
参考答案:C
本题解析:Rm-的核外电子数为x,则R的原子序数是x-m。因此R的中子数是a-x+m,所以W g Rm-离子所含中子的物质的量为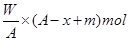 ,答案选C。
,答案选C。
点评:在计算有关原子的组成时,需要掌握几个关系式,即质子数+中子数=质量数、质子数=核外电子数=原子序数=核电荷数。
本题难度:一般
4、选择题 比较1 mol N2和1 mol CO的下列物理量:①质量②分子总数③原子总数,其中相同的是
A.①
B.①②
C.①②③
D.②③
参考答案:C
本题解析:N2和CO的相对分子质量为28,所以1 mol N2和1 mol CO的①质量②分子总数③原子总数,均相同。选C。
本题难度:一般
5、选择题 下列溶液中与100mL0.1mol/L(NH4)2SO4溶液中NH4+离子浓度相同的是
A.10mL 1mol/L (NH4)2SO4溶液
B.50mL 0.2mol/L NH4Cl溶液
C.10mL 0.2mol/L (NH4)2SO4溶液
D.200mL 0.1mol/L NH4NO3溶液