| �߿�ʡ������ | |
|
|
| �߿�ʡ������ | |
|
|
|
���л�ѧ֪ʶ�㽲�⡶�����Ļ�ѧ��Դ����Ƶ����Ԥ�⣨2017�����°棩(��)
�ο��𰸣�D ���������ԭ��صĸ���ʧ���ӣ�����������Ӧ�������õ��ӣ�������ԭ��Ӧ���ݴ˴��� �����Ѷȣ�һ�� 2��ѡ���� �����ڵ綯��������--����ȼ�ϵ�أ�ͨ����NaCl��Һ��NaOH��ҺΪ���Һ�����Ͻ�Ϊ�����������缫Ϊ����������˵����ȷ���� �ο��𰸣�A ��������� �����Ѷȣ�һ�� 3��ѡ���� һ�����������Ҵ�����û������������ܼ����ȼ״����Ч�ʸ߳�32������ط�ӦʽΪC2H5OH+3O2=2CO2+3H2O����ع�����ͼ�����й��ڸõ�ص�˵������ȷ���� |
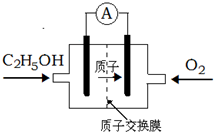
�ο��𰸣�A����ع���ʱ����Դ�ڲ��������ӴӸ�������������Ǩ�ƣ�����H+�Ӹ�������������Ǩ�ƣ���A����
B��ȼ�ϵ���У�ȼ���ڸ���ʧ���ӣ�����ͨ���Ҵ��ĵ缫�Ǹ�������B��ȷ��
C�����������õ����ӱ���ԭ���缫��ӦʽΪ4H++O2+4e-�T2H2O����C��ȷ��
D��ÿ����0.2molC2H5OHת��2.4mol���ӣ����Ե缫��ⱥ��NaCl��ˮ��Һ������������������1molH2ת��2mol���ӣ�����ת��2.4mol����ʱ��������Ϊ1.2mol�������������Ϊ26.88L����D��ȷ��
��ѡA��
���������
�����Ѷȣ�һ��
4������� ���ԭ���ڻ�ѧ��ҵ���й㷺Ӧ�á���ͼ��ʾһ�����أ�װ�е��Һa��X��Y������缫�壬ͨ��������ֱ����Դ��������ش��������⣺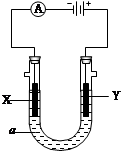
��1��X��Y���Ƕ��Ե缫��a�DZ���NaCl��Һ��ʵ�鿪ʼʱͬʱ�����߸����뼸�η�̪��Һ����
�ٵ�����X���ϵĵ缫��ӦʽΪ ��
��X�������۲쵽�������� ����
��Y�缫�ϵĵ缫��ӦʽΪ ��
����õ缫��Ӧ����ķ����� ��
���ܷ�Ӧ�Ļ�ѧ����ʽ ��
��2��X��Y���Ƕ��Ե缫�����CuSO4��Һ������·��ͨ��0.4mol ����ʱ������ͭ��ͬʱ����һ���缫�ɵ� L O2 (��״����)
�ο��𰸣�(1)�� 2H+ + 2e_�� H2�� �缫���������ݲ������缫��������Һ�ʺ�ɫ
��2Cl-��2e- ��Cl2���������Ӽг�ʪ��ĵ���KI��ֽ����Y�缫�����ڣ�����ֽ�����������ΪCI2��
��2NaCl��2H2O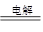 2NaOH��H2����Cl2�� (��) 2.24L
2NaOH��H2����Cl2�� (��) 2.24L
�����������1���ٸ���װ��ͼ��֪��X�͵�Դ�ĸ�����������X����������Һ�е������ӷŵ磬����X�缫�ĵ缫��Ӧʽ��2H+ + 2e_�� H2���������ӷŵ磬�ƻ���������Χˮ�ĵ���ƽ�⣬�Ӷ�ʹ������Χ��Һ�Լ��ԣ���ʵ�������ǵ缫���������ݲ������缫��������Һ�ʺ�ɫ��
��Y�缫����������Һ�е�Cl-�ŵ磬��Y�缫�ϵĵ缫��ӦʽΪ2Cl-��2e- ��Cl2�����������������ԣ���ʹʪ��ĵ���KI��ֽ�������ݴ˿��Լ����������������Ӽг�ʪ��ĵ���KI��ֽ����Y�缫�����ڣ�����ֽ�����������ΪCI2��
���ܷ�Ӧ�Ļ�ѧ����ʽΪ2NaCl��2H2O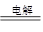 2NaOH��H2����Cl2����
2NaOH��H2����Cl2����
��2��OH���ŵ�ĵ缫��Ӧʽ��4OH����4e��=2H2O��O2��������ݵ��ӵĵ�ʧ�غ��֪���������������ʵ�����0.1mol���ڱ�״���µ������2.24L��
���㣺������ԭ��Ӧ�õ��й��ж��Լ��缫��Ӧʽ����д�ͼ���
�����������Ǹ߿��еij������ͣ������е��Ѷȵ����⡣���������ǿ�����ض�ѧ�������������ͽ��ⷽ����ָ����ѵ��������������ѧ���������������淶�Ĵ�������������Ĺؼ�����ȷ���صĹ���ԭ����Ȼ��������������ü��ɡ�
�����Ѷȣ�һ��
5��ѡ���� ij������ȼ�ϵ����CsHSO4����Ϊ����ʴ���H+��������ṹ����ͼ������ܷ�Ӧ�ɱ�ʾΪ��
2H2��O2===2H2O�������й�˵����ȷ����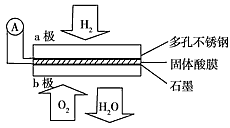
[? ]
A. ����ͨ�����·��b������a��
B. b���ϵĵ缫��ӦʽΪ��O2��2H2O��4e-===4OH-
C. ÿת��0.1 mol���ӣ�����1.12 L��H2
D. H+��a��ͨ�����������ʴ��ݵ�b��
�ο��𰸣�D
���������
�����Ѷȣ�һ��
| ���� �� С������ӡ�� �������� ���ر��� �����ض����� | |
| ��һƪ�����л�ѧ֪ʶ���ȫ�����仯��.. | |
| �����Ŀ |