1、选择题 下列说法正确的是(? )
A.20983Bi和 21083Bi的核外电子数不同
B.NH3的电子式为: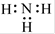
C.全部由非金属元素组成的化合物可能含离子键
D.离子化合物不可能含共价键
参考答案:C
本题解析:20983Bi?和 ?21083Bi属于同位素关系,质子数相同,核外电子数等于质子数,所以二者相同,A错误;氨气的电子式正确的是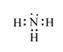 ,B错误;全部由非金属组成的化合物可能含离子键如铵盐:NH4Cl、(NH4)2SO4 等是离子化合物,C正确;离子化合物是指含有离子键的化合物,可以含有共价键,D错误。故选C。
,B错误;全部由非金属组成的化合物可能含离子键如铵盐:NH4Cl、(NH4)2SO4 等是离子化合物,C正确;离子化合物是指含有离子键的化合物,可以含有共价键,D错误。故选C。
本题难度:一般
2、选择题 关于114号元素的预测中,正确的是(?)
A.其单质是良好的半导体材料
B.+2价比+4价稳定
C.原子有6个电子层,最外电子层上有 4 个电子
D.有+2、+3、+4价
参考答案:B
本题解析:略
本题难度:简单
3、选择题 在元素周期表中短周期的X和Y两种元素可组成化合物XY3,则下列说法正确的是
A.XY3晶体一定是分子晶体
B.XY3中各原子的最外层一定满足8电子的稳定结构
C.X和Y一定不属于同一主族
D.Y原子序数为m,X原子序数可能是m±4或m+6 或m+8等
参考答案:D
本题解析:
正确答案:D
A、可能是离子化合物,如AlF3;B不正确,AlCl3中铝不是8电子的稳定结构,C、SO3中O、S在同一族。
本题难度:一般
4、选择题 X、Y、Z、R、W是5种短周期元素,原子序数依次增大;它们可组成离子化合物Z2Y和共价化合物RY3、XW4;已知Y、R同主族, Z、R 、W同周期。下列说法错误的是(? )
A.原子半径:Z>R>W
B.气态氢化物稳定性:HmW>HnR
C.XW4分子中各原子均满足8电子结构
D.Y、Z、R三种元素组成的化合物水溶液一定显碱性
参考答案:D
本题解析:Y、R同主族且能形成共价化合物RY3,所以Y是氧,R是硫。Z2Y为离子化合物,Z属于第三周期,所以Z是钠。XW4是共价化合物,且W的原子序数大于硫的,所以W是氯,X是碳。同周期自左向右原子半径逐渐减小,非金属性逐渐增强,A正确。非金属性越强,氢化物的稳定性越强,B?正确。CCl4的电子式为 ,所以各原子均满足8电子结构,C正确。Y、Z、R三种元素组成的化合物如果是硫酸钠,则溶液显中性,即D是错误的。答案选D。
,所以各原子均满足8电子结构,C正确。Y、Z、R三种元素组成的化合物如果是硫酸钠,则溶液显中性,即D是错误的。答案选D。
本题难度:一般
5、选择题 下列有关结构和性质的说法中不正确的是 ( )
A.元素周期表中从ⅢB族到ⅡB族十个纵行的元素都是金属元素
B.碱性:NaOH > NH3・H2O ,所以元素的金属性:Na > N
C.同周期第ⅡA族与第ⅢA族的元素原子序数之差不一定为1
D.第ⅦA族元素从上到下,其氢化物的稳定性逐渐减弱
参考答案:B
本题解析:A、正确;B、比较金属性强弱的依据是:最高价氧化物对应水化物的碱性强弱。而NH3・H2O不是氮元素的最高价氧化物对应水化物,故B错误;C、原子序数只差可能为1、11、25;D、从上到下,非金属性逐渐减弱,其氢化物的稳定性减弱。
本题难度:一般