1、选择题 关于图中各装置的叙述不正确的是( )
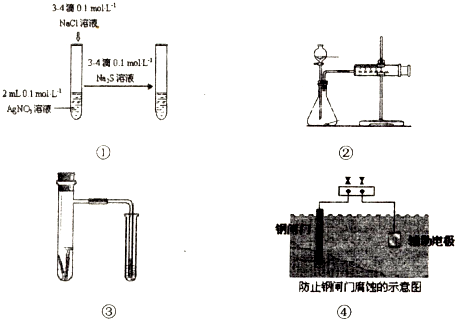
A.装置①能验证AgCl沉淀可转化为溶解度更小的Ag2S沉淀
B.装置②能测量锌与硫酸的反应速率
C.装置③能验证铁的吸氧腐蚀
D.装置④的X电极是负极,则能验证外接电源的阴极保护法
参考答案:A.硝酸银过量,可与硫化钠反应生成硫化银沉淀,不能证明AgCl沉淀可转化为溶解度更小的Ag2S沉淀,如要证明,应在AgCl饱和溶液中加入硫化钠,故A错误;
B.装置②能测量锌与硫酸的反应速率,故B正确;
C.吸氧腐蚀消耗氧气,具支试管内压强减少,小试管液面上升,故C正确;
D.装置③为外加电源的阴极保护法,钢闸门与外接电源的负极相连,电源提供电子而防止铁被氧化,故D正确;
故选A.
本题解析:
本题难度:简单
2、选择题 下表中的实验操作能达到实验目的或能得出相应结论的是
选项
| 实验操作
| 实验目的或结论
|
A
| 向盛有1mL 0.01mol・L-1AgNO3溶液的试管中滴加5滴0.01mol・L-1NaCl溶液,有白色沉淀生成,再向其中滴加 0.01mol・L-1NaI溶液,产生黄色沉淀。
| 常温下,
Ksp(AgCl)>Ksp(AgI)
|
B
| 取少量 KClO3晶体溶于适量的蒸馏水,再加入硝酸酸化的AgNO3溶液。
| 检验KClO3中的氯元素
|
C
| 向某溶液中滴加Ba(NO3)2溶液产生白色沉淀,再加稀盐酸沉淀消失。
| 说明原溶液中一定含有CO32-或 SO32-
|
D
| 将混有Ca(OH)2杂质的Mg(OH)2样品,放入水中搅拌成浆状后,加入足量饱和氯化镁溶液充分搅拌、过滤,沉淀用蒸馏水洗涤。
| 除去Mg(OH)2样品中的Ca(OH)2
|
?
参考答案:D
本题解析:A项中,当加入NaI后溶液中的c(Ag+)c(I-)>Ksp(AgI),就会有黄色沉淀出现,不能确定Ksp(AgCl)>Ksp(AgI)是否成立;B项中,硝酸酸化的AgNO3溶液用来检验Cl-,而不是ClO3-离子,不正确;C项中,若原溶液中是SO32-,加Ba(NO3)2溶液后产生BaSO3沉淀,再加入盐酸,H+和NO3-会将SO32-氧化为SO42-,变为BaSO4而沉淀不消失,不正确;
本题难度:一般
3、选择题 常温下,Ksp(CaSO4)=9×10-6,CaSO4在水中的沉淀溶解平衡曲线见图。下列说法正确的是

[? ]
A.温度升高,化学平衡常数K、电离常数Ka、难溶电解质的 溶度积常数Ksp均增大
B.a点对应的Ksp等于c点对应的Ksp
C.b点将有沉淀生成,平衡后溶液中c(SO42-)等于3×10-3 mol/L
D.d点溶液通过蒸发可以变到c点
参考答案:B
本题解析:
本题难度:一般
4、计算题 一定温度下,测得某纯水的pH为6.5。试计算:
(1)此时水的离子积常数Kw为多少?
(2)若在此纯水中加一定量Ba(OH)2固体,配制成0.005mol・L-1。的Ba(OH)2溶液,保持原温度,其溶液的pH为多少?
(3)取上述Ba(OH)2溶液200mL,加入含0.01mol 的浓溶液,待反应完全后,上层清液中Ba2+浓度变为多少?[体积变化忽略不计,Ksp(BaSO4)=1.08×10-10]
的浓溶液,待反应完全后,上层清液中Ba2+浓度变为多少?[体积变化忽略不计,Ksp(BaSO4)=1.08×10-10]
参考答案:(1)Kw=10-13
(2)pH=1
(3)
本题解析:
本题难度:一般
5、选择题 已知t℃时,Ksp[Al(OH)3]=l×l0-33,Ksp[Mg(OH)2]=4×10-12。在含有0.20 mol/L H+且c(Mg2+)=c(A13+)=0.10mol/L的溶液中不断加入KOH溶液,沉淀的质量m(沉淀)与加入KOH溶液的体积V[KOH(aq)]关系的示意图正确的是(? )
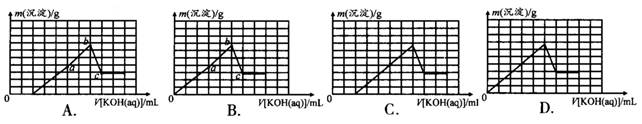
参考答案:A
本题解析:B、D图像起点错误,根据题意加入的OH-先后分别与H+、Al3+、Mg2+反应,当Mg2+完全沉淀为Mg(OH)2时,过量的OH-再溶解Al(OH)3沉淀。溶液中H+几乎反应完,根据每消耗1 molOH-生成Al(OH)3和Mg(OH)2的质量分别为26 g和29 g,因此两条直线的斜率不同,生成Al(OH)3的斜率小些,生成Mg(OH)2的斜率较大。
本题难度:一般