1��ѡ���� ��ʢ��Cl2����������ƿ�ס��ҡ����������졢���и�ע������Һ���е�һ�֣���������������ͼ��ʾ����ס��ҡ����������졢��ע���Һ��ֱ���
��AgNO3��Һ����NaOH��Һ����ˮ���ܵ���-KI��Һ����FeCl2��KSCN���Һ����NaBr��Һ
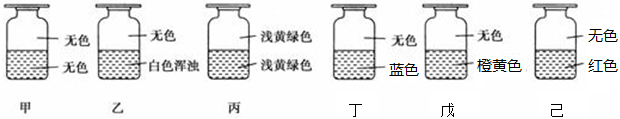
A���ܢ٢ڢޢݢ�
B���ޢ٢ۢܢڢ�
C���ޢۢڢܢ٢�
D���ڢ٢ۢܢޢ�
2��ѡ���� ��ѧ��Ӧ�У���ʱ���ڡ�һ�����ʹ�������һ�������Բ�����ȫ��Ӧ����������������з�Ӧ�����������������?�ٹ�����п��18 mol��L��1�����ᷴӦ���ڹ��������������������ڴ��������³�ַ�Ӧ����Ũ�����������MnO2��Ӧ���ܹ���ͭ��Ũ���ᷴӦ���ݹ���ϡ����������Ӧ������ϡ�������״ʯ��ʯ��Ӧ
A���ڢۢܢ�
B���ڢۢ�
C���٢ܢ�
D���٢ڢۢܢݢ�
3��ѡ���� ���л�ѧʵ����ʵ������۶���ȷ���ǣ�?��
ѡ��
| ʵ����ʵ
| ����
|
A
| ��SO2ͨ�뺬HClO����Һ������H2SO4
| HClO�����Ա�H2SO4ǿ
|
B
| �����ھƾ��ƻ����ϼ����ۻ���������
| ���������������۵������
|
C
| ϡ��Ũ����ֱ���ͭ��Ӧ����ԭ����ֱ�ΪNO��NO2
| ϡ���������Ա�Ũ����ǿ
|
D
| ��SO2ͨ����ˮ�У���ˮ��ɫ
| SO2����Ư����
4��ʵ���� (16��)������һ����Ҫ�Ļ���ԭ�ϣ��ڹ�ũҵ������������������Ҫ��Ӧ�á����������ѧ֪ʶ�ش��������⣺
I��������ͨ�뺬���۵⻯�ص���Һ�У��ɹ۲쵽�������ǣ�??��
˵���ȵ��ʵ�������?�ⵥ�ʵ������ԡ��������������
��ij��ѧ��ȤС��ƻ�������������������ȡ��������Һ��
(1)�䷴Ӧԭ��Ϊ��(�����ӷ���ʽ��ʾ)?��
(2)ʵ�������ƺ�4.0 mol��L-1��NaOH��Һ��������Һ��Ҫ?L�������״����2.24 L����ǡ����ȫ��Ӧ��
(3)����250 mL 4.0mol��L-1NaOH��Һ��ʵ�鲽�裺
a��������Ҫ�������ƹ����������
b�������������ƹ��塣
c�����ձ��е���Һע������ƿ��������������ˮϴ���ձ��ڱ�2��3�Σ�ϴ��ҺҲע��250 mL����ƿ��
d������������ˮ�ܽ�����õ��������ƹ��壬��ȴ��
e���Ǻ�ƿ�����������µߵ���ҡ�ȡ�
f������������ƿ�м�����ˮ���̶�����1~2cmʱ�����ý�ͷ�ιܼ�����ˮ����Һ�����Һ����̶������С�
������������������ƹ����������?��
�������������ȷ����˳����?��
������ʵ����Ҫ�������У���ƽ��ҩ�ס��ձ�����������??��?��
5��ѡ���� ��HCl����ͨ�뵽����ʳ��ˮ�лᷢ���ı仯��
A����Һ������ǿ
B��������������������
C���������
D������������
|