1、简答题 实验题:
某化学兴趣小组做了如下三个实验:
实验A:集气瓶中放青色、未熟的水果(蔬菜),盖上玻璃片;
实验B:集气瓶中放青色、未熟的水果(蔬菜),通入一定量的乙烯;
实验C:集气瓶中放青色、未熟的水果(蔬菜),瓶底放少量KMnO4固体,盖上玻璃片.
请根据所学化学知识完成下列问题:
(1)预期实验结果:水果成熟的先后顺序是______(用序号填写)
(2)解释你的预期结果的原因______.
为探究?Na、Mg、Al的金属活动性顺序,某课外小组同学进行了如下实验:
| 实验步骤 | 1将一小块金属钠放入滴有酚酞溶液的冷水中;
2将一小段用砂纸打磨后的镁带放入试管中,加入少量水,加热至水沸腾,冷却后,向试管中滴加酚酞溶液;
3将一小段镁带投入稀盐酸中;
4将一小片铝投入稀盐酸中.
实验现象
A剧烈反应,迅速生成大量的气体
B浮在水面上,熔成小球,不断游动,小球渐小最终消失,溶液变红
C反应不剧烈,产生无色气体
D有气体产生,溶液变成红色
|
(1)请在下表中填写与实验步骤对应的实验现象序号:
(2)请写出钠与水反应的方程式______.
(3)请你补充该小组同学用原子结构理论对上述实验结论的解释:
同周期元素从左到右核电荷数逐渐增多,原子半径逐渐______,失电子能力逐渐______,因此______性逐渐减弱.
参考答案:I、(1)乙烯可以做水果催熟剂,而高锰酸钾固体能和乙烯反应,故答案为:BAC;
(2)乙烯可以做水果催熟剂,而高锰酸钾固体能和乙烯反应,因此B中水果最先熟,而C中水果最后熟,
故答案为:乙烯可以做水果催熟剂,而高锰酸钾固体能和乙烯反应,因此B中水果最先熟,而C中水果最后熟;
II:(1)金属钠、镁、铝位于同一周期,按照从左到右的顺序失电子能力逐渐减小,和水及酸反应置换出氢气的程度是越来越难,和水以及酸反应的现象可以根据此来回答,故答案为:实验步骤1234实验现象BDAC(2)金属钠和水反应生成氢氧化钠和氢气,即2Na+2H2O=2Na++2OH-+H2↑,故答案为:2Na+2H2O=2Na++2OH-+H2↑;
(3)同周期元素从左到右核电荷数逐渐增多,原子半径逐渐减小,失电子能力逐渐减弱,金属性逐渐减弱,故答案为:减小,减弱,金属.
本题解析:
本题难度:一般
2、推断题 现有A、B、C、D、E、F六种常见的短周期主族元素,原子序数依次递增,原子半径A<D<C<B<F<E,B、C、D、E、F的简单离子的电子数为10,且原子的最外层电子数的关系为A+D=B+F=8;已知HNO2为弱酸,NaNO2具有下列性质: 2NO2-+2I-+4H+=2NO+I2+2H2O;2MnO4-+5NO2+6H+=2Mn2++5NO3-+3H2O请回答:
(1)B与E可形成离子化合物E3B,试写出它的电子式:_______________。
(2)已知B2A4与BA3具有相似的性质,B2A4通过炽热的氧化铜粉末,粉末由黑色变为红色,且产物对大气无污染,其化学反应方程式:_____________________。
(3)在常温下,A、B、C三种元素形成的两种常见PH均为5的强电解质溶液G和H,且水电离出的氢离子浓度比值为最大,则G、H的化学式分别为___________、___________G和H溶液中由水电离出的氢离子浓度比值为_________________。
(4)①已知A、B、C三种元素组成的一种离子化合物B2A4C2,其溶液显酸性,原因为________________________。(用文字说明原因)
②A、B、C三种元素组成的另一种离子化合物B2A4C3,其水溶液也显酸性,设计一个实验方案鉴别以上两种离子化合物___________________。
参考答案:(1)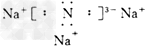
(2)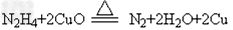
(3)NH4NO3、HNO3;104?
(4)①NH4+的水解程度大于NO2-的水解程度;②取少量两种溶液,分别滴加稀硫酸加热,产生红棕色气体的为NH4NO2,取?少量两种溶液,分别滴加酸性高锰酸钾溶液,紫色褪去的为NH4NO2
本题解析:
本题难度:一般
3、选择题 砹是核电荷数最大的卤族元素,推测砹及其化合物最不可能具有的性质是
A.HAt很不稳定
B.砹是白色固体
C.AgAt不溶于水
D.砹易溶于某些有机溶剂
参考答案:B
本题解析:根据递变规律推断,氢化物稳定性减弱,AgCl、AgBr、AgI都不溶,所以AgAt也不溶,Br2、I2能被苯、汽油、四氯化碳等有机溶剂萃取,则砹也能,颜色逐渐加深,所以砹不能为白色.
本题难度:一般
4、推断题 有原子序数不大于18,原子序数依次递增的A,B,C,D 4种元素,A,C两种元素的电子层数相同,A和C形成化合物AC,D和A形成化合物AD,9gB与足量的稀盐酸反应,可生成标准状况下的11.2 L H2,且向所得溶液中加入NaOH,可观察到先有沉淀生成,继续加入NaOH,沉淀溶解。
(1)写出这4种元素的名称和符号。_______________________
(2)写出这4种元素最高价氧化物对应水化物的化学式,分析其酸碱性的变化情况。
_________________________
参考答案:(1)(A)镁、(Mg)、(B)铝(A1)、(C)硫(S)、(D)氯(Cl)
(2)5种元素的氧化物对应水化物按碱性逐渐减弱,酸性逐渐增强的排列顺序如下:Mg(OH)2、Al(OH)3、
H2SO4、HClO4
本题解析:
本题难度:一般
5、选择题 现有4种短周期元素的有关信息如下表所示:则甲、乙、丙、丁四种元素的原子序数从大大小排列的是

[? ]
A.甲、乙、丙、丁
B.丁、甲、乙、丙
C.丙、丁、甲、乙
D.乙、甲、丁、丙
参考答案:D
本题解析:
本题难度:简单