1、判断题 将一块钠用小刀切开,暴露在空气中,可以观察到如下现象:
(1)金属钠表面变暗。
(2)过一会又变潮湿,同时使用放大镜观察,发现多处有小气泡生成。
(3)再过较长时间又转变为白色晶体。
(4)白色晶体最终变成白色粉末。
试写出上述反应现象的有关化学方程式。
参考答案:(1)4Na+O2 2Na2O
2Na2O
(2)Na2O+H2O 2NaOH
2NaOH
2H2O+2Na2 NaOH+H2↑
NaOH+H2↑
(3)2NaOH+CO2+9H2O Na2CO3・10H2O
Na2CO3・10H2O
(4)Na2CO3・10H2O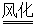 Na2CO3+10H2O
Na2CO3+10H2O
本题解析:钠表面变暗,是因为钠与空气中的氧气反应生成氧化钠。氧化钠易与空气中的水反应生成氢氧化钠,而氢氧化钠易与空气中的CO2反应生成Na2CO3和H2O;由于钠与水接触反应,生成的氢气从溶液中逸出而形成许多小气泡。NaOH溶液易吸收空气中的二氧化碳生成碳酸钠,碳酸钠在水溶液中以Na2CO3・10H2O形式结晶析出。由于Na2CO3・10H2O在干燥空气中易风化,故再过一段时间,Na2CO3・10H2O失去结晶水变为粉末状碳酸钠。
本题难度:简单
2、选择题 下列叙述正确的是( )
①Na2O与Na2O2都能和水反应生成碱,它们都是碱性氧化物
②Na2CO3溶液和NaHCO3溶液都能跟CaCl2溶液反应得到白色沉淀
③钠在常温下不容易被氧化
④Na2O2可作供氧剂,而Na2O不行
⑤Cu与HNO3溶液反应,由于HNO3浓度不同可发生不同的氧化还原反应
A.都正确
B.②③④⑤
C.②③⑤
D.④⑤
参考答案:D
本题解析:①错,碱性氧化是指与酸反应生成盐和水的氧化物,Na2O是碱性氧化物,则Na2O2与酸反应除了生成盐外还要生成氧气,不属于碱性氧化物;②错,NaHCO3溶液不能跟CaCl2溶液反应得到白色沉淀;③错,钠在常温下容易被氧化;④⑤正确;
本题难度:一般
3、计算题 在长期载人太空飞行的宇航器中,每个宇航员平均每天需要消耗0.9 kg氧气,呼出1.0 kg二氧化碳,为了能保持飞船座舱内空气成分的稳定,宇航科学家进行了大量的科学探索。有的科学家设计出“金属过氧化物处理系统”,即不断把座舱内的空气通入盛有金属过氧化物(以过氧化钠为例)的容器,并把处理后的气体充入座舱。有关反应的化学方程式是:①____________________________________;②______________________________________。
将处理后的气体充入座舱时,应注意采取的一项措施是_______________________。有人提出的用超氧化钾代替过氧化钠供氧,预计其优点是___________________。
参考答案:Na2O2的质量是3.9 g,Na2O的质量是3.1 g。
本题解析:H2SO4+? 2NaOH====Na2SO4+2H2O
98? 80
200 g×4.9%? m(NaOH)
m(NaOH)="8" g
设有Na2O2和Na2O的质量分别为x、y
2Na2O2+2H2O====4NaOH+O2↑
156? 160
x? m1(NaOH)
m1(NaOH)=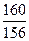 ?x
?x
Na2O+H2O====2NaOH
62? 80
y? m2(NaOH)
m2(NaOH)=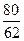 y
y

本题难度:简单
4、选择题 关于钠的性质,下列叙述不正确的是(?)
A.钠是软金属,新切面易失去金属光泽并变灰暗
B.极易与水反应,因为它的氧化性很强
C.钠与硫化合时很剧烈,甚至会发生微爆声
D.实验室常将金属钠保存在煤油中
参考答案:B
本题解析:钠原子最外层只有1个电子,极易失去,表现出非常强的还原性,化学性质非常活泼。通常情况下,既可与某些非金属(如氧气、氯气、硫等),又可与某些化合物(如水、酸、盐等)发生剧烈反应,有的甚至发生爆炸。A正确,碱金属都很软,可用刀切,切面易被氧气氧化失去金属光泽并变灰暗。B不正确,钠与水反应实质是钠失去电子体现还原性。C正确。D正确,因为钠的密度比煤油的大,故保存在煤油中可以达到与空气隔绝的目的。
本题难度:简单
5、选择题 将少量的金属钠放入盛有CuSO4溶液的烧杯中,剧烈反应,则烧杯中发生的反应是(?)
①2Na+CuSO4====Na2SO4+Cu ?②Cu+2H2O====Cu(OH)2↓+H2↑
③2Na+2H2O====2NaOH+H2↑?④2NaOH+CuSO4====Cu(OH)2↓+Na2SO4
A.①
B.①②
C.③④
D.①③
参考答案:C
本题解析:金属钠投到任何盐溶液中,首先是Na先与水反应生成H2和NaOH,而不可能是Na与金属阳离子间反应。
本题难度:简单