| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学必考知识点《盐类水解的原理》试题强化练习(2017年最新版)(八)
参考答案:A 本题解析:根据电荷守恒可知,2c(SO42-)+c(OH-)=c(NH4+)+c(H+)。所以如果溶液中c(NH4+)=2c(SO42-)时,c(OH-)=c(H+),即溶液显中性,答案选A。 本题难度:一般 3、填空题 下表中列出五种短周期元素A、B、C、D、E的信息,请推断后回答:
参考答案: 本题解析: 本题难度:困难 4、选择题 常温下,稀释0.1 mol・L-1Na2CO3溶液,图中的纵坐标可以表示 |
参考答案:C
本题解析:碳酸钠溶于水CO32-水解CO32-+H2O HCO3-+OH-,HCO3-+H2O
HCO3-+OH-,HCO3-+H2O H2CO3+OH-。稀释促进水解。根据图像可知,随着水的加入,纵坐标是增加的。A、水解平衡常数只与温度有关系,因此稀释过程中水解平衡常数不变,A不正确;B、稀释促进水解,溶液中OH-个数增加,但OH-浓度降低,因此溶液的pH减小,B不正确;C、稀释促进水解,HCO3-的浓度减小,但HCO3-个数增加,C正确;、稀释促进水解,c(CO32-)减小,D不正确,答案选C。
H2CO3+OH-。稀释促进水解。根据图像可知,随着水的加入,纵坐标是增加的。A、水解平衡常数只与温度有关系,因此稀释过程中水解平衡常数不变,A不正确;B、稀释促进水解,溶液中OH-个数增加,但OH-浓度降低,因此溶液的pH减小,B不正确;C、稀释促进水解,HCO3-的浓度减小,但HCO3-个数增加,C正确;、稀释促进水解,c(CO32-)减小,D不正确,答案选C。
考点:考查稀释对碳酸钠水解平衡的影响以及离子浓度变化判断
本题难度:一般
5、选择题 下表是在相同温度下,三种酸的一些数据,下列说法正确的是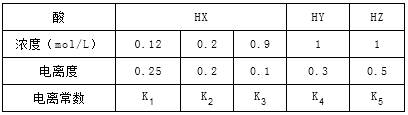
A.相同温度下,从HX的数据可以说明:弱电解质溶液浓度越低,电离度越大,且K1>K2>K3=0.1
B.室温时,若在NaZ溶液中加水,则c(Z-)/[c(HZ)×c(OH-)]的比值变小,若加少量盐酸,则比值变大
C.等物质的量的NaX、NaY和NaZ的混合,c(X-)+c(Y-)-2c(Z-)=2c(HZ)-c(HX)-c(HY),且c(Z-)<c(Y-)<c(X-)
D.相同温度下,K5>K4>K3
参考答案:D
本题解析:A、电离常数只受温度的影响,温度不变,电离平衡常数不变,即K1=K2=K3,错误;B、根据题意HZ是弱酸,NaZ是强碱弱酸盐,Ka=c(H+)×c(Z-)/c(HZ),Kw=c(H+)×c(OH-),c(Z-)/[c(HZ)×c(OH-)]=Ka×Kw,两个只受温度的影响,说法错误;C、根据数据,得出酸性强弱的顺序:HZ>HY>HX,酸性越强,水解程度越小,c(Z-)>c(Y-)>c(X-),错误;D、酸性越强,电离程度越强,电离常数越大,所以K5>K4>K3,正确。
考点:考查电离常数、盐类水解的规律等相关知识。
本题难度:困难
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高中化学知识点总结《气体的净化.. | |