| �߿�ʡ������ | |
|
|
| �߿�ʡ������ | |
|
|
|
�߿���ѧ֪ʶ���ܽᡶ��ѧ��Ӧ���ʡ����㹮�̣�2017�����°棩(��)
�ο��𰸣�C �����������ͼ����Կ�����������a��Ϊb,���ʵķ�Ӧ���ʼӿ죬�ﵽƽ������Ҫ��ʱ�����̣��������ʵ�ת���ʲ��䡣ֻ�м�������������⣬���ѡ����C�� �����Ѷȣ�һ�� 4������� ��ӦA��g��+B��s��?C��g������H��0����������������ʱ���ı�����һ��������������C�����ʣ� �ο��𰸣���1�������¶ȣ���ѧ��Ӧ���ʼӿ죬�ʴ�Ϊ���ӿ죻? ��������� �����Ѷȣ�һ�� 5������� ��12�֣���2L�ܱ������ڣ�800��ʱ��Ӧ��2NO(g)+O2(g)�P2NO2(g)��ϵ�У�n(NO)��ʱ��ı仯�����
��֪��K��300�棩��K(350��)���÷�Ӧ��_?�� (2)��ͼ�б�ʾNO2�ı仯��������?�� ��O2��ʾ��0~2s�ڸ÷�Ӧ��ƽ������v=?�� 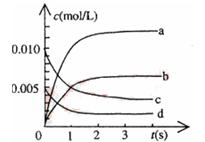 (3)��˵���÷�Ӧ�Ѵﵽƽ��״̬����?�� a��v(NO2)=2v(O2)? b��������ѹǿ���ֲ��� c��v��?(NO)=2v�� (O2)? d���������ܶȱ��ֲ���[ (4)Ϊʹ�÷�Ӧ�ķ�Ӧ����������ƽ��������Ӧ�����ƶ�����?�� a����ʱ�����NO2����? b���ʵ������¶� c������O2��Ũ��? d��ѡ���Ч���� �ο��𰸣� ����������� �����Ѷȣ�һ�� | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ���� �� С������ӡ�� �������� ���ر��� �����ض����� | |
| ��һƪ�����л�ѧ�ر�֪ʶ�㡶��������.. | |
| �����Ŀ |