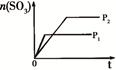
1、选择题 下列研究目的和示意图相符的是(? )
?
| A
| B
| C
| D
|
研
究
目
的
| 固定容积的密闭容器中,压强对反应:
2SO2(g)+O2(g)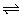 2SO3(g)的影响 2SO3(g)的影响
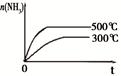
| 固定容积的密闭容器中,温度对反应:
N2(g)+3H2(g) 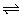 ?2NH3(g) ΔH< 0的影响 ?2NH3(g) ΔH< 0的影响
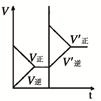
| 固定容积的密闭容器中,增大CO2浓度,对已达平衡的反应:
CO(g)+H2O(g)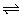 CO2(g)+H2(g)的影响 CO2(g)+H2(g)的影响
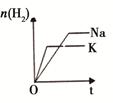
| 等质量Na、K 分别与足量水反应
|
示
意
图
| 
| 
| 
| 
|
?
2、填空题 在密闭容器中进行反应①Fe(s)+C02(g)  FeO(s)+CO(g) ΔH1=akJ・mol一
FeO(s)+CO(g) ΔH1=akJ・mol一
反应②2CO(g)+02(g)  2C02(g)?△H2="b" kJ・mol-
2C02(g)?△H2="b" kJ・mol-
反应③2Fe(s)+02(g)  2FeO(s)△H3
2FeO(s)△H3
(1) △H3=?(用含a、b的代数式表示)。
(2)反应①的化学平衡常数表达式K=?,已知500℃时反应①的平衡常数K=1.0,在此温度下2 L密闭容器中进行反应①,Fe和C02的起始量均为2.0 mol,达到平衡时CO2的转化率为??,CO的平衡浓度为?。
(3)将上述平衡体系升温至700℃,再次达到平衡时体系中CO的浓度是C02浓度的两倍,则a?0(填“>”、“<”或“=”)。为了加快化学反应速率且使体系中CO的物质的量增加,其他条件不变时,可以采取的措施有?(填序号)。
A.缩小反应器体积? B.再通入CO2? c.升高温度? D.使用合适的催化剂
(4)下列图像符合反应①的是?(填序号)(图中V是速率、φ为混合物中CO含量,T为温度)。

3、实验题 某化学学习小组借助下列装置(夹持装置已略)及相关试剂粗略测量空气中O2的体积百分数。
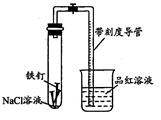
(1)实验前用碱液清洗铁钉,再用0.100mol/L的H2SO4溶液浸泡至有气泡产生。用H2SO4溶液浸泡的目的是_____ 。
(2)为尽量减小误差,下列操作的正确顺序是______ (填序号)。
①装人铁钉②插入注射器向铁钉表面滴入适量 NaCl溶液并打开止水夹③将导管口浸入品红溶液④塞 上单孔活塞⑤检查装置气密性
(3)实验中试管内发生的总反应为__ ____ ;用该实验方案测量空气中O2的体积百分数时应测量的数据是:①导管与试管内部空间总体积,②______ 。
(4) 实验时发现上述测量过程因反应较慢耗时较长,对其影响因素作如下分析,请补充 写出假设三:
假设一:电解质溶液的PH不同
假设二:NaCl溶液的浓度不同
假设三:
(5)借助上述实验装置,通过调节溶液的pH验证假设一,获得了如下实验数据:

①当pH=2时,没有观察到稳定液柱形成的原因是__ ____
②根据实验数据分析,为缩短实验测定时间,pH的最佳范围是______
③按上述实验装置,设计实验证明假设二。
第一步:___________ ;
第二步::相同温度下,加入系统表面积的铁钉,组装两套完全相同的上述装置,分别用注射器将NaCl溶液滴入铁钉表面;
第三步:记录形成稳定液柱所用时间和液柱的高度,比较分析数据得出结论。
4、选择题 在C(s)+CO2(g)=2CO(g)反应中,可使反应速率增大的措施是(?)
①增大压强;②增加炭的量;③通入CO2;④恒压下充入N2;⑤恒容下充入N2;⑥升温
①③④? B.②④⑥? C.①③⑥?D.③⑤⑥
5、选择题 下列关于化学反应速率的说法中正确的是( )
A.根据化学反应速率的大小可以知道化学反应进行的快慢
B.化学反应速率为0.8mol?L-1?s-1,是指1s时,物质的量浓度为0.8mol?L-1
C.对任何化学反应来说,反应速率越大化学现象越明显
D.化学反应速率是指一定时间内,任何一种反应物浓度的减少或任何一种生成物浓度的增加